Амилолитические препараты
Амилолитические препараты широко выпускаются в нашей стране и за рубежом. В основном это крупнотоннажное производство. Амилазы находят применение почти во всех областях, где перерабатывается крахмалсо-держащее сырье. Амилазы используют для осахаривания зернового и картофельного крахмала. Самым большим потребителем амилолитических ферментов является спиртовая и пивоваренная промышленности, где в настоящее время солод (проращенное зерно) успешно заменяется амилолитическими ферментными препаратами.
Источники получения амилаз
Амилазы очень широко распространены в природе. Они синтезируются многими микроорганизмами (бактерии, грибы, актиномицеты, дрожжи), животными и растениями. До развития ферментной промышленности главным промышленным источником получения амилаз в европейских странах было проросшее зерно (солод). Для медицинских целей амилазы получали из животного сырья. В настоящее время главным источником амилаз являются микроорганизмы, особенно бактерии, грибы и реже дрожжи.
Механизм действия и свойства амилаз
Субстратами для действия амилаз являются крахмал, состоящий из амилозы и амилопектина, продукты частичного гидролиза крахмала и гликоген.
Крахмал - растительный полисахарид с очень сложным строением. Это двухкомпонентное соединение, состоящее из 13-30% амилозы и 70-85% амилопектина. Оба компонента неоднородны, их молекулярная масса (М. м.) колеблется в широких пределах и зависит от природы крахмала. Амилоза - это неветвящийся полимер, в котором остатки глюкозы соединены a-1, 4-гликозидной связью; степень полимеризации около 2000. В «аномальных» амилозах с одной-двумя a-1, 6-связями полимеризация может возрасти до 6000 (рис.1). Амилоза практически не обладает восстанавливающей способностью, так как в каждой молекуле амилозы имеется только одна свободная альдегидная группа.
Молекула амилозы представляет собой растянутую спираль, шаг которой составляет 10,6 А и в каждый виток входит 3 остатка глюкозы. Максималь-

![]()

Рис 1. Строение амилозы:
а — амилоза без аномальных отклонений; б - схема возможных ветвлений амилозы; в — спираль амилозы в растворе с заключенными в ее полость молекулами йода.

Концевые звенья с
альдегидными группами 1 разветвление
- 2 разветвления 4 разветвления 8 развет

16 концевых звеньев
64 концевых
звена
Рис. 2.2. Амилопектин, схема дихотомического деления амилопектина (по К. Мейеру):
а - в плоскости; б - в пространстве.
ная длина молекулы амилозы достигает 7000 А. В растворе спираль сжимается за счет увеличения витка, в котором уже участвует 6 остатков глюкозы. При вхождении молекул йода в спираль амилозы возникает характерный синий цвет. Строго говорить о величине молекулы амилозы нельзя, т. е. даже из одного образца крахмала извлекается амилоза, с величиной молекулы от 500 до 2000 остатков глюкозы. Амилопектин имеет большую молекулярную массу, чем амилоза, и более сложное строение. Это ветвящийся полисахарид. Предполагается, амилопектин ветвится дихотомически, т. е. число концевых звеньев всегда на единицу больше числа звеньев, дающих ветвление, а сумма этих чисел дает общее число звеньев по всей цепи (см. рис. 2.2).
Механизм действия. К группе амилотических ферментов относятся a- и b-амилазы, глюкоамилаза, пуллуланаза, изоамилаза и некоторые другие ферменты. Амилазы бывают двух типов: эндо- и экзоамилазы. Четко выраженной эндоамилазой является а-амилаза, способная к разрыву внутримолекулярных связей в высокополимерных цепях субстрата.
Глюкоамилаза и b-амилаза являются экзоамилазами, т. е. ферментами, атакующими субстрат с нередуцирующего конца.
При изучении механизма действия амилаз имеются определенные сложности, и прежде всего они заключаются в том, что субстрат - крахмал неоднороден и имеет различные характеристики по степени полимеризации гли-козидной цепи и количеству ветвлений.
Реакции, катализируемые амилазами, имеют две стадии: короткую -предстационарную и длительную - стационарную. Во время первой стадии эндоамилаза быстро уменьшает молекулярную массу субстрата, образуя смесь линейных и разветвленных олигосахаридов. Второй этап реакции продолжается, пока продукты гидролиза не перестанут окрашиваться йодом; он протекает значительно медленнее и зависит от индивидуальных свойств фермента и его природы. Поэтому конечные продукты гидролиза а-амилазами могут быть различными. Первая стадия воздействия фермента на субстрат хотя и носит неупорядоченный характер, имеет для всех видов a-амилаз схожий механизм.
Существует две гипотезы о механизме действия экзоамилаз на субстрат. Первая гипотеза предполагает, что, воздействуя на субстрат по одноцепочечному или «молниеобразному» механизму, экзоамилаза образует фермент-субстратный комплекс с захватом нередуцирующего конца цепи.
Дальнейшее продвижение фермента по этой цепи происходит до полного ее гидролиза. По второй гипотезе (b- и глюкоамилаза действуют на субстрат путем механизма множественной атаки, т. е. фермент образует комплекс с молекулой субстрата, затем через несколько этапов этот комплекс распадается и фермент связывается с новой молекулой субстрата. Иными словами, при множественной атаке происходит нечто среднее между неупорядоченным механизмом и одноцепочечной, «молниеобразной» атакой. Для полного гидролиза по этому механизму одна
молекула субстрата должна образовывать много раз фермент-субстратные комплексы. При этом возможен гидролиз нескольких связей в одном каталитическом акте.
Механизм воздействия амилаз на субстрат может быть рассмотрен с нескольких позиций:
1) вид разрываемой связи (a-1,4 или a-1,6);
2) тип воздействия на субстрат (эндо- или экзо-);
3) влияние на скорость гидролиза степени полимеризации субстрата;
4) возможность гидролиза олигосахаридов;
4) способность фермента к множественной атаке субстрата.
Наличие признаков амилаз, отраженных в 3 и 4 позициях, при действии на линейные субстраты может свидетельствовать о существовании у этих ферментов подцентровой структуры. Вероятно, активный центр амилазы может состоять из нескольких подцентров, каждый из которых может вступать в контакты с глюкозным остатком. Энергия взаимодействия (А;), выраженная в единицах свободной энергии (кДж/моль), определяет подцентровое сродство фермента к субстрату. Это сродство индивидуально и может быть как положительным, так и отрицательным. Вероятность существования подцентровых структур амилаз помогает установить строение активного центра амилаз, дает более четкое объяснение субстратной специфичности, но не дает объяснений механизма гидролиза разветвленных субстратов.
a-Амилаза. а-Амилаза (а-1,4-глюкан-4-глюканогидролаза, КФ 3.2.1.1.) является эндоамилазой, вызывающей гидролитическое расщепление a-1,4-гли-козидных связей внутри высокополимеризованного субстрата. Фермент назван a-амилазой потому, что он высвобождает глюкозу в a-мутамерной форме.
а-Амилаза - водорастворимый белок, обладающий свойствами глобулина и имеющий М. м. 45 000-60 000. Своего рода исключением является a-амилаза В. macerans, которая имеет М. м. 130 000. Есть указания, что некоторые термостабильные a-амилазы имеют М. м. 14 000-15 000, но в их молекулах содержится в 2-3 раза больше атомов кальция.
Все а-амилазы относятся к металлоэнзимам, содержание в них Са колеблется от 1 до 30 г атом на 1 г моль фермента. Полное удаление кальция
приводит к инактивации фермента. Повторное введение кальция в среду может частично восстановить его активность. a-Амилаза В. subtilis с помощью иона цинка способна образовывать димерную форму, чего лишены другие a-амилазы. Все a-амилазы устойчивы к воздействию протеаз. Они богаты тирозином и триптофаном. Глютаминовая и аспарагиновая кислоты составляют 25% массы белка. Наличие этих кислот в а-амилазе связывают с их оса-харивающей способностью. Так, разжижающие a-амилазы не имеют сульфгидрильных групп, а осахаривающие содержат один остаток цистеина. Сравнительно мало или совсем отсутствуют в а-амилазах содержащие серу аминокислоты. Некоторые a-амилазы грибного происхождения имеют углеводный фрагмент, в состав которого могут входить манноза, ксилоза, гексозоамин, но функции его не установлены.
В зависимости от вида микроорганизма свойства ос-амилаз могут сильно отличаться не только по механизму воздействия на субстрат и конечным продуктам, но и по оптимальным условиям для проявления максимальной активности.
Действуя на целое крахмальное зерно, a-амилаза атакует его, разрыхляя поверхность и образуя каналы и бороздки, т.е. как бы раскалывает зерно на части. Клейстеризованный крахмал гидролизуется ею с образованием на окрашиваемые йодом продукты - в основном состоящие из низкомолекулярных декстринов. Процесс гидролиза крахмала многостадийный. В результате воздействия a-амилазы на первых стадиях процесса в гидролизате накапливаются декстрины, затем появляются неокрашивающиеся йодом тетра- и тримальтоза, которые очень медленно гидролизуются a-амилазой до ди- и моносахаридов.
Все a-амилазы проявляют наименьшее сродство к гидролизу концевых связей в субстрате. Некоторые же а-амилазы, особенно грибного происхождения, на второй стадии процесса гидролизуют субстрат более глубоко с образованием небольшого количества мальтозы и глюкозы. Схему гидролиза под действием а-амилазы можно записать следующим образом:
а-Амилаза
Крахмал,----------------> а-Декстрины + Мальтоза + Глюкоза
гликоген (много) (мало) (мало)
-Амилаза. b-Амилаза (a-1,4-глюкан мальтогидролаза, КФ 3.2.1.2) - активный белок, обладающий свойствами альбумина. Каталитический центр фермента содержит сульфгидрильные и карбоксильные группы и имидозольный цикл остатков гистидина. b-Амилаза -экзофермент концевого действия, проявляющий сродство к предпоследней -1,4-связи с нередуцирующего конца линейного участка амилозы и амилопектина.
В отличие от a-амилазы b-амилаза практически не гидролизует нативный крахмал, тогда как клейстеризованный крахмал гидролизуется ею с образованием мальтозы b-конфигурации, поэтому данная амилаза по аналогии с a-амилазой называется b-амилазой. Если гидролизу подвергается амилоза, то гидролиз идет полностью до мальтозы. Незначительное количество декстринов может образовываться при гидролизе «аномальных» амилоз, так как гидролиз b-амилазой идет только по линейной цепи до a-1,6-связей. Если субстратом для b-амилазы служит амилопектин, то гидролиз идет в значительно меньшей степени. b-Амилаза отщепляет фрагмент с нередуцирующего конца участка от внешних линейных ветвей, имеющих по 20-26 глюкозных остатков, с образованием 10—12молекул мальтозы. Гидролиз приостанавливается на предпоследней a-1,4-связи, граничащей с a-1,6-связью. В гидролизате накапливается 54-58% мальтозы, остальное составляют высокомолекулярные декстрины, содержащие значительное количество а-1,6-связей - так называемые b-декстрины. Действие b-амилазы на крахмал можно записать в виде следующей схемы:
b-Амилаза
Крахмал,----------------> Мальтоза + р-Декстрин
гликоген (54-58%) (42-46%)
b-Амилазы проявляют большую стабильность в отсутствие ионов Са2+. Молекулярная масса b-амилазы растений достаточно высока, она составляет от 50 000до 200 000. Фермент может состоять из одной или четырех
субъединиц до 50 000 каждая. Фермент содержит SH-группы и чувствителен к действию тяжелых металлов. Считается, что (b-ами-лаза обладает высокой способностью к множественной атаке субстрата. Для амилозы средней молекулярной массы в одном присоединении фермента к субстрату возможно отщепление до четырех остатков мальтозы. При увеличении молекулярной массы субстрата возможно и большее количество мест атаки.
Глюкоамилаза. Глюкоамилаза (а-1,4-глюкан глюкогидролаза, КФ 3.2.1.3.) широко распространена в природе. Она синтезируется многими микроорганизмами и образуется в животных тканях, особенно в печени, почках, плаценте кишечника и т. д. Фермент в литературе известен под различными названиями: амилоглюкозидаза, g-амилаза, лизосомальная a-глюкозидаза, кислая мальтаза, матулаза и экзо-1,4-a-глюкозидаза. Глюкоамилаза катализирует последовательное отщепление концевых остатков a-D-глюкозы с нередуцирующих концов субстрата. Это фермент с экзогенным механизмом воздействия на субстрат. Многие глюкоамилазы обладают способностью так же быстро, как и a-1,4-связь, гидролизовать a-1,6-глюкозидные связи. Но это происходит только в том случае, когда за a-1,6-связью следует a-1,4-связь, поэтому декстран ими не гидролизуется. Отличительной особенностью глюкоамилаз является способность в десятки раз быстрее гидролизовать высокополимеризованный субстрат, чем олиго-и дисахариды.
В литературе высказывается мнение, что механизм атаки субстрата глюкоамилазой может быть двух типов: либо одно-цепочечный, либо множественной атаки, и что активный центр имеет под-центровую структуру.
Почти все глюкоамилазы являются гликопротеидами, содержащими от 5 до 35% углеводов, которые состоят из олиго-, ди- и моносахаридов. Углеводный компонент может быть целостным фрагментом или же разбитым на индивидуальные соединения, которые прикрепляются к белку через треонин и серин. Например, у глюкоамилазы A. niger их 20. Большинство известных глюкоамилаз имеет оптимум рН при 4,5-5,2, реже - при 5,7-6,0, в основном для дрожжевых глюкоамилаз.
РН-стабильность микробных глюкоамилаз лежит в широком диапазоне -от 2,5 до 9. Термостабильность глюкоамилаз лежит в интервале от 30 до 45°С и редко повышается до 55-60°С. Глюкоамилазы различного происхождения заметно отличаются по молекулярной массе, которая, по данным различных авторов, имеет значения от 48 000 до 210 000. Следует заметить, что далеко не все микробные глюкоамилазы способы полностью гидролизовать крахмал до глюкозы. Еще в 60-х годах И.Фукумото предложил все микробные глюкоамилазы разделить на два типа:
1) полностью гидролизующие крахмал до глюкозы и
2) гидролизующие крахмал до глюкозы на 80-85%.
В то время предполагалось, что степень гидролиза зависит только от свойств глюкоамилаз и их происхождения. Позже было показано, что при росте культуры параллельно накапливаются и другие амилолитические ферменты, обладающие не только гидролитическим, но и трансферазным действием. Это гликозилтрансфераза и a-амилаза. Даже в случае, если система открытая и продукт гидролиза (глюкоза) постоянно удаляется из системы, процесс может дойти до полного гидролиза крахмала до глюкозы. Если же система закрытая и концентрация субстрата велика, то при достижении определенной концентрации глюкозы в реакционной среде в результате переноса глюкозильных остатков на глюкозу, ди- и олигосахариды начинают накапливаться изомальтоза, паноза, нигероза, изомальтотриоза и другие сахара, которые имеют горький вкус. В результате процесс не может дойти до полного превращения крахмала в глюкозу и возникает ошибочное представление, что глюкоамилаза не полностью гидролизует крахмал. Сама же глюкоамилаза может проявлять небольшую трансферазную активность, но только при концентрации глюкозы свыше 60-70%. Поэтому ранее принятое деление глюкоамилаз на два типа следует считать необоснованным.
ТЕХНОЛОГИЧЕСКИЕ СХЕМЫ И РЕЖИМ ПОЛУЧЕНИЯ СПИРТА
Технология этилового спирта из крахмалистого сырья основана на ферментативном гидролизе зернового или картофельного крахмала и сбраживании образующихся сахаров дрожжевыми микроорганизмами, т.е. является биохимической технологией.
Процесс получения спирта из зерно-картофельного сырья включает следующие стадии: очистка и подготовка сырья, водно-тепловая обработка его, осахаривание разваренной массы и охлаждение сусла, приготовление засевной культуры дрожжей, сбраживание сусла, перегонка бражки и ректификация спирта.
Производство спирта из крахмалистого сырья осуществляется по периодической, полунепрерывной и непрерывной схемам. По периодической схеме с использованием разварников Генце получали этиловый спирт с конца XIX в. В настоящее время эта схема осталась только на некоторых спиртовых заводах малой мощности (до 800 дал). Полунепрерывная схема производства, основанная на использовании периодически действующих аппаратов, впервые была внедрена на заводах СССР в 1917—1950 гг. По этой схеме до сих пор работают около 15—20% спиртовых заводов страны.
ПРИНЦИПИАЛЬНАЯ ТЕХНОЛОГИЧЕСКАЯ СХЕМА ПОЛУЧЕНИЯ ЭТИЛОВОГО СПИРТА ИЗ КРАХМАЛИСТОГО СЫРЬЯ
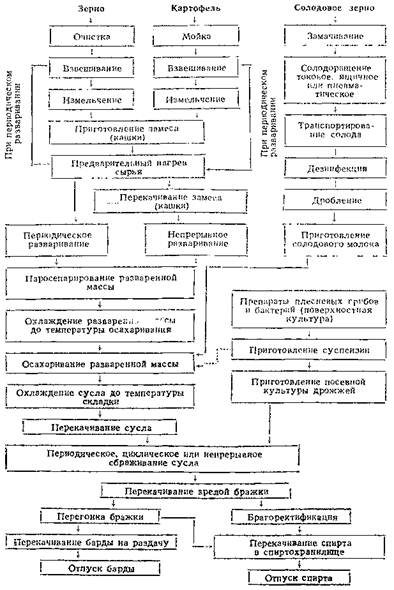
ОСАХАРИВАЮЩИЕ МАТЕРИАЛЫ
Крахмал, растворенный при разваривании зерна и картофеля, гидролизуют (осахаривают) амилолитическими ферментами зернового солода или культур микроорганизмов, преимущественно микроскопических (плесневых) грибов и бактерий.
Амилолитические ферменты содержатся во многих высших растениях, но наиболее богато ими пророщенное в определенных условиях зерно растений семейства мятликовых (злаков), называемое солодом. Способность солода осахаривать крахмал известна с древнейших времен, и с тех пор солод используется при получении спирта. Также давно известно свойство микроскопических грибов осахаривать крахмал. С их помощью восточные народы приготовляли различные охмеляющие напитки.
Культуры микроскопических грибов или ферментные пре параты применяют в спиртовой промышленности большинства зарубежных стран, причем в основном в виде концентрированных сиропообразных препаратов или сухого порошка, реже — в виде культуральной жидкости.
Культуры микроскопических грибов имеют ряд преимуществ по сравнению с солодом. Их выращивают на пшеничных отрубях или в составе питательной среды используют обычную кукурузную муку, тогда как для приготовления солода расходуется 14...20 % кондиционного (96 % проростаемости) зерна в расчете на массу крахмала сырья.
При солодоращении теряется 16...18 % крахмала, часть крахмала солода в процессе производства спирта остается неосахаренной и, следовательно, не сбраживается. Кроме того, с солодом вносятся в сусло посторонние микроорганизмы, вследствие чего в большей мере протекают и другие виды брожения, отрицательно отражающиеся на выходе спирта. В случае применения смеси солодов из различных злаков с целью полного осахаривания крахмала работа солодовен усложняется.
Культуры микроскопических грибов содержат комплекс амилолитических ферментов, отличающихся от ферментов солода и позволяющих глубже и полнее гидролизовать крахмал. В микроскопических грибах активнее целлюлозолитические ферменты, расщепляющие гемицеллюлозы до сахаров, часть которых сбраживается дрожжами, при этом повышается выход спирта.
С помощью культур микроскопических грибов можно увеличить концентрацию ферментов и таким образом сократить продолжительность осахаривания и последующего дображивания сусла в 2...3 раза.
Микроскопические грибы быстро размножаются, для выращивания поверхностной культуры достаточно около 1,5 сут, проращивание же зерна для получения солода длится 9... 10 сут. Глубинные культуры выращивают в стерильных условиях, что обеспечивает «чистоту» процесса спиртового брожения.
Действие солода и культур микроскопических грибов не ограничивается осахариванием крахмала, они еще способствуют накоплению в сусле достаточного количества органического азота для питания дрожжей и частичному растворению клеточных стенок эндосперма сырья. В осуществлении этих процессов, а также в выращивании солода и микроскопических грибов участвуют многочисленные ферменты, поэтому необходимо знание их химической природы, строения и механизма действия.
ПОЛУЧЕНИЕ СОЛОДА
Технология солода складывается из следующих основных процессов: замачивание и проращивание зерна; сушка солода и удаление ростков. На отечественных спиртовых заводах для осахаривания используют сырцовый — несушеный солод (неправильно называемый «зеленым»). Этот солод не может долго храниться, поэтому на каждом спиртовом заводе его готовят в количествах, необходимых для текущей работы.
ЗАМАЧИВАНИЕ ЗЕРНА
Основная цель замачивания — увлажнить зерно; дополнительная — отмыть от остатков пыли, удалить легкие зерновые и незерновые примеси и подавить микроорганизмы. Замачивание ведут с применением воздуха и воды, чередуя насыщение зерна водой и аэрацию.
Во время замачивания протекают физико-химические и биохимические процессы, приводящие к глубоким изменениям в зерне.
ФИЗИКО-ХИМИЧЕСКИЕ ПРОЦЕССЫ ПРИ ЗАМАЧИВАНИИ ЗЕРНА
Зерно прорастает нормально при влажности 40...46 %. При меньшей влажности ростки быстро увядают, накапливается мало ферментов, эндосперм плохо и неравномерно растворяется. Переувлажненное зерно долго не начинает прорастать, а затем быстро трогается в рост с большим выделением теплоты. Замачивание обычно заканчивается по достижении влажности 38...40 %, но обильно орошают зерно водой во время проращивания.
Вода поступает в зерно через плодовую и семенную оболочки, обладающие полупроницаемостью, поэтому в процессе замачивания главную роль играют ультрафильтрация и осмодиффузия. Цветочная пленка (мякинная оболочка) в начале замачивания непроницаема, и вода впитывается по тонким капиллярам — трахеидам зародышевой части, не покрытой этой оболочкой. Сорбируясь крахмалом, белками и другими высокополимерами и растворяя минеральные вещества, через полупроницаемые стенки клеток зародыша и эндосперма вода проникает внутрь зерна.
Со временем вследствие вымывания инкрустирующих веществ становится проницаемой и мякинная оболочка.
В нормально замоченном зерне ячменная влага распределена неравномерно. Наибольшая влажность (около 47 %) в основании — в зоне расположения зародыша; в самом зародыше влажность еще выше (68...75 %). В середине зерна влажность 38 %, в кончике 39 %.
Скорость замачивания зависит от структуры, размера зерна и температуры. Пленчатое, высокобелковое и крупное зерно обычно увлажняются медленнее, чем голое, низкобелковое и мелкое, хотя нередки исключения из этого правила. Зерно, выращенное в сухом жарком климате, впитывает влагу хуже зерна, полученного во влажном умеренном теплом климате. С повышением температуры скорость замачивания возрастает
Зерно большинства культур замачивают при 18...20 °С (смеси зерна и воды). При более высокой температуре необходимы частая смена воды, энергичное аэрирование, тщательное подавление микрофлоры, что усложняет управление процессом. Исключение составляет просо, которое насыщается влагой труднее, поэтому температуру замачивания его поддерживают в пределах 25...30 °С.
В воде с высокой жесткостью (14... 15 мгэкв/л) и большой щелочностью замачивание замедляется. Такое же действие оказывают хлориды; сульфаты, наоборот, ускоряют замачивание.
Во время замачивания зерно набухает, увеличиваясь в объеме, например, на 40...45 % (ячмень). Из твердого и хрупкого оно становится мягким и эластичным.
БИОХИМИЧЕСКИЕ ПРОЦЕССЫ ПРИ ЗАМАЧИВАНИИ ЗЕРНА
В результате увеличения влажности зерна при замачивании резко усиливается жизнедеятельность и в первую очередь дыхание зерна, сопровождающееся потребностью в кислороде. Вместе с тем запас кислорода в воде очень быстро уменьшается, напри-
мер при замачивании ячменя на 60...80 мин он исчезает, поэтому обеспечение зерна кислородом затруднено. Проникновению кислорода в зерно через зародыш (в начале замачивания) препятствует щиток, а через оболочки впоследствии — большое количество воды в тканях. Диффузия кислорода в воде примерно в 10 000 раз медленнее, чем в газе; кроме того, растворимость его в воде в 40 раз меньше, чем диоксида углерода. Недостаток кислорода в процессе замачивания подтверждается и значением дыхательного коэффициента, который выше единицы (около 1,07), а через 8 ч от начала замачивания равен 1,38, т. е. наблюдается уже анаэробное дыхание.
При кислородном голодании образуется этиловый спирт, вредно влияющий на жизнеспособность зародыша. В таких условиях частично нарушается структура тканей и зерно легко переувлажняется. Во время последующего проращивания требуются длительная перестройка типа дыхания, сжигание спирта и других метаболитов, на образование которых были затрачены углеводы. Отсюда следует, что с самого начала замачивания должны быть созданы условия для нормального дыхания зерна.
При замачивании зерна одновременно с усилением дыхания происходит глубокая перестройка всего ферментного комплекса.
ПРОРАЩИВАНИЕ ЗЕРНА
Цель солодоращения — накопление ферментов, растворение межклеточных пластинок и стенок клеток эндосперма, что необходимо для снабжения развивающегося зародыша питательными веществами и перехода ферментов в сусло.
Зерно проращивают в таких условиях, чтобы расход крахмала
на дыхание и образование новых вегетативных органов был минимальным, при возможно меньшем обсеменении микроорганизмами, особенно кислотообразующими.
МОРФОЛОГИЧЕСКИЕ И ЦИТОЛИТИЧЕСКИЕ ИЗМЕНЕНИЯ ЗЕРНА
При проращивании в зерне происходят процессы распада и синтеза. В эндосперме гидролизуются резервные вещества — крахмал, белки, а также пектиновые вещества, гемицеллюлозы, целлюлоза; образующиеся растворимые продукты поступают через щиток в зародыш. В результате процессов синтеза из зародыша вырастают стебелек и корешки.
БИОХИМИЧЕСКИЕ ИЗМЕНЕНИЯ ЗЕРНА
Ферменты синтезируются в вегетативных частях растения — листьях и стеблях — и уже из них мигрируют в созревающее зерно. По исследованиям А. Н. Баха и А. И. Опарина, активность ферментов в зерне вначале увеличивается, в период молочной спелости достигает максимума, в период восковой спелости снижается и, наконец, во вполне созревшем зерне еле проявляется. При проращивании зерна активность ферментов вновь увеличивается, достигая даже значительно большей величины, чем в период молочной спелости.
Понижение активности амилаз при созревании зерна объясняется связыванием их с белками. В таком, зимогенном, состоянии амилазы нерастворимы и потому неактивны. Активность их восстанавливается после воздействия протеаз, освобождающих амилазы из зимогена.
В созревающем зерне ячменя, ржи, пшеницы и овса присутствуют a- и b-амилазы, но в зрелом зерне обнаруживаются лишь следы b-амилазы. Заметное содержание свободной a-амилазы найдено в зерне ржи и овса. В пророщенном зерне всех этих культур содержание р-амилазы не превышает таковое при действии папаина на исходное зерно, т. е. р-амилаза накапливается в солоде в результате освобождения из зимогена. Полагают, что ос-амилаза накапливается таким же путем и частично синтезируется.
Динамика изменения ферментативной активности ячменя при его проращивании (по Г. И. Фертману и А. Н. Лазаревой) показана на рис. 3. Видно, что величины АС и ДС достигают максимального значения на 10-е сутки, по другим данным, у ржи — на 7...8-е сутки. Декстринолитическая способность возрастает v овса на 10... 12-е, у
проса — на 5...6-е сутки. Исходя из этого, устанавливают и продолжительность солодоращения.
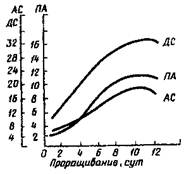
Рис. 3. График изменения ферментативной активности в прорастающем ячмене
В солоде амилолитические ферменты распределены неравномерно: в ячменном приблизительно 70 % амилаз локализовано в нижней части эндосперма, прилегающей к щитку, в верхней части их около 25, в щитке 4, в стебельке и корешках 1 %.
Цитолитические ферменты в процессе проращивания зерна также активируются, и активность их возрастает до определенного времени, у ячменя — до 5...7 сут. Наибольшей активности цитазы соответствует переход твердого состояния мучнистого тела в рыхлое, когда эндосперм легко может быть растерт между пальцами.
Главная роль в растворении клеточных стенок принадлежит гемицеллюлазам и пектиназам. Основной составной частью ге-мицеллюлоз ячменя является b-глюкан, гидролиз которого катализируется эндо-b-глюканазой. Меньшая роль принадлежит ара-бинозидазе и ксиланазе.
В зерне злаков из протеиназ содержится фермент типа папаина, из пептидаз — аминопептидазы, карбоксипептидазы и дипептидазы.
В результате действия протеиназ из зимогена освобождаются амилазы, под действием пептидаз накапливаются аминокислоты, главным образом аспарагиновая и глутаминовая. Активность протеаз возрастает в процессе солодоращения соответственно увеличению активности амилаз
Протеиназы ячменя, как и папаин, в зависимости от природы гидролизуемого белка могут проявлять свою активность при рН 3,8; 6,3 и 8,6, в соответствии с чем их подразделяют на кислые, нейтральные и щелочные. При солодоращении наибольшую каталитическую активность проявляют кислые протеиназы, активаторами которых служат сульфгидрильные соединения, содержащие группу —Н, цистин и восстановленный глютатион. В первые сутки проращивания зерна количество глютатиона значительно увеличивается, причем в зародыше более энергично, чем в эндосперме. В последующие сутки накопление глютатиона в зародыше происходит медленнее, но все время в зародыше его больше, чем в эндосперме.
Активность кислой протеиназы в продолжение солодоращения возрастает приблизительно в 40 раз. Пептидазная активность проявляется также сильно, но позже протеиназной.
К концу проращивания в зерне накапливаются довольно активные липаза и фосфатаза (фитаза, нуклеотидаза). Активность фосфатазы тем выше, чем ниже температура солодоращения.
По данным А. Н. Баха и А. И. Опарина, в зерне активность ферментов дыхания — оксидазы, пероксидазы и каталазы — выше активности гидролитических ферментов. В результате проращивания повышается активность обеих групп ферментов, но соотношение их активности резко изменяется в обратную сторону и тем сильнее, чем ниже температура. Поэтому в процессе солодоращения накапливается значительное количество гидролитических ферментов при сравнительно небольших тратах крахмала на дыхание.
ИЗМЕНЕНИЕ ХИМИЧЕСКОГО СОСТАВА ЗЕРНА
Несмотря на то что солодоращение протекает при сравнительно низких температурах, сильно отличающихся от оптимальных для действия ферментов, за время проращивания зерна происходят существенные изменения его химического состава.
Наибольшие преобразования претерпевает крахмал — основной резервный углевод зерна. Приблизительно 20 % от всего его количества гидролизуется: из них 8...9 % расходуется на дыхание, 3...4 % на построение стебля и корней и 8... 10 % остается в виде сахара, придающего солоду сладкий вкус.
Свободные сахара состоят главным образом из сахарозы, ин-вертного сахара и мальтозы. При температуре проращивания 15...16 °С образуются преимущественно сахароза и продукты ее гидролиза, при температуре 20...23 °С — мальтоза.
В нерастворенных гранулах крахмала при рассмотрении под микроскопом хорошо видны канальцы и повреждения поверхности, что является результатом действия амилаз. Размер гранул несколько уменьшается, повышается содержание амилозы, внешние цепи амилопектина укорачиваются. Температура клейс-теризации возрастает приблизительно на 4 С, а вязкость клейстера, наоборот, понижается.
Количество целлюлозы в зерне и солоде почти одинаково. Это объясняется тем, что наряду с растворением клеточных стенок эндосперма примерно такое же количество клетчатки образуется в новых вегетативных органах. Количество пентозанов в солоде на 2...3 % больше, чем в исходном зерне. Большая часть пентозанов растворима в воде и состоит не только из высокомолекулярных продуктов гидролиза, но и из моносахаридов (ксилозы, арабинозы).
Белковые вещества также претерпевают значительные изменения. Присуществующих способах производства спирта азотистое питание для дрожжей накапливается в основном процессе солодоращения. Некоторое количество растворимого азота образуется и при осахаривании разваренной массы, но оно относительно невелико.
Изменения состава белковых веществ ячменя и солода характеризуют данные, приведенные в табл. 1. Наиболее сильному гидролизу подвергается гордеин, несколько меньшему — глютелин; количество альбумина и глобулина почти не изменяется. Одновременно в 4...5 раз увеличивается содержание аминокислот. Об их составе некоторое представление может дать анализ ячменя и пивоваренного солода.
Содержание общего азота в зерне и солоде, %
| Белковые вещества | Ячмень | Солод |
Гордеин Глютелин Глобулин Альбумин Протеазы Аминокислоты | 36 30 10 12 5 7 | 17 21 11 10 9 32 |
Общее содержание азота на протяжении всего периода соло-доращения остается практически таким же, содержание аминного азота резко возрастает на 6...8-е сутки, а затем темпы роста замедляются. Белки исходного ячменя гидролизуются примерно на 55 %, из которых около 23 % сосредоточивается в проростках в виде качественно иных белков.
В процессе солодоращения содержание жиров уменьшается на 10...30 %. От фосфорорганических соединений отщепляются фосфаты. Образуются продукты неполного окисления углеводов — лимонная, щавелевая, молочная и другие органические кислоты, которые вместе с аминокислотами повышают общую кислотность, например с 1,5...2,5 мл 1 н. раствора NaOH на 100 г ячменя до 4,4...7,5 мл на 100 г солода. Однако значения рН в вытяжках из ячменя и солода вследствие буферных свойств мало различаются, но буферная емкость вытяжки из солода на 20...40 % больше.
При солодоращении освобождается инозит и возрастает содержание других витаминов — тиамина и рибофлавина, имеющих важное значение для жизнедеятельности и бродильной энергии дрожжей. Образуются эфиры и другие соединения, придающие солоду специфический запах: свежих огурцов — ячменному, стручков акации, медовый или яблочный — просяному и т. д.
ИНТЕНСИФИКАЦИЯ ПРОЦЕССА СОЛОДОРАЩЕНИЯ
Для интенсификации солодоращения с сокращением срока проращивания и повышением ферментативной активности в спиртовой промышленности применяют биостимуляторы — гиб-берелловую кислоту и комплексный ферментный препарат МЭК-1.
Гибберелловую кислоту используют в виде водного раствора при поливе зеленого солода в процессе выращивания, а также при замачивании зерна перед солодоращением. При поливе расход гибберелловой кислоты (в пересчете на чистое ее количество) — 600 мг/т (ячмень, рожь и овес) и 400 мг/т (просо). Если
эту кислоту добавляют на стадии замачивания зерна, то расход ее увеличивается и составляет 660...800 мг/т.
При использовании гибберелловой кислоты продолжительность выращивания ячменного и овсяного солода 8...9 сут. Ферментативная активность зеленого солода, обработанного гибберелловой кислотой, повышается не менее чем на 15 % по сравнению с необработанным солодом.
Для интенсификации солодоращения нормального зерна, а также при получении солода из нестандартного зерна в целях повышения прорастаемости и увеличения ферментативной активности в качестве биостимулятора кроме гибберелловой кислоты применяют комплексный ферментный препарат МЭК-1. Под его действием интенсифицируются процессы растворения мучнистой части зерна, образования амилолитических ферментов при проращивании, в результате чего продолжительность солодоращения сокращается с 10...12 до 6...7 сут.
В комплексный ферментный препарат МЭК-1 входят Амилосубтилин Г1Ох и Амилоразин П1Ох.
Препарат МЭК-1 (мультиэнзимная композиция, тип I) представляет собой порошок светло-бежевого цвета влажностью 12...13 %. Амилолитическая активность препарата (АС) 2650 ед/г, протеолитическая (ПС) — 30 ед/г. Расход МЭК-1 составляет 50 г стандартного препарата на 1 т солодового зерна при замачивании. Препарат применяют в виде рабочего водного раствора (50... 100 г препарата растворяют в 10 л воды). Рабочий раствор используют не только для замачивания, но и для полива при проращивании из расчета 200 л на I т солодового ячменя.
