Теоретическая часть.
Вода является слабым электролитом. Обратимый процесс диссоциации этого электролита можно представить следующим уравнением:
Н2О D Н+ + ОН-
Значение константы диссоциации позволяет судить о том, что равновесие процесса диссоциации воды смещено в сторону исходных веществ.
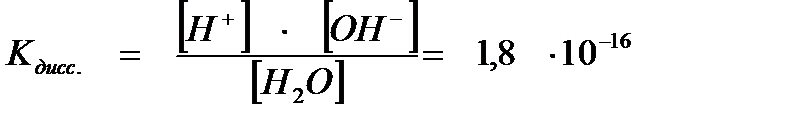
Концентрацию воды [Н2О] в знаменателе предыдущей дроби можно считать величиной постоянной и равной:
[Н2О] = = 55,56 моль/л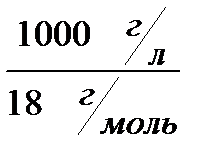
Таким образом,
[Н2О] ∙ Кдисс.= 55,56 ∙ 1,8 ∙ 10-16 = 10-14
Эту величину, представляющую собой произведение концентраций ионов водорода на концентрацию ионов гидроксила называют ионным произведением воды, или константой воды Kводы:
Kводы = [Н+] ∙ [ОН ] = 10 -14
Kw является постоянной величиной как для чистой воды, так и для разбавленных растворов любых электролитов.
Величина ионного произведения воды увеличивается при повышении температуры.
В чистой воде концентрации гидроксид-ионов и ионов водорода равны:
[Н+] = [ОН- ] = √KW= √10-14 = 10 -7 моль/л
Для оценки реакции среды была введена специальная величина - водородный показатель среды, или рН представляющая собой логарифм концентрации ионов Н+ с обратным знаком.
рН = - lg [H+]
Для чистой воды:
рН = - lg 10 -7 = 7
Если в растворе концентрация ионов Н+ больше, чем 10-7 моль/л, то рН такого раствора будет меньше 7, что является показателем кислой среды раствора.
Если [Н+] < 10 -7 моль/л, то рН > 7 и раствор имеет щелочную реакцию среды.
| Величина рН | Концентрация, моль/л | Среда | |
| ионов водорода | гидроксид – ионов | ||
| < 7 | > 10 -7 | < 10 -7 | Кислая |
| =7 | = 10 -7 | =10 7 | Нейтральная |
| > 7 | <10 -7 | > 10 -7 | Щелочная |
Величина концентрации (активности) ионов водорода в растворе определяется, в основном, двумя методами: колориметрическим и потенциометрическим.