Квантовые числа
Теория строения атома
- Атом состоит из ядра и электронной оболочки.
- Электронная оболочка — совокупность всех электронов в данном атоме.
- Электрон не имеет определенной траектории движения.
- Речь идет о вероятности нахождения электрона в разных частях атомного пространства.
Часть атомного пространства в которой вероятность нахождения электрона наибольшая называется атомной орбиталью.
Квантовые числа
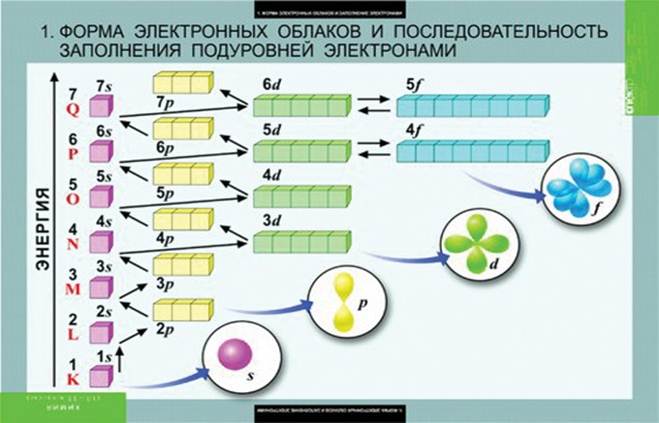
- Главное квантовое число n — характеризует энергию и размер орбитали и электронного облака. n=1,2,3...бесконечность. Совокупность орбиталей, которые имеют одинаковое значение главного квантового числа — энергетический уровень.
- Побочное (орбитальное) квантовое число l = 0,1,2,3...n-1. Орбитали, для которых l=0, имеют форму шара и называются s-орбиталями. Орбитали, для которых l=1, имеют форму гантели и называются p-орбиталями.
- Магнитное квантовое число ml = -l...0...+l. Характеризует направление орбиталей (электронных облаков) в пространстве.
- Спиновое квантовое число (спин) ms= +1/2, -1/2. Характеризует вращение электрона вокруг своей оси.
Принцип Паули — в атоме не может быть двух электронов с одинаковым набором четырех квантовых чисел. Следовательно, на одной орбитали не может быть больше двух электронов.
Электроны на одной орбитали с противоположными спинами называются спаренными.
Правило Гунда — на одном подуровне электроны располагаются так, чтобы абсолютное значение суммы спиновых квантовых чисел было максимальным.