Вспомогательные вещества
Назначение.Почти все известные в настоящее время лекарственные формы изготавливают с использованием вспомогательных дополнительных веществ. Вспомогательные вещества должны быть
* Краснюк И. И. Фармацевтическая гомеопатия. — М.: Издательский центр «Академия», 2005. — С. 37.
разрешены к медицинскому применению соответствующими нормативными документами: ГФ, ФС или специальными ОСТами.
Создание эффективных лекарственных препаратов требует применения большого числа вспомогательных веществ. До недавнего времени к вспомогательным веществам предъявляли требования фармакологической и химической индифферентности. Однако выяснилось, что эти вещества могут в значительной степени влиять на фармакологическую активность: усиливать действие лекарственных веществ или снижать их активность, изменять характер действия по разным причинам. При использовании вспомогательных веществ можно регулировать фармакодинамику лекарственных веществ (совокупность эффектов, вызываемых лекарственным веществом) и их фармакокинетику (изменение во времени концентрации лекарственных веществ в биологических жидкостях, органах и тканях).
Механизм влияния вспомогательных веществ на лекарственный препарат может быть обусловлен следующими факторами:
влиянием как дисперсной системы (стабилизация суспензий, эмульсий) на физико-химические свойства лекарственных веществ (средств) или лекарственной формы;
взаимодействием вспомогательных веществ с лекарственными (химическое взаимодействие, комплексообразование, адсорбция).
Так, например, мази, содержащие антибиотики и изготовленные на вазелине, в силу плохой резорбции малоэффективны. В данном случае необходима основа, включающая 6 частей вазелина и 4 части ланолина безводного, которую и используют в настоящее время для изготовления многих мазей с антибиотиками. Пилюли с солями алкалоидов (например, с атропина сульфатом) неэффективны, если в качестве вспомогательных веществ использовать порошки из лекарственного растительного сырья (из-за прочной адсорбции алкалоидов растительной клетчаткой).
Правильным подбором вспомогательных веществ можно локализовать действие лекарственных средств. Например, для действия мази на эпидермис кожи используют вазелин, так как он не обладает способностью проникать в более глубокие слои кожи. Напротив, для таких лекарственных веществ, как гормоны, калия йодид и другие, которые должны оказывать общее действие на организм, в качестве основы мазей используют соответствующие вещества, чаще всего их комбинации, которые повышают проницаемость клеточных мембран. Диметилсульфоксид (димексид), добавленный в глазные капли, ускоряет проникновение антибиотиков в ткани глаза. Использование метил целлюлозы позволяет удерживать лекарственные вещества в тканях длительное время, что обеспечивает их пролонгированное действие, которое необходимо при многих хронических заболеваниях. Так, в офтальмологии при глаукоме (повышенное внутриглазное давле-
ние) для ликвидации острого приступа используют глазные капли пилокарпина гидрохлорид, приготовленные только на воде. Затем для поддержания лечебной концентрации применяют (в течение определенного времени) те же глазные капли, но с добавлением пролонгирующих компонентов: метилцеллюлозы (МЦ), поливинола и т. п.
Вспомогательные вещества влияют не только на терапевтическую эффективность лекарственного вещества, но и на физико-химические характеристики лекарственных форм в процессе их изготовления и хранения. Добавление различных стабилизирующих веществ обеспечивает высокую эффективность лекарственных препаратов в течение длительного времени, что имеет не только большое медицинское, но и экономическое значение, так как позволяет увеличить срок годности лекарственных препаратов.
Вспомогательные вещества являются обязательными ингредиентами почти всех лекарственных препаратов и при использовании вступают в контакт с органами и тканями организма, поэтому к ним предъявляются определенные требования. Многие вспомогательные вещества поступают от различных предприятий (химической, пищевой промышленности и т. д. ), поэтому требования к ним должны быть едиными. Многие вспомогательные вещества включены в Государственный реестр лекарственных средств (документ, в который вносят сведения о средствах, разрешенных к применению и производству в стране), ФС, регламентирующие качество вспомогательных веществ, ГОСТы.
В медицине и фармации применяют только те вещества, которые разрешены Фармакологическим и Фармакопейным комитетами Минздравсоцразвития России.
Вспомогательные вещества оказывают значительное влияние на лекарственный препарат в целом (табл. 5. 2).
К вспомогательным веществам предъявляются высокие требования. Они должны быть;
биологически безвредными (по возможности, биологически полезными), не токсичными, не вызывать аллергических реакций;
химически индифферентными по отношению к веществам, входящим в состав препарата, материалам технологического оборудования, упаковочным и укупорочным материалам, и к факторам окружающей среды в процессе изготовления препарата и при хранении;
должны соответствовать по формообразующим свойствам особенностям изготовляемой лекарственной формы, придавать ей требуемые свойства: структурно-механические, физико-химические;
проявлять необходимые функциональные свойства (стабилизирующие, корригирующие и т. п. ) при минимальном содержании в препарате;
| Влияние вспомогательных веществ на лекарственные препараты | |
| Влияние на фармакологическую активность | Влияние на качество и стабильность |
| Усиление или ослабление (сни- жение активности) лекарствен- ного средства. Обеспечение местного действия или общего воздействия на орга- низм. Изменение скорости наступле- ния эффекта (ускорение или пролонгирование действия). Обеспечение направленного транспорта или регулируемого высвобождения лекарственных веществ | Обеспечение стабильности: антимикробной; химической; физико-химической (термодина- мической). Оптимизация технологических показателей (вязкости, раствори- мости, сыпучести, однородности). Корригирование органолепти- ческих свойств лекарственного препарата (улучшение вкуса. запаха, цвета) |
способствовать проявлению требуемого фармакологического эффекта (обеспечивать биологическую доступность);
быть экономически выгодными (экономически целесообразными);
не должны ухудшать физико-химические и структурно-механические свойства лекарственного препарата при хранении;
подвергаться микробной контаминации, не способствовать микробной контаминации или предотвращать микробную контаминацию лекарственного препарата; выдерживать в случае необходимости стерилизацию;
оказывать отрицательного влияния на органолептические свойства препарата или улучшать их.
Номенклатура вспомогательных веществ, используемых в технологии лекарственных форм, весьма многочисленна, поэтому для систематизации и облегчения их дальнейшего изучения и правильного подбора целесообразна их классификация. Однако по разным причинам (разнообразие химической структуры, влияние на лекарственные формы — стабильность, пролонгирование, исправление вкуса, и их терапевтическую эффективность), предлагаемые классификации не могут считаться совершенными.
Классификация вспомогательных веществ.Вспомогательные вещества классифицируют: по происхождению, размеру (величине) молекул, а также функциональной роли в лекарственной форме.
По происхождению различают природные, синтетические и полусинтетические вещества (табл. 5. 3).
| Таблица 5. 3 | |||
| Классификация вспомогательных веществ | |||
| Природные вещества | Примеры | Синтетические и полусинтети- ческие вещества | Примеры |
| Органи- ческие | Белки, жиры, полисахариды, спирты, эфиры, углеводороды и др. | Органические | ПЭГ, поливи- нол, поливинил- пирролидон, твины, эмульга- тор Т-2 и др. |
| Неоргани- ческие | Тальк, глина белая, бенто- нит, природ- ный модифици- рованный оксид кремния (оксил) и др. | Элементоорга- нические | Полиоргано- силоксановые жидкости (эсилон-4, эсилон-5), мыла и др. |
Природные вспомогательные вещества получают путем переработки растительного, животного и микробиологического сырья и минералов. Природные вспомогательные вещества имеют преимущество по сравнению с синтетическими благодаря высокой биологической безвредности, поэтому их поиск, по-видимому, будет продолжаться и в дальнейшем. В настоящее время примерно 1/3 используемых вспомогательных веществ приходится на природные. Растительные биополимеры используют в качестве эмульгаторов, стабилизаторов, пролонгаторов и в других целях при производстве лекарственных форм.
Природные вспомогательные вещества имеют существенный недостаток — они подвержены микробной контаминации, поэтому растворы полисахаридов и белков быстро портятся. Кроме того, в составе микрофлоры неорганических соединений могут обнаруживаться не только условно-патогенные, но и патогенные микроорганизмы. В данном случае использование приемлемых методов стерилизации и добавление антимикробных веществ (консервантов) может значительно снизить до предельно допустимых норм микробную контаминацию природных вспомогательных веществ. Синтетические и полусинтетические вспомогательные вещества широко применяются в технологии лекарственных форм. Это обусловлено их доступностью, т. е. возможностью синтеза веществ с заданными свойствами, более эффективных и менее токсичных. При получении полусинтетических вспомогательных веществ можно усовершенствовать свойства природных веществ. Например, производное метилцеллюлозы — оксипропилцеллюлоза (в отличие от растворимой в воде натриевой соли метилцеллюлозы) —
не растворяется в гидрофильных средах, поэтому ее используют для защиты лекарственных веществ от кислой среды желудочного
сока.
Производные ланолина (ацетилированные, оксиэтилированные и др. ) в отличие от ланолина по составу близки к кожному жиру человека, не вызывают аллергических реакций и благодаря меньшей вязкости по сравнению с ланолином удобнее при изготовлении мазей.
По размеру (величине) молекулы вспомогательные вещества подразделяют: на низкомолекулярные; олигомеры (масса молекулы менее 10 000); высокомолекулярные, или полимеры (масса молекулы более 10 000).
Наиболее часто применяют в качестве вспомогательных веществ высокомолекулярные вещества (ВМВ), образующие растворы различной вязкости в зависимости от концентрации. С этим свойством связано и основное их использование в различных лекарственных формах: жидких, вязкопластичных и твердых, т. е. в растворах, мазях и т. п. Их молекулы (макромолекулы) представляют собой длинные нити, переплетающиеся между собой или свернутые в клубки. От строения молекул часто зависит специфика изготовления растворов (в технологии лекарственных форм ВМВ в основном используют в виде растворов).
Применяют ВМВ в технологии практически всех лекарственных форм: как основы для мазей, суппозиториев, пилюль и др.; стабилизаторы; пролонгирующие компоненты; вещества, исправляющие неблагоприятные органолептические свойства лекарственного препарата; кроме того, как упаковочные и укупорочные материалы. Широкое применение ВМВ в технологии лекарственных форм связано также с их поверхностно-активными свойствами.
Введение в технологию новых ВМВ позволило создать новые лекарственные формы: многослойные таблетки длительного действия; спансулы (гранулы, пропитанные растворами ВМВ); микрокапсулы; имплантируемые лекарственные формы, лекарственные формы с регулируемым высвобождением, глазные лекарственные пленки; специфические детские лекарственные формы (жевательные резинки, конфеты, драже).
Наиболее частое применение полимеров в технологии лекарственных форм объясняется тем, что они позволяют решить большинство технологических проблем:
обеспечить биологическую доступность, необходимую скорость наступления фармакологического эффекта или доставку к органу-мишени; контролируемое высвобождение, поддержание терапевтической концентрации в течение требуемого периода; повысить точность дозирования; снизить токсичность и побочное действие; маскировать неприятный вкус и запах;
сохранить стабильность при хранении, предохранить лекарственные вещества от воздействия внешних факторов;
обеспечить оптимальную упаковку и укупорку;
повысить экономичность и эффективность производства.
Применяемые в фармации полимеры не должны содержать токсических мономеров, должны выдерживать стерилизацию, обладать оптимальным комплексом технологических (физико-химических и структурно-механических) свойств. К некоторым полимерам предъявляют требование растворимости в биологических средах.
Прогресс в области фармацевтической технологии тормозится недостатком высококачественных биоразрушаемых или биоусвояемых нетоксичных полимеров. Благодаря развитию синтетической химии, особенно химии полимеров, в последние десятилетия сложились условия для направленного поиска новых вспомогательных веществ, таких как метилцеллюлоза и ее производные, поли-винол, полиэтиленгликоли, поливинилпирролидон, полиакриламид, силиконы, различные эмульгаторы.
По функциональной роли вспомогательные вещества подразделяют: на формообразователи, стабилизаторы, солюбилизаторы, регуляторы высвобождения и всасывания, корригенты (табл. 5. 4).
| Функциональная роль вспомогательных веществ | ||
| Вспомогательные вещества | Функции и лекарственной форме | Примеры |
| Твердые | Формообразова- ние | Haполнители, пластификаторы: основы для порошков (сахар, крахмал, тальк), пилюли (растительные порошки, экстракты) и др. |
| Жидкие | Дисперсионные среды, растворители, экстрагенты | |
| Упруговязко-пластичные | Основы для мазей, пластификаторы, регуляторы | |
| Структурообра-зователи и стабилизаторы термодинамических свойств системы | Стабилизация | температуры плавления Вещества, предотвращающие седиментацию, коагуляцию, коалесценцию, агрегацию, конденсацию |
| Ингибиторы химических процессов | Вещества, предотвращающие гидролиз, окисление, разложение и другие химические процессы |
| Вспомогательные вещества | Функци в лекарственной форме | Примеры |
| Консерванты | Стабилизация | Вещества, предотвращающие микробную контаминацию |
| В основном поверхностно- активные ве- щества (ПАВ) | Солюбилизация | Вещества, способствующие мицеллярному растворению лекарственных веществ |
| Активаторы всасывания; пролонгаторы | Регулирование высвобождения и всасывания | Диметилсульфоксид, диметилформамид, ПАВ в низких концентрациях |
| Вещества, улуч- шающие вкус, цвет, запах | Корригирование | Сиропы, эфирные масла, красители и др. |
| Регуляторы осмотических свойств растворов | Электролиты (натрия хлорид, мафия сульфат, натрия нитрат); глюкоза | |
| Регуляторы рН | Буферные растворы (фосфат- ный, нитратный, гидрокарбо- натный), кислоты (хлористо- водородная, лимонная), щелочи (натрия гидроксид, натрия гидрокарбонат) |
Формообразователи.Это наиболее многочисленная группа вспомогательных веществ. Их используют в качестве дисперсионных сред (вода или неводные среды) в технологии жидких лекарственных форм, наполнителей для твердых лекарственных форм (порошков, пилюль, таблеток и др. ), основ для мазей, суппозиториев.
К формообразователям относятся вещества, способные обеспечить специфические для данной лекарственной формы структурно-механические свойства и физико-химические показатели: требуемое агрегатное состояние, оптимальную дисперсность и реологические показатели. Кроме того, они обеспечивают необходимую концентрацию лекарственных веществ, соответствующий объем или массу лекарственного препарата, определенную геометрическую форму.
Среди дисперсионных сред для изготовления жидких лекарственных форм наиболее часто используют воду очищенную и для инъекций. В качестве неводных растворителей или в составе комбинированных применяют этанол, глицерин, масла жирные, ва-
зелиновое масло, полиэтиленоксид (чаще — с молекулярной массой — 400), пропиленгликоль, этилолеат, силиконовые жидкости (эсилоны), бензилбензоат.
Среди дисперсионных сред определенный интерес с фармацевтической точки зрения представляют силиконы (Siliconum) — кремнийорганические олигомеры (кремнийорганические жидкости). По структуре они могут быть линейные, сетчатые и циклические.
Основу силиконов составляет силоксановый скелет — цепь чередующихся атомов кремния и кислорода. Свободные связи кремния заполнены органическими радикалами (метальным, этильным, фенильным и др. ). Наиболее широкое применение получили диэтилполиорганосилоксановые жидкости:

Полимер со степенью полимеризации 5 получил название эси-лон-4, а со степенью полимеризации 15 — эсилон-5. Они представляют собой бесцветные, прозрачные, вязкие, гигроскопичные жидкости без запаха и вкуса. В связи с отсутствием химически активных групп они характеризуются высокой инертностью: не окисляются, не подвергаются действию агрессивных сред, обладают гидрофобными свойствами, термостойки, не смешиваются с водой, этанолом, глицерином. Силиконы совместимы с липофильными компонентами мазей (вазелином, парафином, маслами растительными). В эсилонах хорошо растворяются неполярные вещества (ментол, камфора, фенол).
Благодаря биологической инертности силиконов, они перспективны для применения в качестве носителей в лекарственных препаратах при различных способах введения. Их также используют для силиконизирования стеклянной тары для повышения химической и термической стойкости, снижения гигроскопичности сухих экстрактов.
Силиконовые жидкости используют в защитных кремах, лосьонах и мазях. Хорошая переносимость кожей (не нарушают тканевое дыхание, теплообмен), тканями и слизистыми оболочками, длительная стабильность и совместимость со многими лекарственными веществами послужили основанием для их использования в качестве растворителей или носителей в лекарственных формах.
Экстрагенты в отличие от других дисперсионных сред должны обладать рядом специфических свойств: селективной (избирательной) растворяющей способностью; высокой диффузионной способностью (проникать в клетки растительного и животного сырья),
десорбирующими свойствами (растворять и извлекать действующие вещества из клеток). Для изготовления твердых лекарственных форм в качестве вспомогательных веществ (нередко их называют наполнителями) используют сахар молочный, или белый, крахмал, тальк, порошки лекарственных растений и их экстракты (сухие) и другие компоненты в зависимости от вида лекарственной формы.
При изготовлении мазей в качестве основ наиболее часто применяют вязкопластичные вещества и их сочетания:
липофильные (вазелин, жиры, силиконовые основы и др. );
гидрофильные (гели полиэтиленоксидов, крахмально-глицериновые гели, растворы производных целлюлозы, желатиновые гели
и др. );
дифильные (чаще всего эмульсионные основы).
Для изготовления суппозиториев используют вещества и их сочетания как нерастворимые в воде (масло какао, основа жировая, масла гидрогенизированные — основа — твердый жир типов А, В и др. ), так и растворимые (упругие гели желатина, полиэтиленоксидов и др. ). Для изготовления суппозиториев применяют основы, утвержденные ФС 42-3466-97, которые получены на основе твердого жира (Solides adeps). Они представляют собой смесь глицеридов высокомолекулярных жирных кислот и состоят или только из жира кондитерского твердого на основе пластифицированного саломаса, или с добавлением различных эмульгаторов, определяющих тип основы.
Коллаген (Collagenum) — основной белок соединительной ткани представляет значительный интерес как формообразователь для различных лекарственных форм. Он состоит из макромолекул трех-спиральной структуры. Коллаген получают путем щелочно-солевой обработки спилка кожи крупного рогатого скота, в которой его содержится до 95 %.
Коллаген применяют для покрытия ран в виде пленок с фура-цилином, кислотой борной, маслом облепиховым, метилурацилом, гемостатических, а также глазных пленок с антибиотиками. Удовлетворительные технологические и биологические свойства коллагена (отсутствие токсичности, хорошая резорбция, утилизация в организме, стимуляция репаративных процессов) обеспечивают возможность широкого использования его при изготовлении лекарственных форм.
Как формообразователи и стабилизаторы физико-химических процессов используют гели желатина.
Желатин (Gelatina) — высокомолекулярное вещество белковой структуры — получают при выпаривании обрезков кожи. Основной аминокислотой желатина является гликокол (25, 5 %), содержится также много аланина (8, 7%), аргинина (8, 2%), лейцина (7, 1 %), лизина (5, 9%) и глютаминовой кислоты. Благодаря высоким гелеобразующим свойствам его используют для из-
готовления мазей, суппозиториев, желатиновых капсул и других лекарственных форм.
Из неорганических полимеров наиболее часто в качестве формообразователен используют бентонит, аэросил (оксил), тальк.
Бентонит (Bentonitum) — природный неорганический полимер. Встречается в виде минералов кристаллической структуры с частицами размером менее 0, 01 мм. Бентонитовые глины имеют сложный состав и представляет собой в основном алюмогидроси-ликаты с общей формулой: Al2O3 SiO2 mН20. В их состав входит 90% оксидов алюминия, кремния, магния, железа и воды, присутствуют катионы К+, Na+, Са2+, Mg2+, поэтому глинистые минералы могут вступать в ионообменные реакции. Это позволяет получать системы с заданными свойствами, так называемые модифицированные бентониты. Последние активно взаимодействуют с водой. Вследствие образования гидратной оболочки частицы глинистых минералов способны прочно удерживать воду и набухать в ней, значительно увеличиваясь в объеме. Наибольшей набу-хаемостью обладают натриевые соли бентонитов (объем их увеличивается в 17 раз), кальциевые соли (в 2, 5 раза), еще больше увеличивается объем полусинтетических бентонитов — триэтанол-аминобентонитов (в 20 — 22 раза).
Бентониты биологически безвредны. Индифферентность к лекарственным веществам, способность к набуханию и гелеобразо-ванию позволяют использовать их при производстве мазей, таблеток, порошков для внутреннего и наружного применения, пилюль, гранул. В концентрации 3 — 5 % их используют для стабилизации суспензий. Бентониты обеспечивают мягкость, дисперсность, высокие адсорбционные свойства, легкую отдачу лекарственных веществ и стабильность лекарственных препаратов.
Аэросил (Aerosilum, Oxylum) — коллоидный кремния диоксид (SiO2) представляет собой очень легкий, белый, высокодисперсный, микронизированный, с большой удельной поверхностью порошок, обладающий выраженными адсорбционными свойствами, относится к неорганическим полимерам. В водном растворе концентрацией 1—4% образует студнеобразные системы с глицерином, маслом вазелиновым.
Его применяют для стабилизации суспензий с различной дисперсионной средой, что способствует лучшей фиксации суспензий на коже и усиливает терапевтический эффект. Загущающую способность аэросила используют при получении гелей для мазевых основ. В порошках его также применяют для предотвращения увлажнения гигроскопичных смесей и как диспергатор.
Адсорбционные свойства аэросила используют также в целях стабилизации сухих экстрактов (уменьшения их гигроскопичности). Добавление аэросила к пилюлям значительно повышает их устойчивость к высыханию в процессе хранения. Он усиливает
вязкость суппозиторной массы, придает ей однородность, обеспечивает равномерное распределение лекарственных веществ, позволяет вводить жидкие и гигроскопичные вещества.
Эфиры целлюлозы занимают особое место среди ВМВ, используемых в технологии лекарственных форм. Физиологическая безвредность, ценные физико-химические и технологические свойства этих вспомогательных материалов позволяют применять их в качестве стабилизирующих, пролонгирующих, основообразующих средств, а также для повышения качества многих лекарственных форм.
Общая формула целлюлозы: [С6Н7O(OH)3_xOR)x]n.
В технологии используют простые и сложные эфиры целлюлозы.
Метилцеллюлоза растворимая (Methylcellulosum solubile)
[С6Н7O2(ОН)3-x(ОСН3)х]n,
где х — число замещенных ОН-групп в одном звене; п — степень полимеризации.
Относительная молекулярная масса метилцеллюлозы составляет 150 000 — 300 000. Она представляет собой простой эфир целлюлозы и метанола. Может иметь вид слегка желтоватого порошка, гранулированного или волокнистого продукта без запаха и вкуса. Растворяется в холодной воде, глицерине, не растворяется в горячей воде.
При изготовлении водных растворов метилцеллюлозу заливают кодой (половиной требуемого объема раствора), нагретой до температуры 80 —90 С. После охлаждения раствора до комнатной температуры добавляют остальную холодную воду. Охлажденные растворы прозрачны. При нагревании до температуры выше 50 °С водные растворы метилцеллюлозы обратимо коагулируют. При охлаждении гель снова переходит в раствор. Растворы обладают выраженными поверхностно-активными свойствами (высокой сорбционной, эмульгирующей и смачивающей способностями). При высыхании они образуют прозрачную прочную пленку.
В технологии в качестве загустителей и стабилизаторов применяют 0, 5— 1 % водные растворы. В таких же концентрациях метил-целлюлозу применяют для гидрофилизации липофильных основ мазей и линиментов, в качестве эмульгатора и стабилизатора при изготовлении суспензий и эмульсий, а также как пролонгирующий компонент глазных капель. Глицерогели 3 — 8 % применяют как невысыхающие основы для мазей.
Na-карбоксиметилцеллюлоза (Methytcellulosum-natrium) — натриевая соль простого эфира целлюлозы и гликолевой кислоты (Na-КМЦ):
[C6H7O2(OH)3(OCH2COONa)x]n,
где х — число замещенных ОН-групп в одном звене; п — степень полимеризации.
Na-KMIi (молекулярная масса 75 000 — 85 000) — белый или слегка желтоватый порошок, либо волокнистый продукт без запаха, растворимый в холодной и горячей воде. В разных концентрациях (0, 5%, 1 %, 2%) применяют как пролонгатор действия лекарственных веществ в глазных каплях и инъекционных растворах, в качестве стабилизатора, формообразователя в эмульсиях и мазях (4 —6 %). Гели Na-КМЦ в отличие от гелей метилцеллюло-зы совместимы со многими консервантами.
Помимо МЦ и Na-КМЦ в технологии готовых лекарственных средств используют оксипропилметилцеллюлозу и ацетилцеллю-лозу.
Поливинол (Polyvinolum) — наиболее распространенный синтетический водорастворимый полимер винилацетата. Поливинол (поливиниловый спирт — ПВС) — синтетический полимер алифатического ряда, содержащий гидроксильные группы:
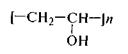
где п — число структурных единиц в макромолекуле полимера.
Поливинол представляет собой порошок белого или слегка желтоватого цвета, растворимый в воде при нагревании. Обладает высокой реакционной способностью благодаря наличию гидроксиль-ных групп.
В технологии лекарственных форм 1, 4 — 2, 5% растворы ПВС применяют в качестве эмульгатора, загустителя и стабилизатора суспензий; 10 % растворы — в качестве основ для мазей и глазных пленок.
Поливинилпирролидон (Polyvinylpyrrolidonum) (ПВП) представляет собой полимер N-винилпирролидона. Его получают при полимеризации мономера — винилпирролидона:

где п — степень полимеризации.
Поливинилпирролизон — бесцветный, прозрачный, гигроскопичный полимер (молекулярная масса 10000—100 000). Наиболее широко применяют ПВП с молекулярной массой 12600 — 35 000. Он растворим в воде, спиртах, глицерине, легко образует комплексы с лекарственными веществами (витаминами, антибиотика-
ми). ПВП используют в медицине и фармацевтической технологии как стабилизатор эмульсий и суспензий, пролонгирующий компонент, наполнитель для таблеток и драже. Он также входит в состав плазмозаменителей, аэрозолей, глазных лекарственных пленок. Гели на основе ПВП используют для изготовления мазей, в том числе предназначенных для нанесения на слизистые оболочки.
Полиакриламид (Polyacrilamidum). В последние годы получили очень широкое распространение полиакриламид (ПАА) и его производные: 
Полиакриламид — полимер белого цвета, без запаха, растворим в воде, глицерине. Получен и биорастворимый полимер, его широко используют для лекарственных биорастворимых глазных пленок, которые обеспечивают максимальное время контакта с поверхностью конъюнктивы. Растворы 1 % используют для пролонгирования действия глазных капель. Успешно применяют и другие виды лекарственных пленок-тринитролонг. Водные растворы ПАА совместимы со многими электролитами, ПАВ и консервантами. Он перспективен для создания новых лекарственных форм.
Полиэтиленоксиды (Polyaethylenoxyda) (ПЭО) или полиэтилен-гликоли (ПЭГ) представляют собой полимеры этиленоксида
Н(-ОСН2-СН2-)nОН
которые получают путем полимеризации этиленоксида в присутствии воды и калия гидроксида.
Консистенция ПЭО зависит от степени полимеризации. В нашей стране выпускают ПЭО с различной степенью полимеризации (молекулярная масса 400 — 4 000). ПЭО-400 представляет собой вязкую прозрачную бесцветную жидкость, ПЭО-1500 — воски (температура плавления 35 — 41 °С), ПЭО-4000 — твердое вещество белого цвета с температурой плавления 53 — 61 °С.
Характерная особенность ПЭО заключается в хорошей растворимости в воде, этаноле. Они не смешиваются с углеводородами и жирами, образуют с ними эмульсию; малочувствительны к изменению рН, стабильны при хранении.
ПЭО обладают малой токсичностью, что обусловливает широкое применение в технологии изготовления мазей, эмульсий, суспензий, суппозиториев и других лекарственных форм. Основы для мазей чаще всего представляют собой композицию жидких и твердых ПЭО вязкопластичной консистенции. Однако они оказывают дегидратирующее действие на слизистые оболочки.
Способствовать формообразованию могут также наполнители, пластификаторы, регуляторы температуры плавления и другие вспомогательные вещества, например, при изготовлении таблеток, пилюльной массы (растительные порошки, глины и т. п. ), наполнитель для изготовления тритураций (молочный сахар).
Как регуляторы температуры плавления в мазях, суппозиториях применяют воск или парафин. В качестве примера можно привести суппозитории с хлоралгидратом, когда вещество образует с жировой основой состав с понижением температуры плавления, вплоть до плавления при комнатной температуре, что нежелательно. В этом случае часть масла какао заменяют воском из расчета 0, 7 г на 1, 0 г хлоралгидрата.
Стабилизаторы.Стабильность — это свойство лекарственных средств сохранять исходное качество в течение определенного времени с момента изготовления (выпуска).
Стабилизаторы имеют большое значение для сохранения стабильности гетерогенных (неоднородных) систем (суспензий и эмульсий). Они позволяют изготовить и использовать лекарственные препараты труднорастворимых или практически нерастворимых лекарственных средств в воде и других дисперсионных средах.
К стабилизаторам гетерогенных дисперсных систем можно отнести производные метилцеллюлозы, пектины, альгинаты, бентонитовые глины, аэросил, твины и спены, и ряд других веществ. Нередко в целях снижения количества этих веществ и повышения их активности используют различные сочетания стабилизаторов.
К группе термодинамических (структурно-механических) стабилизаторов дисперсных систем относятся следующиe вещества: диспергаторы, загустители, структурообразователи; ПАВ (эмульгаторы, стабилизаторы суспензий), т. е. вещества, способные повышать агрегативную и седиментационную устойчивость микрогетерогенных систем.
Из большого многообразия веществ этой группы наибольшего внимания заслуживают ПАВ благодаря полифункциональности. По международной номенклатуре их называют тензиидами (от лат. tensio — натяжение). ПАВ — это, как правило, ВМВ или олигомеры, иногда низкомолекулярные вещества, которые обладают рядом специфических свойств:
имеют дифильный характер молекулы;
гидрофильные и липофильные группы в молекуле сбалансированы и характеризуются определенным значением гидрофильно-липофильного баланса;
обладают значительным дипольным моментом μ = eL, где е — величина заряда; L — расстояние между положительно и отрицательно заряженными группами и хорошо гидратирующимися по-
лярными группами, что обусловливает сродство ПАВ к воде. Графически их иногда изображают в виде головастика, где голова — гидрофильные группы молекулы, а хвост — липофильный углеводородный радикал (О—);
способны снижать межфазное натяжение, сосредоточиваясь на границе раздела фаз, образуя прочные пленки в виде моно- или полимолекулярного слоя.
Для ориентации в большом количестве ПАВ (в настоящее время известно более 1000) в 1949 г. была предложена классификация на основе соотношения гидрофильных и гидрофобных групп в молекуле ПАВ — гидрофильно-липофильного баланса. Последний прямо пропорционален массе гидрофильных групп и уменьшается с увеличением липофила.
Все ПАВ имеют величину гидрофильно-липофильного баланса на шкале от 0 до 40. Чем он меньше, тем больше сродство ПАВ к неполярным веществам. Так, например, при его значении 3 — 6 ПАВ стабилизируют эмульсии типа «вода/масло» (гидрофилыю-липофильный баланс эмульгатора Т-2 равен 5, 5). С повышением баланса улучшаются гидрофильные свойства ПАВ, что сопровождается возрастанием их растворимости в воде. При значениях 7—9 они становятся смачивателями; при значениях 8—18 стабилизируют эмульсии типа «масло/вода» (гидрофильно-липо-фильпый баланс ГЛБ МЦ равен 10, 5), при значениях 15—18 и более ПАВ становятся солюбилизаторами (например, твин-80 (ГЛБ = 15) обладает высокой солюбилизирующей активностью в концентрации 0, 5%).
В основе классификации поверхностно-активных веществ лежит способность к диссоциации (ионизации). Их подразделяют на неионогенные и ионогенные.
Ионогенные классифицируют: на анионоактивные (натриевые, калиевые, кальциевые мыла), катионоактивные (соли четвертичных аммониевых оснований), амфотерные (амфолиты) — ведут себя как анионоактивные или катионоактивные в зависимости от рН.
Согласно научной литературе рекомендуется применять катионоактивные ПАВ в кислой среде, анионоактивные — в щелочной.
Механизм стабилизирующего действия ПАВ обусловлен их способностями:
адсорбироваться на поверхности твердых частиц или капелек жидкости, ориентируясь определенным образом;
снижать межфазное натяжение на границе раздела фаз и соответственно поверхностной энергии (энергии Гиббса), так как ∆G = Sσ; ∆G→min, если σ→min;
образовывать защитную пленку (моно- или полимолекулярный слои); сольватный слой; двойной электрический слой (в случае ионогенных ПАВ);
повышать вязкость (ВМВ — производные целлюлозы, например, в концентрации 5 — 7 % используют как основы для мазей).
Применение ПАВ и ВМВ — один из способов повышения химической устойчивости лекарственных веществ. При этом стабилизирующее действие происходит путем мицеллообразования и связывания молекул лекарственных веществ с мицеллами. Например, анионоактивные ПАВ уменьшают скорость гидролиза дикаина в 10 раз, новокаина — в 4 раза.
Неиногенные ПАВ. Наибольшее предпочтение отдают неионо-генным ПАВ, которые обладают следующими свойствами:
малочувствительны к изменению значения рН, способны проявлять свои свойства в любой среде; как правило, биологически безвредны; образуют стабильные эмульсии при содержании их в концентрации порядка десятых долей процента и не более 2 %.
Крахмал (Amylum) составляют полисахариды (97, 3 — 98, 9%), белковые вещества (0, 28—1, 5%), клетчатка (0, 2 — 0, 69%), минеральные вещества (0, 3 — 0, 62 %). Крахмал состоит из двух фракций — амилозы и амилопектина. Молекула амилозы представляет собой длинную молекулу, состоящую из гликозидных остатков (до 700). Амилопектин имеет более сложное строение и состоит из разветвленных молекул, содержащих до 2000 остатков D-глюкопи-ранозы. Чем короче цепи, тем фракция лучше растворяется в воде. Так, амилоза растворяется в теплой воде, а амилопектин только набухает. Клейстеризация выражается в сильном набухании крахмальных зерен, их разрыве и образовании вязкого гидрогеля.
Крахмал используют в твердых лекарственных формах, в том числе пилюлях (в смеси с глюкозой и сахаром), мазях: слизь крахмала (Mucilago Amyli) (ГФ VII) 2 % — как обволакивающее средство для снижения раздражающего действия на слизистую оболочку. В качестве стабилизатора суспензий и эмульсий применяют 10 % раствор.
На 100, 0 г 10% эмульсии применяют раствор, изготовленный по прописи, г:
крахмал.............................................................. 5, 0
вода холодная..................................................... 10, 0
вода горячая........................................................ 35, 0
Микробные полисахариды (polysaccharida microbica) составляют важный класс природных полимеров, обладающих разнообразными свойствами (пролонгирующими, стабилизирующими и т. п. ), благодаря которым они могут применяться как основы для мазей, линиментов. В Санкт-Петербурге разработана технология получения ряда новых микробных полисахаридов, которые характеризуются апирогенностью, малой токсичностью, что определяет возможность использования их в качестве вспомогательных веществ. Из группы этих веществ следует отметить аубазидан — вне-
клеточный полисахарид, получаемый при микробиологическом синтезе с помощью дрожжевого гриба Aureobasidium pululans. Благодаря своему строению, разветвленной структуре, конфигурации и конформации моносахаридов в молекуле полимера (молекулярная масса 6 — 9 млн) он обладает хорошей растворимостью в воде, дает вязкие растворы, пластичные гели, может взаимодействовать с другими веществами, что определяет его практическое применение. Аубазидан (0, 6% и выше) образует гели, которые могут использоваться как основа для мазей, 1 % гель — для пленок и губок. В концентрации 0, 1—0, 3% его используют как пролонгатор глазных капель. В данном случае положительным моментом является устойчивость растворов при термической стерилизации до 120°С. Он также является эффективным стабилизатором и эмульгатором.
Эмульгатор Т-2 — смесь полных и неполных эфиров стеариновой кислоты и ди- или триглицерина. Представляет собой воскообразные куски желтого цвета, без запаха, вкуса, растворим в горячей воде.
Используют для стабилизации эмульсии бензилбензоата, эмульсионных линиментов и мазей (консистентная эмульсия «вода/вазелин»), входит в состав суппозиторных основ (суппорин М, твердый жир тип В), используется для предотвращения несовместимости в случае несмешиваемости жидкостей или вязких масс.
Спены (Spans) — сложные эфиры сорбитана с высшими жирными кислотами:

Наиболее часто применяют спен-20 — эфир лауриновой кислоты С11Н33СООН, спен-40 — эфир пальмитиновой кислоты C15H31COOH, спен-60 — эфир стеариновой кислоты С17Н35СООН, спен-80 — эфир олеиновой кислоты C17H33COOH. Спены — липофильные соединения. Они растворимы в маслах, а также этаноле, образуют эмульсии типа «вода/масло». В связи с неионогенным характером совместимы со многими лекарственными веществами.
Твины (Twins) представляют собой моноэфиры полиоксиэтили-рованного сорбитана (спена) и высших жирных кислот. Твины получают путем обработки спенов этиленоксидом в присутствии натрия гидроксида (катализатор). Этерификация происходит по месту свободных гидроксилов. Твины хорошо растворяются в воде и орга-
нических растворителях. К медицинскому применению разрешен твин-80, представляющий собой моноэфир олеиновой кислоты.
Твин-80 — неионогенное ПАВ. Он служит хорошим эмульгатором с высоким значением ГЛБ (15—16), поэтому применяется как солюбилизатор, стабилизатор эмульсий и суспензий, в том числе и для инъекционного введения.
Жиросахара (Adiposacchara) — неполные сложные эфиры сахарозы и высших жирных кислот (стеариновой, пальмитиновой, лауриновой и др. ). Представляют собой ПАВ твердой, вязкой и жидкой консистенции, не имеют запаха и вкуса, в организме распадаются на жирные кислоты, фруктозу и сахарозу, индифферентны для кожи. Жиросахара применяют в качестве солюбилиза-торов, эмульгаторов (при изготовлении эмульсий для парентерального введения), стабилизаторов.
Катионоактивные ПАВ. Среди различных групп катионоактив-ных ПАВ — наиболее сильные бактерицидные средства (этония хлорид, тиония хлорид и т. п. ). Соли четвертичных аммониевых оснований достаточно токсичны, как ПАВ применяются редко, чаще — как консерванты.
Примером может служить бензалкония хлорид, ДМДБАХ, — диметилдодецилбензалкония хлорид (0, 01 --0, 02 %).
Включение в лекарственные формы представителей неионо-генных ПАВ одновременно с катиопоактивными нерационально, так как это приводит к снижению бактериостатических свойств и требует повышения концентрации солей четвертичных аммониевых оснований, что будет приводить к увеличению токсических свойств лекарственной формы.
Анионоактивные ПАВ. К ним относят камеди, мыла, алкилсуль-фаты (например, натрия лаурилсульфат), пектиновые вещества.
Камеди (аравийская, абрикосовая, сливовая и др. ) — это калиевые, кальциевые, магниевые соли полиарабиновой и других полиуроновых кислот. Перспективны натриевые соли альгиновой кислоты (alginata).
 |
Кислота альгиновая представляет собой ВМВ из морских водорослей (ламинарий). Она образует вязкие водные растворы и пасты, обладает гомогенизирующими, разрыхляющими, стабилизирующими свойствами. Поэтому альгинаты широко используют в составе различных фармацевтических препаратов в качестве разрыхляющих, эмульгирующих, пролонгирующих, пленкообразующих вспомогательных веществ, а также для приготовления мазей и паст.
Кислота альгиновая и ее натриевая соль практически безвредны. Это наиболее перспективные новые вспомогательные вещества, особенно для производства готовых лекарственных препаратов.
Мыла — это соли высших жирных кислот (например, стеариновой). Натриевые, калиевые, аммониевые соли растворимы в воде
(стабилизируют эмульсии типа «масло/вода»); натриевое мыло — твердое, калиевое — жидкое (зеленое). Медицинское мыло используют для стабилизации эмульсии бензилбензоата, аммонийное — для стабилизации аммиачного линимента, в этом случае эмульгатор получается в процессе изготовления эмульсии при взаимодействии аммиака, олеата аммония и других жирных кислот подсолнечного масла. Кальциевые, железистые, алюминиевые соли не растворимы в воде (стабилизируют эмульсии типа «вода/масло», эмульсионные основы для мазей). Алкилсульфаты R — СН2 —О —SО3Na, где R = (С9—С17), применяют для стабилизации эмульсий типа «масло/вода», а также используют в качестве компонентов основ для мазей.
Пектин (Pectinum) и пектиновые вещества входят в состав клеточных стенок многих растений. Это ВМВ, представляющие собой по структуре полигалактуроновую кислоту, частично этери-фицированную метанолом. Характерным свойством растворов пектина является высокая желатинирующая способность. Пектин представляет интерес для создания детских лекарственных форм. Пектиновые вещества содержатся в растениях (овощах, плодах), применяются в пищевой промышленности, но широкого применения в фармации пока не нашли. Пока проводятся исследования с хорошими результатами.
Амфотерные ПАВ. Кэтой группе могут быть отнесены бентониты, глины, белки (желатоза, лецитин). В зависимости от значения рН эти вещества проявляют свойства анионоактивных или катионоактивных ПАВ, например, белки:
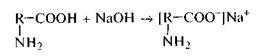
В щелочной среде белок проявляет себя как анионоактивное ПАВ: 
в кислой — как катионоактивное ПАВ.
Желатоза (Gelatosa) представляет собой продукт неполного гидролиза желатина, не обладает способностью желатинироваться, но имеет высокие эмульгирующие свойства. Отрицательным свойством является нестандартность вещества, поэтому в ряде случаев растворы желатозы могут обладать высокой вязкостью и упругостью.
В ГФ в статье «Эмульсии» в качестве эмульгаторов рекомендованы мыла (анионоактивные ПАВ), твин-80, эмульгатор Т-2 (не-ионогенные ПАВ), производные целлюлозы. В статье «Суппозито-
рии» приведены эмульгаторы Т-1, Т-2, твин-80, спирты шерстного воска.
В качестве структурообразователей также широко применяются производные целлюлозы, полисахариды микробного происхождения, полученные методами биотехнологии (аубазидан, родэкс-ман и др. ), оксил SiО2 (5 % в линименте Вишневского).
Ингибиторы химических процессов. Имеют большое значение для лекарственных форм, подвергающихся различным видам стерилизации, особенно термической. Учитывая, что скорость химических реакций возрастает в 2 —4 раза при повышении температуры на каждые 10 °С (правило Вант-Гоффа), проблема инги-бирования химических процессов особенно актуальна для инъекционных и инфузионных, офтальмологических растворов, растворов для новорожденных детей, препаратов, предназначенных для нанесения на раневую и ожоговую поверхности, а также для введения в полости организма, не содержащие микроорганизмов.
Регуляторы рН. Применение стабилизаторов основано на подавлении процессов гидролиза или окислительно-восстановительного разложения лекарственных веществ. К этой группе относят вещества — регуляторы рН и антиоксиданты. В качестве регуляторов значений рН применяют кислоты, соли, щелочи, а также буферные системы. Так, для стабилизации 0, 5 % раствора новокаина для новорожденных детей, растворов новокаина различной концентрации для инфильтрационной анестезии, растворов атропина сульфата, дикаина, дибазола, спазмолитина гидрохлорида; скополамина гидробромида добавляют 0, 1М раствор хлористоводородной кислоты. Эту кислоту добавляют для подавления гидролиза солей, образованных слабым основанием и сильной кислотой, а также для подавления гидролиза сложноэфирной связи. В растворы глюкозы добавляют стабилизатор Вейбеля, содержащий натрия хлорид и кислоту хлористоводородную, что замедляет процесс окисления и карамелизации глюкозы.
Для предотвращения гидролиза солей, образованных сильным основанием и слабой кислотой (натрия нитрит, кофеин —натрия бензоат, натрия тиосульфат и др. ), добавляют натрия гидрокарбонат или натрия гидрооксид (в соответствии с нормативными документами). С добавлением 0, 01 % трилона Б (комплексона, связывающего ионы тяжелых и щелочноземельных металлов) изготавливают 3, 4, 5, 7 и 8, 4 % растворы натрия гидрокарбоната во избежание выпадения осадков магния и кальция карбонатов.
Буферные системы. Иногда наиболее эффективно использовать буферные системы, которые содержат слабую кислоту и сопряженное с ней основание. Буферные растворители широко применяют при изготовлении глазных капель (боратный), растворов для инъекций (фосфатный, цитратный) и др.
Буферные растворы бывают кислотно-основными или окислительно-восстановительными. Кислотно-основные буферные растворы поддерживают постоянство рН при изменении состава среды, окислительно-восстановительные — постоянство окислительно-восстановительного потенциала.
Антиоксиданты. Втехнологии лекарственных форм часто возникает необходимость использовать антиоксиданты — стабилизаторы, тормозящие окислительно-восстановительные процессы. Их применяют не только для ингибирования процессов окисления в инъекционных растворах и глазных каплях, но и в водных извлечениях, мазях, суппозиториях. Особенно чувствительны к окислению ненасыщенные жиры и масла, соединения с альдегидными и фенольными группами, а также полимерные упаковочные материалы.
Известно множество антиоксидантов как натуральных, так и синтетических. Механизмы процессов окисления и торможения с помощью антиоксидантов в настоящее время хорошо изучены. Это, как правило, в химическом отношении — очень реакционно-способные вещества и вступают во взаимодействие с активными ингредиентами, влияя на стойкость и эффективность лекарственных препаратов. В качестве антиоксидантов предложены производные фенола, ароматические амины, производные серы (натрия сульфит и метабисульфит, ронгалит, тиомочевина), а также трилон Б, кислота аскорбиновая, токоферолы и другие соединения.
По механизму действия антиоксиданты подразделяют на три группы:
1) антиоксиданты, которые ингибируют процесс окисления, реагируя со свободными радикалами первичных продуктов окисления, прекращая тем самым процесс развития цепной реакции (бутилоксианизол, бутилокситолуол, нордигидрогваяретовая кислота, токоферолы);
2) восстанавливающие антиоксиданты (сульфит натрия; метабисульфит натрия; органические соединения серы — тиомочевина, ронгалит, унитиол, цистеин; анальгин; кислота аскорбиновая и др. ), имеющие более низкий окислительно-восстановительный потенциал, чем находящиеся в препарате лекарственные вещества. Окислению лекарственных веществ предшествует окисление восстановителя;
3) синергисты антиоксидантов, собственное антиокислительное действие которых незначительно, но они способствуют усилению действия других антиоксидантов, например, образуя комплексы с ионами металлов, катализирующими окисление, или регенерируя антиоксиданты (кислоты лимонная и винная, ЭДТА (трилон Б) и др. ).
В технологии лекарственных форм в последние годы довольно часто используют комплекс стабилизаторов, обладающих синер-
гическим эффектом. Раствор солюзида растворимого 5 % стабилизируют 0, 01 % трилона Б, растворы тиамина бромида (3 и 6 %), а также тиамина хлорида (2, 5 % и 5 %) — 0, 2 % унитиола. Инъекционный раствор апоморфина 1 % стабилизируют комплексным антиоксидантом, содержащим 0, 05 % анальгина и 0, 02 % цистеина.
Обычно антиоксиданты применяют в малых концентрациях (например, кислоту аскорбиновую — в концентрации 0, 02 — 0, 1 %, натрия сульфит — 0, 2 — 0, 5%, натрия тиосульфат — 0, 05 — 0, 1 %, тиомочевину — 0, 005 %, трилон Б — 0, 01 -0, 075 %).
Комплексный антиоксидант (натрия метабисульфита 0, 1 % и трилона Б 0, 03 %) используют в офтальмологических каплях, содержащих: рибофлавина 0, 02 %; кислоты аскорбиновой 0, 2 %; глюкозы 2%, в том числе пролонгированных 1 % раствором МЦ.
В качестве антиоксидантов в лекарственной форме «Суппозитории» согласно ГФ XI разрешено использовать бутилокситолуол, бутилоксианизол и кислоту лимонную.
Консерванты. Подавляя жизнедеятельность микроорганизмов в лекарственных препаратах, консерванты обладают бактериоста-тическим или бактерицидным действием и обеспечивают химическую стерилизацию препарата. Подавляя жизнедеятельность микроорганизмов, консерванты предотвращают возможное инфицирование больного контаминированным препаратом и разложение действующих веществ продуктами жизнедеятельности микроорганизмов.
Консервирование не исключает соблюдения санитарных правил производственного процесса, которые должны способствовать максимальному снижению микробной контаминации лекарственных препаратов. Консерванты ингибируют рост тех микроорганизмов, которые попадают в лекарственные препараты в процессе их многократного использования. Они позволяют сохранить стерильность лекарственных препаратов или предельно допустимое число непатогенных микроорганизмов в нестерильных лекарственных препаратах. К консервантам предъявляют тс же требования, что и к другим вспомогательным веществам, но обращают внимание на наличие широкого спектра их антимикробного действия.
К группе противомикробных стабилизаторов (консервантов) относятся спирты, фенолы, органические кислоты, сложные эфиры парагидроксибензойной кислоты, соли четвертичных аммониевых соединений, эфирные масла. Консервирующим действием могут обладать непосредственно лекарственные вещества, например, тимол, кислота салициловая, бензойная, натрия бензоат, гексаметилентетрамин, скипидар и др. В качестве консервантов-антисептиков разрешены следующие вещества: хлорбутанолгидрат (0, 05 — 0, 5 %), например, для стабилизации 0, 1 % раствора адреналина, 0, 06 % раствора коргликона, 0, 05 % раствора эрготала; фенол (0. 25 — 0, 5%) для консервирования вакцин, препаратов
инсулина; нипагин (0, 1 %) — для стабилизации 0, 03% раствора конваллотоксина, 0, 05 % раствора строфантина К и др. Как консерванты-антисептики наиболее часто используют спирты этиловый, бензиловый, хлорбутанолгидрат.
Спирт этиловый — этанол (Spiritus aethylicus), являясь экстра-гентом при получении настоек, экстрактов и концентратов из лекарственного растительного сырья, в то же время выполняет роль консерванта. Этанол различной концентрации используют при получении гомеопатических эссенций, матричных настоек. Для консервирования некоторых эмульсий применяют этанол в количестве 10—12% от водной фазы, в галеновых и новогаленовых препаратах — до 20 %. Однако в такой концентрации он оказывает слабый эффект, наилучшими антисептическими свойствами обладает 70% этанол.
Большей активностью по сравнению с этанолом обладает спирт бензиловый (Spiritus benzylicus):

Спирт бензиловый представляет собой жидкость с приятным ароматическим запахом и жгучим вкусом, растворяется в воде в соотношении 1: 25, в 50% этаноле в соотношении 1: 1. Спирт бензиловый в концентрации 0, 9% применяют для консервирования глазных капель (содержащих кортизона ацетат), гидрофобных, гидрофильных и эмульсионных мазевых основ; препаратов радиоактивных изотопов и противоопухолевых веществ.
Хлорбутанолгидрат (Chlorbutanolum hydratum) является эффективным консервантом:

Хлорбутанолгидрат представляет собой бесцветные кристаллы с запахом камфоры, очень мало растворим в воде (1: 250), легко растворим в 90% этаноле, маслах жирных и вазелиновом, глицерине. В концентрации 0, 5% применяют для консервирования экстракционных препаратов, соков свежих растений, органопрепаратов. За рубежом его используют для консервирования глазных капель, эмульсий, капель для носа. Он совместим со многими лекарственными веществами.
Фенолы. Другую группу консервантов — органических соединений — представляют фенолы (фенол, хлоркрезол). Наиболее старым из них является фенол (Phenolum):
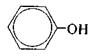
Растворы фенола 0, 25 — 0, 5% эффективны для консервирования инсулина, вакцин и сывороток. Однако при местном применении фенол обладает раздражающим действием. Он нередко вызывает аллергические реакции. Поэтому его не применяют для консервирования мазей, глазных капель, суппозиториев. Среди производных фенола наиболее часто используют хлоркрезол (Clorcre-solum):

Хлоркрезол представляет собой бесцветные кристаллы с характерным запахом, растворим в воде (лучше в горячей) в соотношении 1: 250, этаноле, маслах жирных. Хлоркрезол в 10—13 раз активнее фенола в отношении бактерий и грибов, в то же время он менее токсичен. Растворы хлоркрезола применяют для консервирования глазных капель (0, 05 %), инъекционных растворов (0, 1 %), мазей (0, 1-0, 2%).
В качестве консервантов широко применяют органические кислоты, например, бензойную и сорбиновую.
Кислота бензойная (acidum benzoicum) представляет собой кристаллическое вещество белого цвета со слабым характерным запахом, 1 г кислоты растворим в 350 мл воды или 3 мл этанола, или 8 мл хлороформа. Обычно эту кислоту применяют в виде натриевой соли, очень легко растворимой в воде (1 г в I мл воды). Кислота бензойная и ее соли оказывают сильное действие на дрожжевые грибы, особенно в кислой среде. Их используют для консервирования сахарного и различных лекарственных сиропов, эмульсии масла вазелинового, суспензий с антибиотиками и других препаратов, предназначенных для внутреннего применения.
Сложные эфиры парагидроксибензойной кислоты — парабены (нипагин, нипазол) нашли широкое применение в пищевой, парфюмерной и фармацевтической промышленности разных стран. Они включены в РФ, а также многие зарубежные фармакопеи. Наиболее часто используют метиловый и пропиловый эфиры.
Нипагин (Nipaginum) представляет собой метиловый эфир парагидроксибензойной кислоты. Пропиловый эфир парагидроксибензойной кислоты известен под названием нипазол (Nipasolum).
Эфиры парагидроксибензойной кислоты — это белые кристал-лические, без запаха и вкуса порошки, плохо растворимые в воде, растворимые в маслах и очень хорошо — в органических растворителях. Лучшей растворимостью обладает нипагин, поэтому его чаще применяют в водных растворах, нипазол одинаково растворим в воде и маслах. По антисептическим свойствам парабены в значительной степени превосходят фенол, например пропиловый эфир — в 17 раз. Более сильное консервирующее действие достигается при сочетании 0, 025 г пропилового и 0, 075 г метилового эфиров (1: 3). В таком соотношении смесь может быть использована для консервирования воды очищенной, мазей и эмульсий, особенно, если ее взять 0, 2 % массы мази или эмульсии. В состав гидрокортизоновой мази 1 % входит смесь эфиров в соотношении 0, 08: 0, 02.
Парабены рекомендованы для консервирования глазных капель. Малая токсичность позволяет использовать их для изготовления лекарственных препаратов внутреннего применения, галеновых препаратов (сиропа сахарного), настоев и отваров, концентрированных растворов, суспензий рентгеноконтрастных, гормональных и противотуберкулезных средств, антибиотиков, пероральных эмульсий, их также вводят в состав желатиновых капсул. Широко используют парабены для консервирования мазей и их основ.
Наиболее эффективным и биологически безвредным консервантом является кислота сорбиновая (Acidum sorbicum)
сн3—сн=сн-сн=сн-соон
которая представляет собой белый мелкокристаллический порошок со слабым раздражающим запахом и слабокислым вкусом. В концентрации до 0, 15% она растворима в воде, до 0, 2% — в маслах жирных и минеральных, легко растворима в спирте, эфире, ацетоне, мало — в глицерине.
Под воздействием света в присутствии кислорода сорбиновая кислота окисляется, для повышения стабильности в ее растворы вводят кислоту лимонную (0, 001 —0, 5 %). Кроме кислоты сорби-новой в качестве консервантов применяют ее калиевую соль.
Кислота сорбиновая разрешена во многих странах для консервирования пищевых продуктов, так как менее токсична, чем обычно применяемые кислоты-консерванты, и безвредна для человека даже в больших количествах, способствует повышению иммунобиологической активности организма. Подобно другим кислотам-консервантам сорбиновая кислота наиболее эффективна при значениях рН 3, 0 — 4, 0. Она проявляет очень сильную фунгицидную активность, тормозит рост кишечной палочки, золотистого стафилококка, вульгарного протея и др.
Большой интерес представляет использование кислоты сорби-новой для консервирования галеновых препаратов (сахарный и лечебные сиропы, экстракты и др. ). Ее рекомендуют для консервирования концентрированных растворов, например, натрия бромида, кальция хлорида, микстуры Павлова. Кислота сорбиновая (0, 2 %) — эффективный консервант мазей, особенно эмульсионного типа, и линиментов промышленного производства (алоэ, лютенурина, синтомицина, госсипола и др. ).
При изготовлении лекарств для детей в качестве консервирующих составов используют смеси сиропа сахарного с небольшим количеством этанола или натрия бензоата, например, 82 части сиропа сахарного и 5 частей 80 % этанола.
В ряде случаев консерванты обладают не только антимикробной активностью, но и увеличивают биологическую доступность лекарственного препарата. Например, 0, 01 % раствор бензалкония хлорида увеличивает проникновение пилокарпина в глаз больше чем на 50 %. Бензалкония хлорид, диметилдодецилбензиламмо-ния хлорид являются представителями солей четвертичных аммониевых соединений. Как антибактериальные вещества эти соединения, относящиеся к группе синтетических катионоактивных ПАВ, получили значительное распространение.
Бензалкония хлорид (Benzalconii chloridum) — смесь хлоридов алкилметилбензиламмония является основным из них:

где R от С8Н17 доС18Н37.
Антибактериальная активность бензалкония хлорида проявляется при содержании в радикале от 8 до 16 атомов углерода, активность его сохраняется в присутствии большой группы лекарственных веществ. Он представляет собой кристаллическое вещество белого цвета, очень хорошо растворимое в воде. Водные растворы бесцветны, устойчивы к изменениям температуры и рН среды. При разведении 1: 50 000 бензалкония хлорид эффективен в отношении многих грамотрицательных, грамположительных бактерий и грибов и не обладает токсичностью. При использовании в мазях не оказывает раздражающего и аллергизующего действия. В концентрации 1: 10 000 его применяют почти во всех зарубежных странах преимущественно для консервирования глазных лекарственных форм, назальных капель, где требуются отсутствие раздражающего действия и быстрый бактерицидный эффект.
Другим соединением этой группы является отечественное вещество, синтезированное на кафедре органической химии ММА