Два способа описания природы на макроуровне.
Используя полученные знания на макроуровне в условиях теплового равновесия, можно вполне описать, задав макропараметры, характеризующие как макрообъекты, так и макросостояния. В то же время мы знаем, что каждый макрообъект состоит из известных микрообъектов – атомов, молекул, ядер и электронов. Иными словами, нужно выразить макропараметры через известные характеристики микрообъектов.
Микросостояние обязательно зависит от абсолютной температуры термостата Т, а в более общих случаях от химического потенциала m и давления Р.
В то же время макропараметры, являющиеся характеристиками макрообъектов самих по себе и имеющие аналоги на микроуровне (энергия, число частиц и т.п.), могут быть вычислены по известному микросостоянию в тепловом равновесии. В этом случае соответствующие макропараметры оказываются средними значениями микропараметров по совокупности микрочастиц, составляющих макрообъект., в частности, внутренняя энергия макрообъекта имеет вид
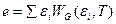 (10.7).
(10.7).
где  – характерные энергии микрочастиц, a WG – распределение Гиббса, имеющее смысл вероятности того, что микрочастица входит в состав групп с энергией
– характерные энергии микрочастиц, a WG – распределение Гиббса, имеющее смысл вероятности того, что микрочастица входит в состав групп с энергией  в условиях теплового равновесия, характеризуемого температурой термостата Т.
в условиях теплового равновесия, характеризуемого температурой термостата Т.
Что же касается энтропии, то она может быть вычислена путем усреднения самого распределения Гиббса. После такого усреднения всякая зависимость от характеристик микрочастиц в энтропии исчезает, и она оказывается зависящей от макропараметров, включая макропараметры Т и m, никак не связанные с характеристиками микрочастиц.
Таким образом, из изложенного следует, что в принципе возможны два независимых способа описания природы на макроуровне. В одном из способов описания используются макропараметры, характеризующие макрообъект и его макросостояние в условиях теплового равновесия. Все они равноправны и взаимосвязи между ними определяются уравнением состояния. Изменение энергии макрообъекта в равновесном макропроцессе определяются формулой
 (10.8),
(10.8),
называемым основнымтермодинамическимравенством. При этом энтропия S характеризует степень неупорядоченности макрообъекта.
В другом способе описания исходят из универсального микросостояния в тепловом равновесии, называемого распределением Гиббса. Оно зависит от макропараметров, которые в первом способе фиксировали макросостояние, и поэтому они не могут быть вычислены по распределению Гиббса. В то же время макропараметры, относящиеся к макрообъекту, например, энергию e можно вычислить как некие средние значения по распределению Гиббса. При этом то же самое изменение энергии макрообъекта в равновесном макропроцессе, что и выше можно записать в виде
 (10.9),
(10.9),
где первый член соответствует передаче теплоты Q, а второй член – работе (-dA).
Контрольные вопросы:
1. Какими особенностями обладает состояние теплового равновесия?
а. При заданных внешних условиях тепловое равновесие единственно.
б. Тепловое равновесие устойчиво.
в. Не зависит от начальных условий, с которых начался переход к тепловому равновесию.
г. Для его задания достаточно фиксировать всего несколько физических величин (макропараметры).
д. Всеми вышеперечисленными.
2. В чем различие между детерминированным и стохастическим движениями?
а. Наличие у стохастического движения энтропии.
б. Наличие у детерминированного движения энтропии.
в. Они одинаковы.
3. Что такое энтропия?
а. Энтропия – это величина, сохраняющаяся наряду с энергией в равновесных микропроцессах;
б. Энтропия – это величина, сохраняющаяся наряду с энергией в равновесных макропроцессах;
в. Энтропия – это микропроцесс;
г. Энтропия – это величина, сохраняющаяся наряду со скоростью в равновесных микропроцессах.
4. Как энтропия изменяется в равновесных процессах?
а. в ходе равновесных макропроцессов не меняется DSравновес=0;
б. в ходе равновесных макропроцессов DSравновес>0;
в. в ходе равновесных макропроцессов DSравновес<0;
г. в ходе равновесных макропроцессов не меняется DSравновес=0.