Уравнение Клаузиуса-Клапейрона
Равновесие в однокомпонентной двухфазной системе.
Таблица 20. с.344
Включение тех или иных генов, определяемых количеством повреждений в ДНК, приводит к разным по значимости клеточным ответам (начиная со стандартной репарации поврежденных нуклеотидов и кончая подавлением клеточного деления). Наиболее
изучена SOS-репарация у Е. coli, главными участниками которой являются белки, кодируемые генами rec А и lex А. Первый из них представляет собой полифункциональный белок Rec А, а второй (белок Lex А) является репрессором транскрипции большой группы генов, предназначенных для репарации ДНК бактерий.
Связывание Rec А с Lex А приводит к расщеплению последнего и соответственно к активации генов репарации. В свою очередь, индукция SOS-системы бактерии служит для фага к сигналом опасности и приводит к тому, что профаг переключается с пассивного на активный (литический) путь существования, вызывая тем самым гибель клетки-хозяина. SOS-система репарации выявлена не только у бактерий, но и у животных, и человека
Заканчивая рассмотрение механизмов репарации, нельзя не отметить, что исправление повреждений в ДНК тесным образом связано с другими фундаментальными молекулярно-генетическими процессами: репликацией, транскрипцией и рекомбинацией. Все
эти процессы оказываются переплетенными в общую систему
(сеть) взаимодействий, обслуживаемую большим числом разнообразных
белков, многие из которых являются полифункциональными
молекулами, задействованными в контроле реализации генетической
информации в клетках про- и эукариот. В то же время
очевидно, что природа «не скупится» на элементах контроля, создавая
сложнейшие системы коррекции тех повреждений в ДНК,
которые несут опасность для организма и особенно для его потомства.
Пример системы: вода и находящийся с ней в равновесии насыщенный пар.
Число степеней свободы
С = 1 + 2 – 2 = 1.
Это означает, что произвольно (независимо) можно изменять только один параметр. Для однокомпонентной системы, к которой неприменимо понятие концентрации, это один из внешних параметров – р или Т. Второй параметр будет являться функцией первого, т.е. между давлением и температурой фазового перехода существует взаимосвязь. Установим ее.
Условием термодинамического равновесия в системе является равенство химических потенциалов компонента во взаимодействующих фазах (нижний индекс отсутствует, поскольку компонент один):
 .
.
Химический потенциал – это мольная энергия Гиббса, которая в случае однокомпонентной системы является функцией только р и Т:
 .
.
Продифференцируем:
 ,
,
где 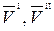 – мольные объемы I и II фаз, м3/моль;
– мольные объемы I и II фаз, м3/моль;  – мольные энтропии I и II фаз, Дж/(моль×К).
– мольные энтропии I и II фаз, Дж/(моль×К).
 ,
,
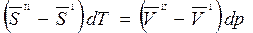 , (1)
, (1)
где 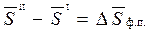 – изменение мольной энтропии при фазовом переходе (переходе вещества из фазы I в фазу II):
– изменение мольной энтропии при фазовом переходе (переходе вещества из фазы I в фазу II):
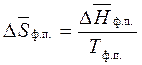 ,
,
где 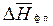 – мольная теплота фазового перехода; Тф.п. – температура фазового перехода.
– мольная теплота фазового перехода; Тф.п. – температура фазового перехода.
Подставим в (1):
 ;
;
 . (2)
. (2)
Уравнение (2) – уравнение состояния однокомпонентной двухфазной системы Клаузиуса-Клапейрона.
Применим полученное уравнение к различным процессам.
1. Фазовый переход конденсированная фаза – пар.
Например,

DНвозг.> 0,
DНисп.> 0.
Особенность таких систем состоит в том, что объем пара намного больше объема твердой и жидкой фаз и в уравнении (2) разность  можно заменить мольным объемом пара
можно заменить мольным объемом пара  :
:
 . (3)
. (3)
Вдали от критических точек пар ведет себя как идеальный газ, поэтому можно применить уравнение Менделеева-Клапейрона:
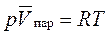 ,
,
 .
.
Подставим в (3):
 . (4)
. (4)
Из уравнения (4) следует, что для процессов испарения и возгонки производная dT/dp > 0. Это означает, что с повышением давления температура кипения жидкости и возгонки твердого тела повышается.
Решение дифференциального уравнения (4) имеет вид:
 . (5)
. (5)
С помощью уравнения (5) можно рассчитать:
1) температуру кипения (или возгонки) вещества Т2 при давлении р2, если известна температура кипения (возгонки) этого вещества Т1 при давлении р1 и средняя мольная теплота испарения (возгонки) вещества;
2) давление насыщенного пара индивидуального вещества р2 при температуре Т2, если известно давление насыщенного пара р1 при температуре Т1 и средняя мольная теплота испарения (или возгонки);
 3) среднюю теплоту испарения или возгонки вещества
3) среднюю теплоту испарения или возгонки вещества 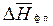 , если известны значения давления насыщенного пара вещества, по крайней мере, при двух температурах.
, если известны значения давления насыщенного пара вещества, по крайней мере, при двух температурах.
2. Фазовый переход
DНпл.> 0,
DНкр. < 0.
Для большинства веществ 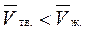 Исключение составляют: вода, глицерин, висмут. Для них
Исключение составляют: вода, глицерин, висмут. Для них 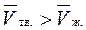
При плавлении льда  , а DНпл.> 0. Следовательно, в уравнении (2) производная dT/dp < 0. Это означает, что с повышением давления температура плавления льда понижается.
, а DНпл.> 0. Следовательно, в уравнении (2) производная dT/dp < 0. Это означает, что с повышением давления температура плавления льда понижается.