Вторую группу ИДС этого рода составляют дефициты подвижности фагоцитирующих клеток.
Врожденные дефекты фагоцитарной системы.
Классическим примером врожденного дефекта фагоцитарной системы является хронический грануломатоз детей. Б.Грэй и Р.Гуд (1972) назвали эту болезнь синдромом парадоксов. Дети, страдающие данным заболеванием, проявляют высокую степень устойчивости к вирулентным стрептококкам, менингококкам, пневмококкам, но оказываются весьма подверженными инфицированию маловирулентными стафилококками, кишечными палочками, грибами и другими сапрофитами.
Эти микробы захватываются макрофагами и лейкоцитами, однако фагоцитоз оказывается незавершенным. Микробы не перевариваются и фагоциты выполняют роль «капсул» защищающих их от специфических факторов иммунного ответа, в частности от антител.
Организм не очищается от микробов, несмотря на гипергаммаглобулинемию.
В лимфатических узлах печени и легких формируются гранулы, отличительным признаком которых служат гистиоциты, содержащие липохромные включения.
Причиной смерти является прогрессивный деструктивный процесс в легких за счет пролиферации и распада гранулем, заканчивающийся сепсисом.
Первичная причина нарушения фагоцитарного процесса заключается в метаболическом дефекте – неспособности клеток продуцировать перекись водорода (Н2О2), что необходимо для нормального процесса обработки бактерий внутри фагоцита. Низкий уровень перекиси является следствием недостаточности НАДФ-оксидазы в фагоцитах больных. Именно этот фермент обеспечивает перенос электронов на кислород с последующим образованием Н2О2.
Хронический грануломатоз относится к группе таких дефектов фагоцитарной системы, которые характеризуются нарушением бактериоцидного эффекта фагоцитов.К ним же относятся дефекты миелопероксидазной, пируваткиназной и глюкозо-6-фосфатдегидрогеназной активности.
Практически во всех случаях развивается повышенная чувствительность к бактериальным инфекциям.
Лечение симптоматическое, хирургическое с применением антибиотиков. Делаются попытки трансплантации фагоцитов.
СИНДРОМ ПРИОБРЕТЕННОГО ИММУНОДЕФИЦИТА {СПИД)
Первое сообщение о неизвестном заболевании — синдроме приобретенного иммунологического дефицита (СПИД) опубликовано в 1981 г. в США. За истекший период количество сообщений о нем возросло, и если вначале все они относились к США и касались единичных случаев, то сейчас география болезни значительно расширилась, а количество к началу 1986 г. составляло 16000. Больные СПИДом были обнаружены в Африке, Европе, Азии и Латинской Америке. Заболевание приобретает эпидемический характер,протекает тяжело и имеет неблагоприятный прогноз. Основные характерные проявления СПИДа — инфекционные процессы, вызываемые условно-патогенными бактериями, вирусами и грибами, и злокачественные опухоли, протекающие на фоне специфического иммунодефицита.
Максимальная заболеваемость СПИДом относится к США. Ежедневно в США выявляется не менее трех-пяти новых больных СПИДом, а в каждый полугодовой интервал число их увеличивается в геометрической прогрессии. В США выявлено 80 % из числа заболевших. В Европе к 1986 г. было зарегистрировано около 1000 заболеваний. Заболевание обнаружено практически уже во всех европейских странах: Франции, Великобритании, Дании, Швейцарии, Испании, Чехословакии, Бельгии, Финляндии. На начало 1988 г. в мире было более 100000 больных СПИДом в 130 странах и от 5 до 10 млн. инфицированных вирусом носителей. В ближайшие годы число больных по прогнозам увеличится в 10 раз.
Первоначально СПИД был обнаружен у молодых мужчин гомосексуалистов, но затем он выявлен и в других группах людей. Группы больных представлены также женщинами — половыми партнерами больных СПИДом мужчин, лицами, пристрастными к внутривенному введению наркотиков, а также ведущими беспорядочную половую жизнь, имеющими большое количество половых партнеров, жителями определенных географических зон, таких как о. Гаити, Центральная и Экваториальная Африка, больными гемофилией — реципиентами препаратов крови. У 8—10 % населения Экваториальной Африки в крови обнаружены антитела к вирусу — возбудителю СПИДа. Более 90 % больных — молодые люди 20—49 лет, большинство заболевших — мужчины.
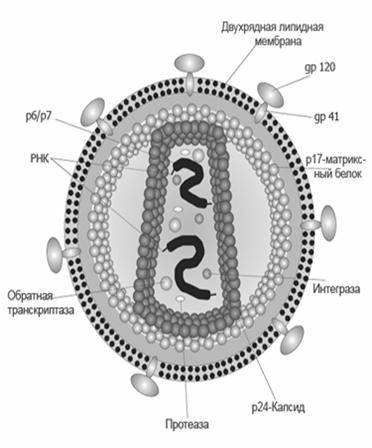
| Возбудитель СПИДа выделен в 1983 г. Л. Монтенье и сотрудниками в Институте Пастера во Франции и Р. Галло в США. Им оказался Т-лимфоцитотропный ретровирус, который был назван HTLV, а позже получил название HIV (Human Immunodeficiency Virus). Сегодня известно несколько серологических разновидностей семейства ретровирусов СПИДа: HIV -1, HIV -II, HIV – III. Биологическая особенность вируса — способность развиваться внутри других вирусов. | |
| Цепь РНК вируса состоит из 9193 нуклеотидов, содержащих 3 гена, кодирующих белки капсида, обратную транскриптазу и другие компоненты вируса. Характерной особенностью ретровирусов является наличие в корпускулах вирусов фермента обратной транскриптазы. Посредством этого фермента синтезируется ДНК-копия РНК-хромосомы | 
| |
вируса, которая встраивается в геном хозяина и с помощью своих сигналов заставляет ДНК хозяина синтезировать вирусный материал и осуществлять сборку вирусных частиц. Вирусы СПИДа убивают Т-хелперы, а также вызывают их раковое перерождение. В результате поражения вирусом СПИДа количество
Т-хелперов в крови снижается.
Инкубационный период может длиться до 10 лет. Считают, что только 50 % инфицированных вирусом людей заболевают СПИДом. К этому приводит сочетание ряда факторов и в первую очередь, видимо, вирусные инфекционные заболевания, при которых в крови и лимфоидных органах появляется очень большое количество Т-хелперов, поражающихся вирусом. Патогенетическое значение может иметь повышение активности нормальных киллеров, осуществляющих лизис не только пораженных вирусом, но и нормальных Т-хелперов. Наступающее при этом нарушение регуляторного действия Т-хелперов приводит к угнетению Т-клеточного иммунитета, что, в свою очередь, приводит к инфекции слизистых оболочек, вызванной условно-патогенной микрофлорой.
Возбудитель СПИДа содержится в крови и семенной жидкости больного. Заражение происходит только тремя способами: половым путем, при переливании инфицированной донорской крови или при пользовании общими шприцами и от инфицированной матери трансплацентарным путем во время беременности. У гомосексуалистов благоприятствующим моментом, вероятно, служит ректальная микротравматизация. Распространение СПИДа среди наркоманов, часто пользующихся общей иглой, обусловлено переносом возбудителя заболевания инфицированным инструментарием аналогично передаче эпидемического гепатита. СПИД не передается через воздух, воду и пищу, при пожатии рук, при поцелуях (но не половых), через собак, кошек, через кровососущих комаров. Не опасны обычные бытовые и социальные контакты с больными СПИДом, но можно заразиться через общие зубные щетки, бритвы, ножницы. При половых контактах от заражения предохраняет применение презервативов.
Патогенез СПИДа пока гипотетичен. Одним из основных его проявлений является иммунодепрессия, благоприятствующая развитию опухолевых процессов и/или агрессивных свойств условно-патогенной микрофлоры. Предполагается, что инфекционный агент может индуцировать онкогенез, стимулируя Т-клеточную пролиферацию с преобладанием одного клона. Высказывается также предположение о принадлежности СПИДа к аутоиммунным заболеваниям с направленностью аутоагрессии на Т-хелперы, возможно, вследствие возникновения антител против сперматозоидов, реагирующих перекрестно с Т-клетками. Иммунологическое обследование здоровых гомосексуалистов реципиентов спермы обнаружило у них высокую частоту аллогенной иммунизации, не выявленную у гомосексуалистов — доноров спермы. В эксперименте доказано, что содержащиеся в сперме человека полиамины (спермин, спермидин и их предшественники) оказывают иммунодепрессивное действие, а инфекционный процесс, в частности вызванный цитомегаловирусом, резко увеличивает биосинтез полиаминов. Иммунодепрессивное действие спермы может быть также связано с ее трансглютаминазной активностью. Именно с содержанием трансглютаминаз в некоторых лекарственных препаратах, в частности противосвертывающих, связывают их депрессивное влияние. По-видимому, продолжительная иммунодепрессия, обусловленная приемом наркотиков, лечением кортикостероидами или другими иммунодепрессантами, также может способствовать развитию СПИДа.
Из мононуклеаров периферической крови больных СПИДом выделено вещество — растворимый супрессорный фактор (РСФ), оказывающий ингибирующее действие на Т-лимфоциты. Фактор отличается от аналогично действующего супрессорного фактора, выделяющегося Т-лимфоцитами, активированными Кон-А. Предполагают, что с продукцией этого фактора связано развитие СПИДа. Возможно, что СПИД — генетически детерминированная патология иммунной системы, проявление которой провоцируется инфекцией.
Основной путь передачи инфекции — половой. Источником инфекции наиболее часто являются здоровые носители обоих полов, т. е. лица с бессимптомной инфекцией, не подозревающие о том, что они заражены вирусом СПИД. Показано, что вирус проникает в Т-хелперы через рецепторы на поверхностной мембране лимфоцитов, представленные белком СD4. Пораженные вирусом Т-хелперы элиминируются из организма, что является главной причиной иммунодефицита при СПИД. Посредством обратной транскриптазы РНК генома вируса трансформируется в двухцепочечную ДНК и включается в геном клеток-мишеней, где представляет собой провирус. ДНК вируса воспроизводится при делении зараженных клеток, которые являются носителями латентной, поддерживающейся таким путем в течение ряда лет инфекции, способной переходить в активную форму. Установлено, что оболочечный гликопротеин 120 (gр. 120) вируса СПИД высвобождается из вирусных корпускул и связывается с молекулами СD4, активированных в результате инфицирования организма другими вирусами и бактериями Т-хелперов. Комплексы gр.120-СD4 распознаются Т-киллерами. Этот механизм приводит к разрушению и Т-хелперов неиифицированных HIV.
Углеводные структуры gр120 распознаются антителами, а аминокислотная часть гликопротеина индуцирует клеточные реакции у больных. Наиболее интенсивный клеточный ответ вызывает структурный компонент НIV-1 —р24. Имеются данные о том, что этот протеин выявляется у части зараженных лиц, где НIV не выделяется. На этом основании рекомендуется для диагностики зараженности одновременно выделять НIV и выявлять р24.
В макрофагах НIV не погибает и фагоцитировавшие вирус макрофаги становятся резервуаром и переносчиками инфекции. Макрофаги обладают способностью проникать через гематоэнцефалический барьер. При занесении ими инфекции в мозг возникают поражения центральной нервной системы: энцефалиты, менингиты, миэлопатии, невропатии и др. На аутопсии признаки поражения ЦНС обнаруживаются 75 % больных СПИД.
Заболевания, вызываемые НIV-1 в особенности высоковирулентными его штаммами, протекают более тяжело. Такие штаммы могут возникать под воздействием факторов, повреждающих ДНК вирусов в клетке и в результате мутаций. НIV-1, по-видимому, перешел к человеку от приматов 20—-100 лет тому назад и циркулировал среди небольших племен Центральной Африки, мало общавшихся с внешним миром. Тысячи случаев заболевания СПИД имели место в 1970-е годы.
Для лечения СПИД применяются десятки противовирусных препаратов и около 50 иммуномодуляторов. Растворимый СD4 в организме будет соединяться с корпускулами вируса, препятствуя их адсорбции на рецепторах Т-хелперов. Проводятся клинические испытания этого препарата. Вакцина против СПИД, по-видимому, будет получена из гликопротеиновых и белковых компонентов вируса, так как геном аттенуированных и инактивированных НIV, внедряясь в ДНК клетки, может активировать все латентные вирусы и стимулировать появление новых патогенных вирусов. Изучается возможность использования для вакцинации антиидиотипических антител к рецептору Т — хелперов СD4.
Клиника. СПИД — нозологически самостоятельное заболевание с тяжелым течением и плохим прогнозом. Летальность составляет 40—75 %, а при более длительном наблюдении 80 и даже 100 %. Болеют люди всех возрастов: СПИД описан у детей семимесячного возраста и после 70 лет.
Заболевание протекает относительно длительно, его часто можно разделить на три периода. Инкубационный период колеблется от 6 до 24—27 месяцев, затем обычно наступает стадия лимфаденопатии, продолжающаяся 2—4 г., и наконец, завершающая стадия полного клинического развития, приводящая к смерти в течение 1 месяца — 1 года. Только 16 % больных СПИДом живут более 3 лет от начала заболевания. С начала клинически развернутой картины у больного появляется и прогрессирует общая слабость, ночные поты, повышается температура чаще до субфебрильпых цифр, но иногда и более высоких, беспокоит упорная диаррея, сопровождающаяся прогрессирующим снижением массы тела. На этом фоне появляются очаги воспалительных процессов. Чаще всего воспалительный процесс имеет легочную локализацию в виде пневмонии, вызванной Pneumocystis carinii. Поражения легких наблюдаются в 45 % летальных исходов.
Часто в патологический процесс вовлекается пищеварительный канал. Поражается слизистая оболочка на всем протяжении, начиная с ротовой полости, включая желудок, тонкие и толстые кишки, желчный пузырь, иногда вплоть до некротического поражения, в связи с чем могут возникать изъязвления, перфорации, асцит.