ИММУНОЛОГИЯ
Классификация сред по степени агрессивного воздействия
Понятие о долговечности.
Коррозия бетона и меры борьбы с ней.
На бетонные и ж/б конструкции, эксплуатируемые в промышленных, гражданских, жилых, сельскохозяйственных зданиях могут действовать агрессивные среды.
Долговечность конструкций определяется стойкостью, как бетона, так и арматуры при воздействии на них агрессивной среды.
Степень агрессивного воздействия на бетоны и ж/б конструкции определяется для жидких сред - наличием и концентрацией агрессивных агентов, температурой, величиной напора или скоростью движения жидкости у поверхности конструкции и зависит от ρ бетона; для газовых сред видом и концентрацией газов, растворимостью их в воде, влажностью и температурой среды; для твердых тел- (соли, аэрозоли, пыли) - дисперсностью , растворимостью в воде, влажностью окружающей среды.
По показателю бетоны условно делятся на три вида, характеризующиеся водосодержанием бетонной смеси при затворении, маркой бетона по водонепроницаемости и водопоглащением бетона по массе. Степень агрессивного воздействия жидких сред зависит от концентрации водородных ионов рН, содержание свободной углекислоты, магнезиальных солей, едких щелочей, сульфатов.
Концентрация ионов водорода характеризует химическую активность жидких агрессивных сред. В кислой среде концентрация ионов Н больше, а в щелочной - малая. С понижением значение рН степень агрессивного воздействия среды на бетон возрастает. Жидкие агрессивные среды, содержащие углекислоту, активно взаимодействуют с цементным бетоном, разрушая его. Однако, агрессивность этих сред зависит от концентрации углекислоты и жесткости воды.
Агрессивными газами являются: кислород, водные пары, углекислый газ, аммиак, сернистый ангидрид, сероводород, окислы азота, хлор, хлористый водород, фтористый водород. В зависимости от вида и концентрации газов газовоздушные среды условно делятся на 4 группы: А, В, С, Д (табл.1).
Указанные агрессивные газы – кислые, и при растворении их в воде образуются кислоты. Степень агрессивности растворов, как и самих газов, возрастает от группы А до группы Д, т.е. по мере повышения концентрации растворенных газов испытывают воздействие газовоздушных сред при температуре до +50оС. При повышение температуры до +70оС степень агрессивного воздействия среды увеличивается примерно на одну ступень. По относительной W все газовоздушные среды относятся к одной из трёх зон: сухой – с относительной W < 60%; нормальной – 61-75% и влажной – более 75%. Область применения различных строительных конструкций в зависимости от зоны влажности, группы агрессивности и степени воздействия газовоздушных сред определена СНиП 11-28-85.
Таблица 1
| Газ | Нормативная концентрация газа (мг/м3) в среде группы | |||
| А | В | С | Д | |
| Двуокись С | До 2000 | Свыше 2000 | - | - |
| Сернистый ангидрид | До 0,5 | Свыше 0,5 до 10 | Свыше 10 до 200 | Свыше 200 |
| НF | До 0,05 | Свыше 0,05 до 5 | Свыше 5 до 10 | Свыше 10 |
| НS сероводород | До 0,01 | Свыше 0,01 до 5 | Свыше 5 до 100 | Свыше 100 |
| Окись азота | До 0,1 | Свыше 0,1 до 5 | Свыше 5 до 25 | Свыше 25 |
| Cl | До 0,1 | Свыше 0,1 до 1 | Свыше 1 до 5 | Свыше 5 |
| HCl | До 0,05 | Свыше 0,05 до 5 | Свыше 5 до 10 | Свыше 10 |
Степень их агрессивного воздействия на бетон определяется специальными нормами по антикоррозийной защите строительных конструкций (СНиП 2.03.11-85)
В зависимости от глубины разрушения бетона при коррозии различают слабо-, средне- и сильноагрессивные среды и неагрессивные.
Таблица 2
Допустимая глубина (см) разрушения бетона за 50 лет эксплуатации
| Степень агрессивности воды-среды | Конструкции | |
| железобетонные | бетонные | |
| Неагрессивная Слабоагрессивная Среднеагрессивная Сильноагрессивная | 1-2 2-4 более 4 | 2-4 4-6 Более 6 |
При взаимодействии на бетон воды-среды может происходить разрушение бетона, характеризующиеся I, II, или III видом коррозии. Разрушение конструкции наступает вследствие недостаточной стойкости бетона.
Поэтому при проектировании конструкций необходимо учитывать состав агрессивной среды, условия службы конструкции, правильно выбрать материалы и назначить плотность бетона, чтобы обеспечить долговечность конструкции.
Коррозия бетона в газовой среде протекает, как правило, при наличии влаги, и возникающие при этом процессы не отличаются практически от коррозии бетона в водной среде.
Жесткость воды в основном определяется наличием растворенных в ней солей Са и Мg. Различают жесткость карбонатную, некарбонатную и общую. При отсутствии в воде карбонатов может происходить растворение цементного камня – его выщелачивание (коррозия) и снижение прочности бетона. Воздействие воды, содержащей магнеугольные соли, приводит к быстрому разрушению бетона в результате коррозии. Коррозия бетона от действия едких щелочей наблюдается на предприятиях химической промышленности. Процесс разрушения бетона вызывается отложением щелочи в порах бетона с образованием за счет углекислоты окружающего воздуха карбонатов Na2CO3 и K2CO3. одновременно со щелочью взаимодействует и алюминатная составляющая портландцемента с образованием растворимых алюминатов Na и К.
В природных и некоторых других водах содержатся сульфаты. Такие воды вызывают сульфатную коррозию.
Кроме водных растворов солей, кислот и щелочей, жидкими агрессивными средами являются также масла, нефтепродукты и растворители. Растительные и животные масла представляют большую опасность для бетона, чем минеральные.
Теперь рассмотрим газовую среду (V ).
Степень агрессивного воздействия твердых сред на бетон и железобетон
показана в табл. 3.
Таблица 3
| Конструкция | Степень воздействия твердых сред при их зоне влажности и характеристике | ||||||||
| сухая | нормальная | влажная | |||||||
| малорастворимая | хорошо растворимая малогигроскопичная | хорошо растворимая гигроскопичная | малогигроскопичная малорастворимая | хорошо растворимая малогигроскопичная | хорошо растворимая гигроскопичная | малорастворимая | хорошо растворимая малогигроскопичная | хорошо растворимая гигроскопичная | |
| Бетонные и асбесто-цементные Желез-бетонные | Н Н Ср Н Сл Ср | Н Сл Ср Н Ср Cu | Н Ср Ср Сл Сл Cu | ||||||
По растворимости твердые среды делятся на малорастворимые (менее 2 г/л) и хорошо растворимые (более 2 г/л).
В большинстве случаев на конструкции действует многофазная среда. Так, например воздушная среда промышленных предприятий содержит в своем составе взвешенную жидкостную фазу в виде тумана и твердую в виде пыли.
Виды коррозии бетона
Предложено подразделять коррозию бетона на три основных вида.
Коррозия первого вида обусловлена растворением в воде составных частей цементного камня. Особое развитие коррозия бетона первого вида получает при фильтрации воды через бетон. Наибольшее распространенным случаем такой коррозии является вымачивание водой Ca (OH)2 , это физический вид коррозии, приводящей к увеличению пористости цементного камня. Наиболее распространенным случаем коррозии является выщелачивание водой.
Установлено, что при потере примерно 10% CaO снижение прочности цементного камня достигает 10%, при потере 20% CaO – 25% и при потере 33% CaO наступает полное разрушение цементного камня. При снижении содержания CaO в цементном камне интенсифицируется и коррозии арматуры в ж/б конструкциях.
При присутствии в воде – среде солей Ca типа Ca(HCO) CaCO уменьшается выщелачивание гидрата окси Ca из цементного камня.
Скорость коррозии первого вида уменьшается за счет карбонизации бетона, поскольку при этом образуется нерастворимое соединение – CaCO3 (Ca(OH)2 + CO2 → CaCO3 + H2O), понижается ионная сила раствора и повышается непроницаемость цементного камня.
Для предупреждения коррозии первого вида выработаны следующие мероприятия. Поскольку выщелачивание происходит при развитой пористости цементного камня, необходимо:
1) Создать бетоны повышенной плотности, как и за счет снижения В/Ц, так и за счет интенсивного уплотнения бетона.
2) Необходимо использовать цементы с ограниченным содержанием 3-х кальциевого силиката (C3S)
3) Вводить в цемент тонкомолотые добавки (минеральные) которые связывая гидроокись Ca в нерастворимые соединения способствуют снижению интенсивности коррозионного разрушения бетона. Предпочтительным можно считать пуццолановый цемент.
4) Карбонизация поверхностного слоя бетона, образующийся на поверхности бетона уплотненный карбонатный слой будет препятствовать выщелачиванию бетона.
5) Целесообразно создавать гидроизоляцию поверхности бетонных конструкций в виде оклейки, облицовки или пропитки поверхностного слоя бетона гидроизоляционных материалов.
Коррозия второго вида:
Коррозия второго вида проявляется в образовании легкорастворимых или аморфных размываемых водой веществ при взаимодействии цементного камня с агрессивными растворами и вызывается действием неорганических кислот.
а) Ca (OH)2 + 2 HCl → Ca Cl2 +2 H2O (легкорастворимыми)
Аналогично с серной и азотной кислотой образуется Ca SO . 2H2O и Ca(NO3)2
Кислоты воздействуют не только на гидрат окиси Ca, но и на минеральные компоненты портландцемента:
3 CaO . 2SiO2 . 3H2O + 6 HCl =CaCl2 + Si(OH)4 + SiO2 . 4 H2O
Образующиеся соли Са легко вымываются Н2О, таким образом коррозия ΙΙ вида переходит в коррозию Ι вида, которая является причиной разрушения цементного камня. Если продукты реакции малорастворимые, они закрывают поры цементного камня и препятствуют проникновению агрессивной среды внутрь, замедляя коррозию, т.е. играют роль ингибирующего вещества.
Разница в стойкости цементов к действию сильно концентрированных кислот почти не ощутим, поскольку разрушение происходит очень быстро. По стойкости к действию кислот слабой концентрации цементы можно расположить в таком порядке: глиноземистый цемент, пуццолановый ПЦ и обычный ПЦ (как при коррозии Ι вида).
В грунтовых водах часто присутствует углекислота Н2СО3, образующаяся в результате биохимических процессов. При углекислотной коррозии происходит реакция: Са (ОН)2 + Н2СО3 → СаСО3 + 2Н2О, а затем:
СаСО3 + Н2СО3 → Са (НСО3)2 , т.е. образуется легкорастворимое вещество.
При этом, чем больше содержится Н2СО3 , тем выше кислотные свойства раствора и скорость коррозии.
При углекислотной коррозии предпочтительно использование для бетонных и ж/б конструкций тех же цементов, что и при действии других кислот.
Для защиты от коррозии ΙΙ вида необходимо: 1) создавать бетоны повышенной плотности; 2) использовать цементы с большим содержанием гидрата окиси Са; 3) обеспечивать защиту поверхности бетонных конструкций за счет оклейки или облицовки водонепроницаемыми коррозионностойкими материалами, либо нанесение лакокрасочных покрытий.
Коррозия ΙΙΙ вида и пути её предотвращения
Данный вид коррозии – это разрушение цементного камня от внутренних напряжений при накоплении в порах и капиллярах малорастворимых солей.
В порах бетона может происходить накопление солей как в результате кристаллизации продуктов химической реакции, протекающей между агрессивной средой и цементным камнем, так и вследствие кристаллизации солей при их поглощении из агрессивных растворов.
Наиболее распространенной разновидностью коррозии, приводящей в результате кристаллизации продуктов реакции между цементным камнем и агрессивной средой, является сульфатная.
При действии на бетон сульфат натрия вступает в реакцию с гидратом окиси Са цементного камня:
Са (ОН)2 + Na2 SО4 + 2 Н2О → Са SО4 . 2 Н2О + 2Na ОН
2Na ОН – является хорошо растворимым веществом, которое легко вымывается из цементного камня. Образование гипса может сопровождаться некоторым увеличением объёма продуктов реакции.
Находящийся в твердой фазе 3-х кальциевый гидроалюминат взаимодействует с гипсом с образованием гидросульфоалюмината Са:
3СаSО4 . 2Н2О + СаО . Аl2О3 ∙6Н2О + 23Н2О → 3 Са SО4∙ 3СаО . Аl2О3 ∙31 Н2О.
Объем его увеличивается в 2 раза по сравнению с объемом исходных продуктов, вследствие чего возникают напряжения в цементном камне и бетоне, достигающие предела их R .
Вначале коррозия III вида проявляется в виде образования на поверхности цементного камня только пленки из кристаллического гипса, даже образуется скопление кристаллов гипса и гидросульфоаллюмината кальция - внутри цементного камня. Скопление гипса происходит в местах наличия Cа(OH)2 . Растворенные в воде сульфаты повышают ионную силу раствора, что обуславливает развитие коррозии I вида (растворения цементного камня), а также коррозии II вида (за счет обменных реакций между составляющими цементного камня и окружающей среды). Присутствие в растворе солей, не принимающих участие в образовании гидросульфоалюмината кальция (NaCl, NaNO3, KCL и др.), а также обуславливается ионной силой, силой раствора и как следствие предупреждается образование и рост кристаллов гидросульфоалюмината Ca.
Разновидностью коррозии бетона III вида является разрушение бетона при кристаллизации солей в порах и капиллярах цементного камня и бетона вследствие их конденсации из агрессивных сред (растворов). В капиллярно-пористое тело бетона соли проникают при капиллярном подсосе из растворов из агрессивной жидкой среды, осаждающиеся в аэрозольном виде (в виде пыли). Соли на поверхности бетона адсорбируют пары H2O из окружающего воздуха и образуют концентрированные солевые растворы, которые вследствие проявления капиллярных сил проникают внутрь тела бетона. Механизм разрушения бетона солями заключается в следующем: растворы солей мигрируют в теле цементного камня и бетона. Микрокапиляры малых размеров пропускают только чистую воду, а соль останется в более крупных порах и капиллярах. При постепенном накоплении солей в крупных порах их растворы становятся насыщенными и кристаллизируются.
При кристаллизации возникает давление кристаллов на стенки пор, вызывающее появление значительных растягивающих напряжений в теле бетона, вплоть до разрушающих.
Подтверждением такому объяснению механизма солевой коррозии является тот факт, что при введении воздухововлекающих добавок и при использовании пористых заполнителей бетоны оказывают большее сопротивление солевой коррозии. Обусловлено это тем, что поры в зернах заполнителей и поры в цементном камне становятся буферным пространством, где постепенно накапливаются соли. За счет этого удлиняются сроки достижения бетоном критического состояния. Сопротивление бетона возрастает тем больше, чем больше пористость заполнителя.
Меры защиты от коррозии
1. Для защиты бетона от солевой коррозии необходимо: применять бетоны с малым водосодержанием (с низким В/Ц); тщательно уплотнять бетонную смесь; использовать воздухововлекающие добавки в бетоне и добавки, уплотняющие цементный камень; применять для получения бетона пористые заполнители, а также цементы, обеспечивающие высокую плотность цементного камня (например портландцемент без минеральных добавок); отводить агрессивные солевые растворы от поверхности конструкции, либо изолировать их путем устройства лакокрасочных, склеечных или облицовочных защитных покрытий, препятствующих проникновению растворов солее внутрь бетона.
2. Борьбу с коррозией III вида следует вести, принимая во внимание следующее:
а) в бетонах на глиноземистом цементе или цементах с малым содержанием Cа(OH)2 (например пуццолановом портландцементе) невозможно образование многоосновных гидроаллюминатов кальция, чем ограничивается или исключается возможность образования гидросульфоаллюмината кальция;
б) введение в бетонную смесь воздухововлекающих добавок (СHB) пластифицирующих веществ, химических добавок (CaCl2), повышающих растворимость гидрата окиси кальция и гипса, кремнеорганических веществ, способствует повышению стойкости цементного камня и бетона к коррозии;
в) эффективно создание защитных слоев на поверхности бетонной конструкции в виде оклеечной, облицовочной или лакокрасочной изоляции.
Дополнение к коррозии II вида:
Действие растворов щелочей.
Строительные конструкции предприятий химической и легкой промышленности подвергаются агрессивному воздействию растворов щелочей: каустической соды, едкого натрия, кальцинированной соли. Коррозия бетона, наблюдаемая в этом случае, вызывает постепенное снижение прочности R бетона. Скорость протекания коррозии зависит от вида щелочи, концентрации раствора, температуры среды, продолжительности агрессивного воздействия, пористости бетона и цементного камня в нем, характера проникновения раствора в тело бетона.
Разрушение бетона происходит вследствие повышения растворимости составляющих цементного камня, содержащих кремнезем и глинозем и образования щелочноземельных силикатов и алюминатов при взаимодействии этих частиц со щелочами.
1. Растворимость гидрата окиси кальция в цементном камне при контактировании с растворами щелочей вследствие присутствия ионов он значительно понижается.
2. Клинкерные минералы портландцемента по–разному взаимодействуют со щелочами. Наибольшую активность проявляет С3А, несколько меньшую С4АF, еще меньшую С2S и совсем малую С3S. Алюминатные составляющие в растворе едкой щелочи относительно быстро разрушаются. Алюминаты кальция Са склонны к гидролизу и распаду в воде. Эта особенность поведения алюминатов обуславливает снижение щелочестойкости цементного камня с 1,5 до 5 раз в случае увеличения С3А в составе портландцементного клинкера в 2 раза.
3. Бетоны на портландцементе показали большую стойкость в растворах щелочей, чем на пуццолановом и шлакопортландцементе это объясняется повышенной пористостью цементного камня и большим содержанием растворимого щелочью SiO2.
Коррозия бетона при растворении щелочами составляющей цементного камня может быть отнесена к коррозии II вида, которая в последствии переходит в коррозию I вида.
4. При карбонизации щелочей углекислотой окружающего воздуха происходит кристаллизация образующихся углекислых солей и возможно разрушению бетона. Это коррозия III вида.
5. Не менее опасна коррозия бетона вследствие разрушения щелочами заполнителей. Появление коррозии обусловлено взаимодействием щелочей с SiO2 заполнителей и разрушением его. Это приводит к снижению прочности бетона, вплоть до полного разрушения – здесь также коррозия III вида. Необходимо отметить, что бетоны на заполнителях из карбонатных и ультраосновных горных пород имеют преимущества перед бетонами на заполнителях из кислых горных пород.
Бетоны разрушаются более интенсивно при одновременном накоплении в их структуре нерастворимых новообразований и снижении прочности цементного камня вследствие растворения его составляющих. С повышением температуры растворов щелочей значительно ускоряются процессы коррозии бетона.
Агрессивность растворов кислот
Бетон на П/Ц весьма нестоек к взаимодействию растворов кислот.
Наиболее агрессивны по отношению к цементному камню являются минеральные кислоты – соляная, серная и азотная. При воздействии 1% - растворов этих кислот бетон разрушается в течение нескольких месяцев, менее агрессивная фосфорная кислота. 1% растворы этой кислоты малоагрессивны к цементному камню, однако с повышением концентрации кислоты в растворе ее агрессивность возрастает. 5%-ный раствор быстро разрушает цементный камень.
Воздействие магнезиальных солей
Соли Mg, присутствуют в морской воде и часто в грунтовых водах и производственных, вызывают магнезиальную коррозию цементного камня, при котором образуются малопрочные соединения с аморфной малосвязанной структурой. Взаимодействуют магнезиальные соли с Ca(OH)2 по условной реакции:
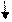 Ca(OH)2 + MgCl2=CaCl2 + Mg(OH)2
Ca(OH)2 + MgCl2=CaCl2 + Mg(OH)2
CaCl2 – легко растворяется H2O
Mg(OH)2 – выпадает в осадок в виде рыхлой и плохо растворимой в К2О массы белого цвета. Растворение извести нарушает структуру цементного камня, что в результате сказывается на снижение его R.
Более агрессивным является магний-сульфатное воздействие на цементный камень:
Ca(OH)2 + MgSO4 + 2H2O → CaSO4 . 2H2O +Mg(OH)2 ↓
 образуется двуводный гипс. Имеет объём, который больше суммарного объёма исходных веществ. Это может вызвать появление напряжений в цементном камне. Если Ca(OH)2 полностью вступит в реакцию, то будет происходить взаимодействие сульфата Mg c C3A6H
образуется двуводный гипс. Имеет объём, который больше суммарного объёма исходных веществ. Это может вызвать появление напряжений в цементном камне. Если Ca(OH)2 полностью вступит в реакцию, то будет происходить взаимодействие сульфата Mg c C3A6H
3CaAl2O3∙6H2O + 3MgSO4∙7H2O → (CaSO4∙2H2O) + 2Al(OH)3↓ + 3Mg(OH)2 +H2O;
3CaO∙2SiO2∙3H2O + 3MgSO4∙7H2O +7H2O → 3(CaSO4∙2H2O) + 3Mg(OH)2↓ + 2(SiO2∙4H2O.
Mg(OH)2 и Al(OH)3 - выпадают в осадок, или выщелачиваются H2O из цементного камня, структура которого ослабляется, гипс постепенно накапливается в растворе, после полного насыщения раствора образуется его твердая фаза.
C3A∙H2O в начале реакции с сульфатом Mg образуют гидросульфааллюминат Ca. Однако этот продукт неустойчив в среде сульфата Mg и даже разлагается.
При малых концентрациях солей в растворах реакции протекают на поверхности бетона и выделяющийся Mg(OH)2 - образует плёнку, препятствующую проникнуть соли внутрь. В этом случае за счет выноса Cа(OH)2 из внутренних слоев проявляется коррозия I вида.
При большой концентрации соли реакционная способность раствора велика, содержание гидрата окиси Са недостаточно для ее нейтрализации, поэтому раствор соли диффундирует внутрь бетона. При этом проявляется коррозия III вида.
Стойкими к коррозии этого вида являются бетоны на цементах с большим содержанием извести – CaO, чем больше содержание извести, тем дольше протекает реакция и дольше длится процесс выноса продуктов реакции из цементного камня. Весьма стойкими являются цементный камень на глиноземистом цементе, поскольку в его составе нет Ca(OH)2. Сульфат Сa взаимодействует в цементном камне с высокоосновными алюминатами Ca, объем образующегося ГСАК превышает V исходных продуктов. Это увеличение объема обуславливает появление в пористой структуре цементного камня напряжений, приводящих к его разрушению.
При наличии в воде - среде (природных водах, в частности морской) NaCl затрудняется образование ГСАК в твёрдой фазе и уменьшается возможность сульфатной коррозии цементного камня.
Более опасным для бетона является воздействие растворов солей, не вступающих в химическое взаимодействие с составляющими цементного камня, при наличии испаряющей поверхности и попеременном насыщении цементного камня или бетона раствором соли и высушивании их.
Раствор соли в цементном камне или бетоне мигрирует к испаряющей поверхности под действием капиллярных сил. В зависимости от структуры цементного камня кристаллизация соли может происходить непосредственно на его поверхности или некотором поверхностном слое. В первом случае концентрация Ca (OH)2 возрастает (имеет I вид коррозии).
Если же размеры пор достаточно велики, испарение воды происходит не только на поверхности изделия, но и в порах поверхностного слоя бетона, происходит кристаллизация солей в порах цементного камня и его разрушение (III вид коррозии).
Существует несколько гипотез о причинах разрушения цементного камня и бетона под воздействием растворов солей при наличии испаряющей поверхности.
Одной из первых была гипотеза о разрушающем давлении при кристаллизации солей в порах цементного камня – разрушение происходит вследствие роста растягивающих напряжений в теле бетона.
Во второй гипотезе разрушение цементного камня и бетона при действии каменных солей происходит за счет увеличения объема новообразований, вследствие чего при накоплении соли в порах возникают внутренние напряжения, вызывающие образования трещин, которые способствуют проникновению агрессивной среды вглубь тела бетона. Разрушение цементного камня обусловлено так же расклинивающим действием воды при насыщении бетона растворами солей, появлением знакопеременных напряжений при чередовании насыщения и высушивания, осмотическими силами и различием коэффициентов термического расширения цементного камня и солей.
По третьей гипотезе основной причиной разрушения цементного камня и бетона, подвергаемых попеременному насыщению растворами солей и высушиванию, считается увеличение объема кристаллов солей при фазовом переходе от менее гидратированных форм к более гидратированным. Наиболее опасно высушивание бетона при температуре выше точки фазового перехода солей с последующим увлажнением его при более низкой температуре, сопровождающееся образованием кристаллогидратов, расширяющихся в объеме.
Каждая из рассмотренных гипотез не дает исчерпывающего объяснения процесса разрушения цементного камня и бетона при агрессивном воздействии растворов солей, характеризующегося сложностью происходящих при этом явлений. По-видимому, механизм коррозии обусловлен совокупностью всех указанных выше факторов.
В условиях взаимодействия солей более коррозионностойкими оказываются бетоны пористой структуры - например, аглопоритобетон по сравнению с бетонами на плотных заполнителях. В крупных порах в зернах заполнителя могут длительное время накапливаться продукты кристаллизации солей из растворов, чем обуславливается более позднее появление опасных напряжений в бетоне.
Мерами защиты цементного камня и бетона от агрессивного воздействия солей является следующие: использование бетона на пористых заполнителях; обеспечение малого водосодержания в цементном камне и бетоне; гидрофобизация бетона и использование воздухововлекающих добавок в нём; изоляция поверхности бетона путем устройства лакокрасочных, оклеечных и облицовочных покрытий; отвод агрессивных растворов солей от поверхности бетонных конструкций.
Органогенная коррозия и биоповреждения бетона
Разрушение материалов под непосредственным воздействием растительных и животных организмов, а также микроорганизмов, называется биоповреждением.
Биологические повреждения наблюдаются в гидротехнических сооружениях, а также в строительных конструкциях сооружений на различных предприятиях пищевой промышленности и др.
При технологической переработке растительных и животных организмов и в результате их жизнедеятельности образуется органическая агрессивная среда, в которой происходит разрушение материалов. Такие разрушения принято называть органогенной коррозией.
Органогенная коррозия наблюдается: в гражданских зданиях – банно-прачечных предприятиях, санузлах и др.; в сельскохозяйственных – животноводческих, птицеводческих помещениях, теплицах, силосо- и овощехранилищах и др.; на предприятиях легкой промышленности первичной переработки шерсти, кожевенных; на предприятиях деревообрабатывающий промышленности – целлюлозно-бумажных производствах, гидролизных заводах; на предприятиях микробиологических производств в биохимических производствах, цехах кормовых антибиотиков, предприятиях по производству ферментных препаратов; на предприятиях пищевой промышленности мясокомбинатах, молочных и сахарных заводов, рыбоконсервных и кондитерских производствах, винодельческих и пивоваренных предприятиях.
Органогенные агрессивные среды и живые организмы в твердых, жидких и газообразных структурах составляющих бетона вызывают различные одновременно действующие разрушительные процессы: химические, физико-химические (в т. ч. электрохимические) и физические.
Химические разрушительные процессы
К химическим разрушительным процессам, проявляющимся в основном в цементном камне, относятся растворение цементного камня и продуктов его взаимодействия с органогенными средами. Известно, что твердые структурные составляющие цементного камня растворяются в Н2О, спиртах, кислотах, альдегидах, т.е. проявляется коррозия I и II вида.
Так, например, мидии, поселяющиеся на поверхности подводных морских гидротехнических сооружений (до 40кг на 1м2) способны выделить до 12,2 см3 СО2 за 1 час на 1 кг своей массы, т.е. 488 см3 СО2 на 1м2 поверхности.
Выделяющаяся углекислота, взаимодействуя с цементным камнем, обуславливает появление углекислотной коррозии цементного камня (коррозия II вида).
В период цветения воды в озерах и реках, интенсивно развиваются растения и животные организмы. В процессе жизнедеятельности поселяющихся на поверхности сооружений живые организмы поглощают из цементного бетона углекислоту и свободную окись Са. В этом случае наблюдается I вид коррозии цементного камня. Органогенные среды, имеющие средства в болотных торфянниковых водах, способствуют также коррозии II вида вследствие превращения органического вещества в гуминовые и др. кислоты. Так, например, при содержании органических веществ в кварцевом песке до 0, 035% R при сжатии цементного бетона снижается.
В рамках старой классической иммунологии (Л.Пастер, И.Мечников) иммунология определялась как наука о невосприимчивости организма к инфекционным болезням. В настоящее время такое понимание иммунитета как части учения об инфекциях есть сужение границ предмета и искажение его сущности.
Иммунология– наука об иммунитете – изучает генетические, молекулярные и клеточные механизмы реагирования организма на чужеродные субстанции, именуемые антигенами.