Адиабатический процесс.
В этом процессе нет подвода теплоты к системе, т.е.нет теплообмена с окружающей средой
q = 0 откуда dq = 0.
Для определения связи параметров в процессе запишем уравнения первого закона термодинамики при dq =0
cvdT + pdv = 0
cpdT - vdp = 0
Разделим одно на другое

откуда

или

После интегрирования получим
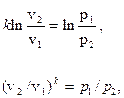
или
pvk = const.
Отсюда видно почему другое название отношения теплоемкостей k = cp/cv- показатель адиабаты. Используя уравнение состояния pv =RT можно провести круговую замену параметров и получить связь любого из параметров состояния системы
p1/ р2= (v2/v1)k
T1/T2= (p1/ р2)(k-1)/k.
Сравнивая уравнения состояния pv = cons t(изотерма) и уравнение адиабаты pvk= const, видим, что кривая адиабатического процесса идет круче.
Изменеие внутренней энергии определяется температурой и теплоемкостью
du = cvdT.
Изменение энтальпии также определяется теплоемкостью и температурой
di = cpdT.
Так как работа это интеграл

то необходимо найти зависимость давления от объема, которое определяется уравнением адиабаты
p = p1v1k/vk.
В данном случае p1,v1 это точка, относительно которой производится отсчет


(учитывая, что p1v1k = р2v2k получим)

С учетом круговой замены при помощи уравнения состояния можно вывести выражения для работы в процессе через другие параметры состояния системы

Так как в этом процессе dq = 0, то теплоемкость c = dq/dT этого процесса будет равна нулю.
По определению энтропия процесса ds = dq/T также равна нулю, т.е. этот процесс происходит при постоянной энтропии и иногда называется изоэнтропным.
В этом процессе работа происходит за счет изменения внутренней энергии системы и наоборот.