Поглощение воды растительной клеткой
Тема 1 Поглощение воды растением
Раздел 2 Водный обмен растений
Вопросы к ЛК 4
1. Какие диапазоны длин волн соответствуют окнам прозрачности атмосферы?
2. Какое рассеивание является причиной снижения контрастности снимков? Почему?
3. В каком случае возникает рассеяние Ми?
4. При каких условиях возникает неселективное рассеяние ЭМИ?
5. Какой тип отражения называют диффузным? В чем заключается его особенность?
6. Какой тип отражения называют зеркальным?
7. Что такое АЛЬБЕДО?
Какие параметры ДЗ называют зависимыми, а какие – независимыми?
1. Поглощение воды растительной клеткой
2. Поглощение воды растением
3. Зависимость поглощения воды от внешних и внутренних факторов
4. Связь водного обмена растений с водным режимом почвы
Среди всех веществ живой клетки вода занимает первое место, составляя 75 – 85 % ее массы. Исключением служат лишь клетки сухих семян и спор, обычно содержащих не более 14 % воды. Вода содержится не только в живых, но и в мертвых клетках (ксилема). В межклетниках она находится главным образом в виде пара. Нормальное функционирование клеток происходит при содержании воды равном 70 - 80 %.
Наиболее богаты водой вакуоли, которые содержат ее до 98 %, затем цитоплазма (до 85 %). В клеточных оболочках, особенно сосудов и трахеид, находится наименьшее количество воды. Здесь она заполняет промежутки между фибриллами целлюлозы и удерживается силами поверхностного натяжения и за счет адсорбционных сил. Содержание воды в хлоропластах и митохондриях существенно ниже, чем в цитоплазме, что связано с присутствием в них значительных количеств липидов.
Вода обладает рядом специфических свойств, определяющих ее громадное значение в жизни растений. Она слабо диссоциирует на водород и гидроксилъный ион. Концентрация каждого из них составляет 10-7 г-ионов на 1 л воды. Чистая вода имеет поэтому значение рН 7. Кроме обычного водорода в воде находятся дваего изотопа: дейтерий и тритий. Отношение между количеством первого и второго равно 6500: 1. Кислород также выступает в виде трех изотопов: обычного изотопа 160 и двух других с атомной массой 17 и 18 (170 и 180). Из изотопов водорода лишь тритий является радиоактивным. Образуется он обычно в атмосфере под воздействием космических лучей и имеет период полураспада 12,5 лет.
Вода имеет целый ряд особенностей, аномальных свойств по сравнению с близкими к ней по химическому составу веществами.
Одним из аномальных свойств воды является ее плотность. Известно, что все вещества при нагревании увеличивают свой объем и в связи с этим уменьшают плотность. Исключение для воды состоит в том, что в интервале температуры от 0 °С до + 4 °С плотность ее не уменьшается, а увеличивается. В момент замерзанияобъем воды мгновенно увеличивается примерно на 11 %. Лед поэтому легче жидкой воды и держится на ее поверхности, плавает. В связи с этим вода в глубоких водоемах даже при очень сильных морозах не замерзает, ибо как только температура воды упадет ниже + 4 °С. она поднимается на поверхность и превращается в лед. У самого дна озера, например, температура воды зимой обычно равна + 4 °С, что весьма благоприятно для жизни его обитателей. Но вода может оставаться в жидком состоянии при температуре вплоть до -70 °С. Это переохлажденная вода. Способность воды сохраняться в переохлажденном состоянии в тканях растений, наличие в них растворов орга-нических и минеральных веществ, способствующих сохранению жидкого состояния, предохраняет растение от гибели при трескучих зимних морозах.
Необыкновенно высоки у воды температура кипения и замерзания. По всем физическим законам вода должна бы кипеть при температуре -75°С, а не при + 100°С и замерзать при -90°С. Эти особенности объясняются наличием структуры воды.
«Исключением из правил» являются и ее необыкновенно высокие теплоемкость, поверхностное натяжение, растворяющая способность, прочность на разрыв (когезия), что также имеет неоценимое значение в жизненных процессах растений.
Для водных растений существенное значение имеет отсутствие у воды цвета. Высокая светопропускающая способность воды делает возможным осуществление растениями под водой процесса фотосинтеза.
В молекуле воды (Н2О) распределение зарядов (двух положительных и двух отрицательных) асимметрично. В связи с тем, что атомы водорода в молекуле расположены по отношению к атому кислорода под тупым углом 104,5°, молекула воды, будучи электронейтральной, имеет на одной стороне отрицательный, а на другой - положительный заряды. Такие молекулы называют диполями.
Наличие дипольного момента, равного произведению величины заряда на расстояние между полюсами, определяет ориентацию молекул воды вокруг ионов: у катионов молекулы воды располагаются к поверхности иона своими отрицательными концами - атомами кислорода, а вокруг анионов - положительными, т.е. атомами водорода.
Связывание молекул воды в электрическом поле ионов получило название электростатической гидратации. Явления электростатической гидратации наблюдаются и около ионизированных химических групп ряда органических соединений. это имеет значение в поддержании особого состояния цитоплазмы, ее устойчивости и вместе с тем - лабильности.
Гидратация - взаимодействие воды с гидрофильными (притягивающими воду) веществами, приводящее к изменению ее свойств. Различают два вида гидратации. Присоединение (притягивание) диполей воды к заряженным частицам различных ионов минеральных солей и ионизированных групп. Образование водородных связей с полярными группами органических веществ (между водородом воды и атомами кислорода или азота).
Водородные связи образуются следующим образом: кислород при образовании ковалентной связи в молекуле воды притягивает электрон водорода; такой «оголенный» водород способен притягивать соседние молекулы воды или сам притягиваться к молекулам веществ цитоплазмы. Водородные связи значительно слабее ковалентных связей (примерно в 24 раза). Наличие в молекуле воды двух протонов и двух одинаковых пар электронов обеспечивает формирование четырех водородных связей с окружающими молекулами воды с образованием особой решетчатой структуры.
Наличие решетчатой или псевдоледяной структуры и представления о мерцающих кластерах позволяют объяснить подвижность структуры жидкой воды и ее низкую вязкость.
В жизни растений важное место занимает электростатическая гuдратацuя белков. Молекулы аминокислот в белках имеют ионизированные rpуппы - карбоксильную и аминоrpуппу. Среди аминокислот, входящих в состав белков, гидрофильными радикалами обладают серин, треонин, аргинин, лизин, пролин, оксипролин, тирозин, триптофан, аспарагиновая и глутаминовая кислоты. Гидрофобные (водоотталкивающие) радикалы имеют следующие аминокислоты: аланин, валин, фенилаланин, лейцин, изолейцин. Гидрофильные радикалы (гpуппы) аминокислот находятся в водном растворе на поверхности глобул белка, а гидрофобные обращены внутрь.
Гидратация изменяет свойства воды. Поэтому в живой клетке различают свободную и связанную воду. К свободной относят воду, которая по своим свойствам не отличается от чистой воды. Среди связанной воды выделяют осмотически и коллоидно связанную. Осмотически связанная вода гидратирует молекулы и ионы, находящиеся в растворе, коллоидно связанная - коллоидные частицы. Прочно связанная вода образует первый слой гидратных оболочек.
Свободная вода легко передвигается в клетках и по всему растению, испаряется и участвует во многих метаболических процессах. Связанная вода обеспечивает устойчивость коллоидных систем. Очевидно, что коллоидно связанная вода является элементом структуры живой растительной клетки.
Биологическая роль воды в значительной степени связана с ее физико-химическими свойствами.
- Вода определяет структуру биологических макромолекул и является непременной составной частью цитоплазмы и всех органелл клеток.
- При уменьшении содержания воды в тканях растений ниже определенного оптимума, различного у разных видов, свойства высокомолекулярных веществ и жизненно важных структур клетки резко меняются, что ведет к изменению направленности и скорости биохимических реакций, а при сильном обезвоживании - к отмиранию клеток.
- Большое значение в жизнедеятельности клеток имеет гидратация клеточного содержимого.
- Высокая растворяющая способность воды необходима для поступления веществ и их передвижения по растению.
- Вода служит средой для протекания многих биохимических реакций.
- Стенки каждой живой клетки, а также стенки сосудов и трахеид смочены водой, что создает непрерывную водную фазу во всем растении.
- Вода клеточного сока, влияя на тургесцентность, определяет объем и упругость клеток и в определенной мере - форму органов растения, различные движения растения и т. д.
- Вода участвует в терморегуляции растений. Так, при потере воды листьями в процессе транспирации их температура понижается обычно на несколько градусов, благодаря чему клетки защищаются от перегрева. Значительная теплоемкость воды смягчает колебания температуры во внешней среде. Образование водородных связей при взаимодействии молекул воды друг с другом, а также с гидрофильными веществами сопровождается повышением температуры. Разрыв же этих связей приводит к понижению температуры тканей. Это способствует сохранению постоянства внутренней среды растения хотя бы на непродолжительный период времени.
- Кроме того, вода - среда для прорастания пыльцы, что имеет значение в росте пыльцевой трубки и оплодотворении растений.
- Молекулы воды включаются в многочисленные процессы метаболизма. Ярким примером служит реакция гидролиза веществ, например превращение крахмала в глюкозу. Вода может присоединяться ко многим веществам; в качестве примера можно привести присоединение воды к фумаровой кислоте с образованием яблочной.
- В процессе фотосинтеза вода служит источником водорода и электронов при ассимиляции СО2, а при дыхании синтезируется и частично снова используется. Вода принимает участие в различных электронно-транспортных процессах, миграции зарядов и т. д.
Растительная клетка как осмотическая система. Под осмосом понимается диффузия воды через полупроницаемые мембраны. Полупроницаемость мембран - это их свойство пропускать воду и не пропускать растворенные вещества. Явление осмоса было открыто в 1828 г. французским ботаником Дютроше. Позже Пфеффером были сконструированы физические приборы - осмометры (осмотические ячейки).
Осмометр представляет собой систему с тремя элементами: полупроницаемая мембрана, раствор определенной концентрации и вода. В этой системе энергия молекул чистой воды (водный потенциал) выше, чем воды в растворе. Поэтому вода будет проходить по градиенту водного потенциала из наружного сосуда во внутренний сосуд и подниматься по трубке, соединенной с внутренним сосудом. При этом будет повышаться гидростатическое давление, под которым находится раствор в осмометре. При некоторой высоте столба раствора в трубке скорости диффузии воды из наружного сосуда во внутренний и из внутреннего в наружный сравняются, и подъем жидкости в трубке прекратится. Давление, которое отвечает такому равновесию, служит количественной характеристикой процесса осмоса. Оно называется осмотическим давлением. Следовательно, осмотическое давление равно тому давлению, которое нужно приложить к раствору, чтобы привести его в равновесие с чистым растворителем, отделенным от раствора полупроницаемой мембраной.
Живая растительная клетка обладает свойствами только что разобранной осмотической системы. Поскольку молекулы воды проходят через клеточные мембраны намного быстрее, чем растворенные вещества, можно с известной долей погрешности говорить о полупроницаемости мембран. Роль полупроницаемой мембраны (хоть и не идеальной) выполняют, прежде всего, плазмалемма и тонопласт, раствора клеточный сок вакуоли клетки.
Передвижение воды через полупроницаемые мембраны подчиняется следующим законам:
1. Осмотическое давление прямо пропорционально концентрации раствора - числу частиц в единице объема независимо от размеров и природы частиц (молекул или ионов).
2. Всякое вещество, концентрация которого равна 1 моль/л, развивает осмотическое давление, равное 22,4 атм (для неэлектролита) при 0°С.
3. Осмотическое давление пропорционально абсолютной температуре Т = 273 + t °С.
4. Осмотическое давление раствора, содержащего несколько веществ, равно сумме осмотических давлений, вызываемых каждым из них.
Осмотическое давление подчиняется в общем виде закону Вант-Гоффа и выражается уравнением Р = CRTi, где Р - осмотическое давление; С - молярная концентрация раствора; R - газовая постоянная, равная 0,0821 л · атм / град. моль; Т - абсолютная температура; i - изотонический коэффициент, показывающий отношение числа частиц (молекул и ионов) в растворе к исходному числу молекул растворенного вещества. Для растворов неэлектролитов, например для сахара, изотонический коэффициент равен 1, для электролитов - больше 1.
Если клетку поместить в воду, то она, как и осмометр, будет поглощать ее и тем сильнее, чем выше концентрация клеточного сока. Но до каких пор клетка будет поглощать воду? При всасывании клеткой воды объем клеточного сока увеличивается, и цитоплазма начинает давить на оболочку клетки, растягивая ее. Оболочка, обладая значительной прочностью и вместе с тем эластичностью, в свою очередь оказывает сопротивление всякой силе, стремящейся ее растянуть, и тем большее, чем более она растянута. После прекращения действия растягивающей силы стенка снова возвращается к своим прежним размерам. Напряженное состояние клеточной стенки, вызванное давлением клеточного содержимого, носит название тургора, а противодавление оболочки на протопласт - тургорного давления.
По мере поступления воды в клетку эндосмос постепенно уменьшается в силу противодавления клеточной стенки. В какой-то момент внутренние и внешние силы диффузии становятся равными. Это состояние называется полным насыщением клетки водой. В данном случае клетка находится в равновесии с водой, осмотическое давление клеточного сока уравновешено тургорным давлением: Р = Т. Иначе можно это записать так: Р - Т = 0. В этом состоянии вода не входит в клетку и не выходит из нее, как бы высоко ни было ее осмотическое давление Р. Примером этого могут служить клетки водорослей и водных высших растений. Их клетки всегда находятся в состоянии почти полного насыщения.
Клетки наземных растений, наоборот, почти никогда не бывают полностью насыщенными водой. Благодаря потере воды листьями в процессе транспирации они обычно не достигают состояния полного тургора. Часть осмотического давления Р остается неуравновешенной тургорным давлением Т, и эта часть осмотического давления способна при погружении такой клетки в воду вызывать приток воды в клетку и некоторое увеличение размеров последней. В данном случае Р будет больше Т: Р = T+S или S = Р - Т. Эта дополнительная часть осмотического давления получила название сосущей силы S . Название не совсем удачное, ибо это не сила, а давление, как и Р и Т, разность между которыми она представляет. Следует подчеркнуть, что именно сосущая сила клетки, а не осмотическое давление клеточного сока определяет поглощение воды клеткой.
По отношению к концентрации клеточного сока внешние растворы могут быть: гипертоническими, осмотическое давление которых больше осмотического давления клеточного сока; изотоническими, осмотическое давление которых равно осмотическому давлению клеточного сока; гипотоническими, у которых это давление меньше, чем давление клеточного сока.
При помещении живой растительной клетки не в воду, а в гипертонический раствор тургор будет стремиться к нулю, а сосущая сила - к величине полного осмотического давления S = Р. В данном случае будут происходить следующие явления: раствор оттянет воду из клетки, клеточная стенка сократится, сократится и цитоплазма клетки, тургор исчезнет. Раствор начнет входить в пространство между стенкой и цитоплазмой, т. е. цитоплазма будет отходить от клеточной стенки. Это отставание цитоплазмы от оболочки клетки при погружении последней в гипертонический раствор называется плазмолизом. Плазмолиз свидетельствует о том,что имеются различия в проницаемости клеточной стенки и цитоплазмы, и, что самое главное, показывает, что цитоплазма жива.
Если плазмолизированную клетку снова поместить в воду, то происходит обратная картина: клетка всасывает воду, объем протопласта увеличивается; цитоплазма начинает плотно примыкать к стенке клетки. Переход плазмолизированной клетки в нормальное состояние носит название деплазмолиза.
Различают уголковый, вогнутый (судорожный) и выпуклый виды плазмолиза. При уголковом плазмолизе цитоплазма отстает только по уголкам клетки. При вогнутом плазмолизе цитоплазма становится угловатой, сохраняет в виде выступов те участки, которые более плотно связаны с клеточной стенкой. Длительный вогнутый плазмолиз можно получить, предварительно обработав клетки солями двухвалентных металлов, например кальция. Выпуклый плазмолиз быстро проявляется при низкой вязкости цитоплазмы, например, при воздействии одновалентных металлов. В этом случае разбухшая цитоплазма в виде колпачка прикрывает сократившийся тонопласт.
В природной обстановке, например при пересадке растений на засоленную почву, осмотическое давление почвенного раствора может быть выше, чем осмотическое давление клеточного сока. В этом случае не только будет поглощаться такими клетками, но, наоборот, будет выходить из клеток, вызывая обезвоживание последних, а затем и отмирание растения.
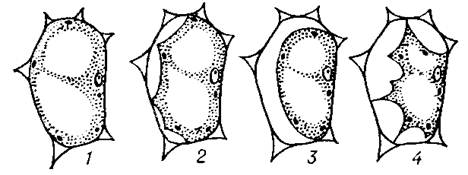
Основные формы плазмолиза (схема): 1- начальная стадия; 2 - вогнутый; 3 - выпуклый (время перехода от вогнутого плазмолиза к выпуклому служит показателем вязкости цитоплазмы); 4 - судорожный (при быстром действии концентрированного плазмолитика и высокой степени вязкости цитоплазмы).
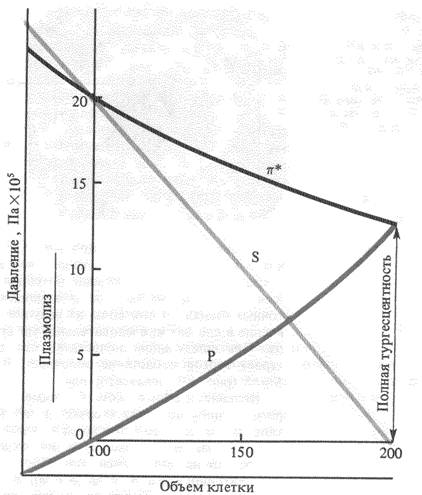
Если потеря тургора происходит не в растворе, как при плазмолизе, а от высыхания в воздухе в жаркие дни, то наблюдается явление циторриза.Цитоплазма при этом от клеточной стенки не отстает, а остается как бы припаянной к ней. Стенки клеток, выпячиваясь внутрь, деформируются, стремятся разорвать цитоплазму с определенной силой (силой циторриза). В данном случае тургор - величина отрицательная, а сосущая сила равна сумме осмотического и тургорного давлений: S = Р - (-Т) = Р + Т. Сила циторриза может достигать величины порядка 12-15 атм. Зависимость всех трех рассматриваемых величин от степени насыщения клетки водой показана на схеме.
Внешние условия существенно влияют на показатели осмотического давления и сосущей силы. Они очень низкие у водных растений (за исключением растений морей и других засоленных водоемов) и растений болот и высокие - у растений засушливых мест. У морских водорослей осмотическое давление достигает 25 - 30 атм. Клетки растений, произрастающих на засоленных почвах, развивают давление, измеряемое 100-150 атм. Растения открытых местообитаний отличаются более высокими величинами осмотического давления и сосущей силы, чем растения затененных мест.
Камбиальные клетки стволов древесных растений имеют осмотическое давление 20 - 30 атм. Паренхимные клетки содержат клеточный сок в концентрациях, соответствующих осмотическому давлению 4 - 5 атм. Сосущая сила клеток хвои ели в таежной зоне достигает 15 - 35 атм, а поглощающих корней колеблется от 6 до 8 атм (у сосны - от 6 до 11 атм).
Для определения осмотического давления используют плазмолитический и криоскопический методы. Плазмолитический метод основан на том, что в растворах плазмолитиков (веществ, вызывающих плазмолиз) разной концентрации начало уголкового плазмолиза клеток будет наблюдаться в том из них, осмотическое давление которого почти соответствует осмотическому давлению клеточного сока (изотонический раствор). Криоскопический метод основан на определении температуры замерзания отжатого клеточного сока.
Сосущую силу можно определить, основываясь: на измерении размеров ткани, помещенной в растворы различных концентраций (метод Уршпрунга); на измерении концентрации растворов, в которые помещены кусочки ткани с помощью рефрактометра (метод Н.А. Максимова и Н.с. Петинова) или по методу струек В.С. Шардакова. Размеры клеток и концентрация внешнего раствора не изменятся при помещении в него ткани в том случае, когда сосущие силы раствора и клеток совпадают.
Осмотические свойства клеток не только определяют поглощение воды растением, но и лежат в основе многих физиологических процессов, определяют различные виды движений у растений, в частности движения устьиц. От осмотических явлений в значительной мере зависит рост клеток. Упругое состояние тканей и органов растения (их тургесцентность) влияет на внешний вид и форму растения. Большая роль принадлежит осмотическим явлениям в передвижении воды и растворенных веществ, устойчивости растений к неблагоприятным внешним воздействиям, регулировании такого сложного процесса, как фотосинтез.
Термодинамические основы водного обмена.Введение в физиологию растений понятий термодинамики дало возможность математически описать и объяснить причины, вызывающие как водообмен клеток, так и транспорт воды в системе почва - растение - атмосфера. Важнейшим термодинамическим показателем состояния воды в системе является водный потенциал. Это производная величина от двух других термодинамических показателей - активности и химического потенциала воды.
Активность воды (аw). Характеризует ту эффективную (реальную) концентрацию, соответственно которой вода участвует в различных процессах. Всякие межмолекулярные и иные взаимодействия, уменьшающие подвижность и рассеиваемость молекул (прежде всего гидратация), снижают активность воды. Активность чистой воды равна единице. В растворе и в клетке активность воды всегда меньше единицы.
Химический потенциал воды (μw). Величина, производная от активности. Она выражает максимальное количество внутренней энергии молекул воды, которое может быть превращено в работу, имеет размерность Дж-моль-1 и рассчитывается по уравнению
μw = μw0 + RTlnaw,
где μw0, - химический потенциал чистой воды (принят равным нулю); R - газовая постоянная; Т- абсолютная температура; аw - активность воды в системе.
Водный потенциал (ψ). Выражает способность воды в данной системе совершить работу по сравнению с той работой, которую при тех же условиях совершила бы чистая вода. Рассчитывается по уравнению
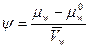
где μw и μw0 — химические потенциалы воды в системе и чистой воды; 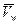 - парциальный мольный объем воды (для чистой воды и разбавленных растворов принимают равным 18 см3 -моль-1).
- парциальный мольный объем воды (для чистой воды и разбавленных растворов принимают равным 18 см3 -моль-1).
Водный потенциал, являясь фактически мерой активности воды, определяет термодинамически возможное направление ее транспорта. Молекулы воды всегда перемещаются от более высокого водного потенциала к более низкому, подобно тому как вода течет вниз, переходя на все более низкий энергетический уровень. Когда система находится в равновесии с чистой водой, ψ=0. В почве, растении, атмосфере активность воды и способность совершать работу ниже, чем у чистой воды, поэтому у обычно отрицателен. Водный потенциал имеет размерность энергии, деленной на объем, что позволяет выражать его в атмосферах, барах или паскалях (1 атм = 1,013 бар = 105 Па; 103 Па = 1 кПа, 106 Па = 1 МПа).
Водный потенциал растения является алгебраической суммой следующих четырех составляющих:
ψ=ψπ+ψm+ψp+ψg
где ψπ - осмотический, ψm - матричный, ψp - гидростатический, ψg - гравитационный потенциалы.
Соотношение между ними и вклад в водный потенциал сильно различаются в зависимости от объекта и окружающих условий.
Гравитационный потенциал (ψg). Отражает влияние на активность воды силы тяжести и заметно сказывается только при поднятии воды на относительно большую высоту. Он составляет примерно 0,01 МПа-м-1, т.е. при перемещении воды вертикально вверх на 10 м гравитационный вклад в водный потенциал составляет 0,1МПа. Это незначительная величина для сельскохозяйственных растений, в том числе и плодовых культур, поэтому обычно она не учитывается.
Осмотический потенциал (ψπ). Компонент водного потенциала характеризующий снижение активности воды частицами растворенного вещества. Поэтому осмотический потенциал всегда является величиной отрицательной:
ψπ= -RTci,
где R - газовая постоянная; Т - абсолютная температура; с - концентрация раствора в молях; i - изотонический коэффициент, равный 1+α(n-1), где α - степень электролитической диссоциации; п - количество ионов, на которое распадается молекула электролита.
Для веществ, не диссоциирующих на ионы, α=0 и n=1. Степень диссоциации электролита, как известно, зависит от концентрации раствора, физиологическое значение имеют 0,1- 0,5 М растворы солей, для которых i составляет 0,7-0,8.
С увеличением количества частиц растворенного вещества как за счет повышения концентрации раствора, так и за счет диссоциации веществ уменьшается активность воды и снижается осмотический потенциал. При температуре 20 °С величина RT равна 2,44 МПа. Для 1 М раствора любого недиссоциирующего вещества осмотический потенциал равен -2,44 МПа, для 0,5 и 2 М растворов соответственно -1,22 и -4,88 МПа. Диссоциация растворенных веществ на ионы усиливает депрессию осмотического потенциала. Осмотический потенциал 0,5 М раствора КNО3 составляет -2,1 МПа (i=1,7), для 0,5 М раствора Са(NО3)2 он равен -2,9 МПа (i=2,4).
Когда раствор отделен от воды полупроницаемой мембраной, которая пропускает только растворитель и непроницаема для растворенных веществ, возникает односторонний ток воды по градиенту ее активности в направлении раствора. Этот процесс называется осмосом, а дополнительное давление, которое должно быть приложено к раствору, чтобы воспрепятствовать одностороннему току воды – осмотическим давлением (π).
Таким образом, осмотический потенциал раствора, отделенного полупроницаемой мембраной от чистого растворителя, реализуется в равном по величине и обратном по знаку осмотическом давлении. Растворы с одинаковым давлением называются изотоническими, между ними нет направленного водообмена. Раствор, имеющий большее осмотическое давление, называется гипертоническим, меньшее - гипотоническим. При разделении полупроницаемой мембраной транспорт воды идет по направлению к гипертоническому раствору.
Клетка, а также все органеллы, окруженные мембранами (хлоропласты, митохондрии и др.), представляют собой осмотические системы. Поскольку мембраны обладают избирательной проницаемостью, и вода проходит через них значительно легче, чем растворенные вещества, допускают, что мембраны полупроницаемы, т.е. проницаемы только для воды. Всю цитоплазму обычно рассматривают как единый полупроницаемый барьер.
В зрелых растительных клетках главным «осмотическим пространством» является вакуоль. Именно клеточный сок, содержащий растворенные в воде различные соли, сахара, органические кислоты, аминокислоты и другие соединения, представляет собой осмотический актив клетки. Суммарная концентрация растворенных веществ в клеточном соке варьирует от 0,2 до 0,8М. Осмотический потенциал клеточного сока измеряется сотнями и достигает тысяч кПа.
Растительные клетки отличаются от идеальных осмотических систем тем, что мембраны в некоторой степени проницаемы и для растворенных веществ. Это снижает осмотический градиент и возможность поступления воды. Отличие от идеального поведения можно выразить с помощью коэффициента селективности, или отражения (σ). В случае абсолютной селективности растворенное вещество «отражается» от мембраны, т.е. совершенно не проникает через нее (σ=1). Если мембрана в одинаковой степени проницаема и для воды, и для растворенного вещества, становится равным 0, осмотического поступления воды нет. Коэффициент отражения зависит от свойств мембран и природы веществ. Так, для корней кукурузы получены следующие значения σ: этанол 0,27, маннитол 0,74, сахароза 0,54, полиэтиленгликоль 0,82, NaCI 0,64, KNO3 0,6, которые фактически характеризуют эффективность мембранного барьера в поддержании осмотического градиента. В качестве осмотически активных веществ при определении термодинамических параметров растительных тканей необходимо использовать соединения со значением о, близким к 1, например полиэтиленгликоль.
Матричный потенциал (ψm). Характеризует снижение активности воды за счет гидратации коллоидных веществ и адсорбции на границе раздела фаз. Матричное связывание воды сопровождается увеличением объема и называется набуханием. В протоплазме преобладает набухание за счет гидратации белков, нуклеиновых кислот, углеводов; в клеточной стенке наблюдаются капиллярный эффект (вода между микрофибриллами и в межмицеллярных пространствах) и гидратация полисахаридов, среди которых по способности к набуханию выделяются пектиновые вещества, содержащие диссоциированные карбоксильные группы.
Состояние набухания протоплазмы имеет решающее значение для интенсивности и направленности обмена веществ. В некоторых частях растений поглощение воды происходит исключительно путем набухания, например у семян, меристематических тканей, клетки которых еще не вакуолизированы. При набухании семян может развиваться давление, измеряемое десятками МПа. Особенно сильной способностью к набуханию отличаются семена бобовых культур с высоким содержанием белков.
Между осмосом и набуханием существует аналогия. Осмотическое и матричное связывание снижает активность воды; поэтому ψπ и ψm всегда меньше нуля. Чем более отрицательное значение они имеют, тем выше способность клеток и тканей поглощать воду. Осмотическому давлению π соответствует давление набухания τ. Сухое набухающее тело обладает потенциальным давлением набухания, которое так же, как и потенциальное осмотическое давление, характеризует максимальную способность поглощать воду.
Гидростатический потенциал, или потенциал давления (ψр). Компонент водного потенциала, обусловленный внутриклеточным давлением. При погружении растительной ткани, имеющей зрелые сильно вакуолизированные клетки, в гипотонический раствор наблюдается эндоосмос. При отсутствии противодавления клеточной стенки поступление воды в клетку определяется ее водным потенциалом (ψ), в начальный момент времени равным осмотическому потенциалу (ψπ) раствора, заполняющего вакуоль, вклад матричных сил очень незначительный, и им можно пренебречь. Однако по мере поступления воды в вакуоль ее объем увеличивается, цитоплазма прижимается к клеточной стенке и возникает тургорное давление, а вместе с ним и равное ему по величине противодавление стенки на клеточное содержимое.
Таким образом, осмотическое поглощение воды ведет к созданию гидростатического давления. Под давлением активность воды возрастает, поэтому гидростатический потенциал имеет положительное значение. При полном насыщении клетки водой (достижении максимального тургора) положительный потенциал Давления полностью уравновешивает отрицательный осмотический потенциал и клетка перестает поглощать воду. В таком стоянии ее водный потенциал равен нулю.
В любой момент времени водный потенциал вакуолизированной клетки определяется соотношением осмотического потенциала и потенциала давления: ψ = ψπ + ψр. При завядании растений гидростатическое давление равно нулю,
ψ = ψ р.
Восстановление тургесцентности сопровождается возникновением и возрастанием гидростатического давления. Водный потенциал имеет отрицательную величину, когда осмотический потенциал еще не полностью реализован в гидростатическом давлении и клетка способна поглощать воду. Водный потенциал равен нулю, когда потенциал давления полностью компенсирует осмотические силы. Величина будет положительной, если гидростатическое давление превосходит эти силы. Такая ситуация наблюдается в клетках, прилегающих к сосудам ксилемы и подающих туда воду.
Необходимо также обратить внимание на то, что в соседних клетках соотношения осмотического и гидростатического потенциалов могут быть разными. У клеток с более низким осмотическим потенциалом возможен более высокий потенциал давления в результате большей насыщенности водой. Поэтому ее водный потенциал окажется выше, чем в соседней клетке, и транспорт воды осуществляется против осмотического градиента. Этим растительные клетки существенно отличаются от классического осмометра, где в результате неограниченного увеличения объема нет гидростатического потенциала и поступление воды идет только по осмотическому градиенту.
В клетках, которые поглощают воду в основном за счет матричных сил, также возникает гидростатическое давление. Протоплазма не может достичь состояния максимального набухания, так как гидростатическое давление, которое проявляется вследствие обусловленного набуханием притока воды, противодействует этому. Способность таких клеток поглощать воду зависит от соотношения матричных сил и потенциала давления:
ψ=ψm+ψp
Таким образом, осмотический и матричный потенциалы определяют максимальную поглотительную способность, реальная же возможность поглощать воду в данный момент характеризуется водным потенциалом, составляющим которого является гидростатический потенциал, зависящий от степени насыщенности клеток водой.