Физические типы кристаллических решеток
Классификация кристаллов
Кристаллическая решетка может обладать различными видами симметрии. Под симметрией кристаллической решетки понимается свойство решетки совпадать с самой собой при некоторых пространственных перемещениях.

Всякая решетка прежде всего обладает трансляционной симметрией, т. е. совпадает сама с собой при перемещении (трансляции) на величину периода идентичности[1]. Из других видов симметрии отметим симметрию по отношению к поворотам вокруг некоторых осей, а также к зеркальному отражению относительно определенных плоскостей.
Если решетка совпадает сама с собой при повороте вокруг некоторой оси на угол 2л/n (следовательно, за один полный поворот вокруг оси решетка совпадает сама с собой п раз), то эта ось называется осью симметрии n-го порядка. Можно показать что, кроме тривиальной оси 1-го порядка, возможны только оси симметрии 2-го, 3-го, 4-го и 6-го порядков. Примеры структур, обладающих такими осями симметрии, показаны схематически на рис. 111.1 (белыми кружками, черными кружками и крестиками обозначены атомы разных сортов).
Плоскости, при зеркальном отражении от которых решетка совпадает сама с собой, называются плоскостями симметрии. Пример плоскости симметрии также дан на рис. 111.1.
Различные виды симметрии называются элементами симметрии кристаллической решетки. Кроме осей и плоскостей, возможны другие элементы симметрии, в рассмотрение которых мы, однако, входить не станем.
Кристаллическая решетка, как правило, обладает одновременно несколькими видами симметрии. Однако не всякое сочетание элементов симметрии оказывается возможным. Как показал выдающийся русский ученый Е. С. Федоров, возможны 230 комбинаций элементов симметрии, получившие название пространственных групп. Эти 230 пространственных групп разбиваются по признакам симметрии на 32 класса. Наконец, по форме элементарной ячейки все кристаллы делятся на семь кристаллографических систем (или сингоний), каждая из которых включает в себя несколько классов симметрии.
 В порядке возрастающей симметрии кристаллографические системы располагаются следующим образом.
В порядке возрастающей симметрии кристаллографические системы располагаются следующим образом.
1. Триклинная система. Для нее характерно, что 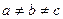 ;
;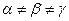 . Элементарная ячейка имеет форму косоугольного параллелепипеда.
. Элементарная ячейка имеет форму косоугольного параллелепипеда.
2. Моноклинная система. Два угла — прямые, третий (в качестве которого принято выбирать угол b) отличен от прямого. Следовательно, 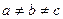 ;
; 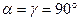 ;
; 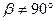 . Элементарная ячейка имеет форму прямой призмы, в основании которой лежит параллелограмм (т. е. форму прямого параллелепипеда).
. Элементарная ячейка имеет форму прямой призмы, в основании которой лежит параллелограмм (т. е. форму прямого параллелепипеда).
3. Ромбическая система. Все углы — прямые, все ребра — разные: 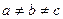 ;
; 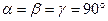 . Элементарная ячейка имеет форму прямоугольного параллелепипеда.
. Элементарная ячейка имеет форму прямоугольного параллелепипеда.
4. Тетрагональная система. Все углы — прямые, два ребра — одинаковые: 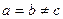 ;
; 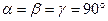 . Элементарная ячейка имеет форму прямой призмы с квадратным основанием.
. Элементарная ячейка имеет форму прямой призмы с квадратным основанием.
5. Ромбоэдрическая (или тригональная) система. Все ребра — одинаковые, все углы также одинаковые и отличные от прямого: 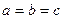 ;
;  . Элементарная ячейка имеет форму куба, деформированного сжатием или растяжением вдоль диагонали.
. Элементарная ячейка имеет форму куба, деформированного сжатием или растяжением вдоль диагонали.
6. Гексагональная система. Ребра и углы между ними удовлетворяют условиям: 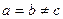 ;
;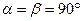 ,
, . Если составить вместе три элементарные ячейки так, как показано на рис. 111.2, то получается правильная шестигранная призма.
. Если составить вместе три элементарные ячейки так, как показано на рис. 111.2, то получается правильная шестигранная призма.
7. Кубическая система. Все ребра — одинаковые, все углы — прямые: a=b=c;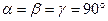 . Элементарная ячейка имеет форму куба.
. Элементарная ячейка имеет форму куба.
В зависимости от природы частиц, помещающихся в узлах кристаллической решетки, и от характера сил взаимодействия между частицами различают четыре типа кристаллических решеток и соответственно четыре типа кристаллов: ионные, атомные, металлические и молекулярные.
 1. Ионные кристаллы. В узлах кристаллической решетки помещаются ионы разных знаков. Силы взаимодействия между ними являются в основном электростатическими (кулоновскими). Связь, обусловленная электростатическими силами притяжения между разноименно заряженными ионами, называется гетерополярной (или ионной).
1. Ионные кристаллы. В узлах кристаллической решетки помещаются ионы разных знаков. Силы взаимодействия между ними являются в основном электростатическими (кулоновскими). Связь, обусловленная электростатическими силами притяжения между разноименно заряженными ионами, называется гетерополярной (или ионной).
Типичным примером ионной решетки может служить изображенная на рис. 112.1 решетка каменной соли (NaCl). Эта решетка принадлежит к кубической системе. Белыми кружками изображены несущие положительный заряд ионы натрия, черными кружками — отрицательные ионы хлора. Как видно из рисунка, ближайшими соседями иона данного знака будут ионы противоположного знака. В газообразном состоянии NaCl состоит из молекул, в которых объединяются попарно ионы натрия с ионами хлора. Образующая молекулу группировка из иона Na и иона Сl утрачивает в кристалле обособленное существование. Ионный кристалл состоит не из молекул, а из ионов. Весь кристалл в целом можно рассматривать как одну гигантскую молекулу.
2. Атомные кристаллы. В узлах кристаллической решетки помещаются нейтральные атомы. Связь, объединяющая в кристалле (а также и в молекуле) нейтральные атомы, называется гомеополярной (или ковалентной). Силы взаимодействия при гомеополярной связи имеют также электрический (но не кулоновский) характер. Объяснение этих сил может быть дано только на основе квантовой механики.
Гомеополярная связь осуществляется электронными парами. Это означает, что в обеспечении связи между двумя атомами участвует по одному электрону от каждого атома. По этой причине гомеополярная связь имеет направленный характер. При гетерополярной связи каждый ион воздействует на все достаточно близкие к нему ионы. При гомеополярной связи воздействие направлено на тот атом, с которым у данного атома имеется совместная электронная пара. Гомеополярная связь может осуществляться только валентными, т. е. наименее связанными с атомом, электронами. Поскольку каждый электрон может обеспечить связь только с одним атомом, число связей, в которых может участвовать данный атом (число соседей, с которыми он может быть связан), равно его валентности.
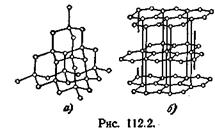 Типичными примерами атомных кристаллов могут служить алмаз и графит. Оба эти вещества тождественны по химической природе (они построены из атомов углерода), но отличаются кристаллическим строением. На рис. 112.2, а показана решетка алмаза, на рис. 112.2, б — решетка графита. На этом примере отчетливо видно влияние кристаллической структуры на свойства вещества.
Типичными примерами атомных кристаллов могут служить алмаз и графит. Оба эти вещества тождественны по химической природе (они построены из атомов углерода), но отличаются кристаллическим строением. На рис. 112.2, а показана решетка алмаза, на рис. 112.2, б — решетка графита. На этом примере отчетливо видно влияние кристаллической структуры на свойства вещества.
Такую же решетку, как у алмаза (решетку типа алмаза), имеют типичные полупроводники — германий (Ge) и кремний (Si). Для этой решетки характерно то, что каждый атом окружен четырьмя равноотстоящими от него соседями, расположенными в вершинах правильного тетраэдра. Каждый из четырех валентных электронов входит в электронную пару, связывающую данный атом с одним из соседей.
3. Металлические кристаллы. Во всех узлах кристаллической решетки расположены положительные ионы металла. Между ними беспорядочно, подобно молекулам газа, движутся электроны, отщепившиеся от атомов при образовании ионов. Эти электроны играют роль «цемента», удерживая вместе положительные ионы; в противном случае решетка распалась бы под действием сил отталкивания между ионами. Вместе с тем и электроны удерживаются ионами в пределах кристаллической решетки и не могут ее покинуть.
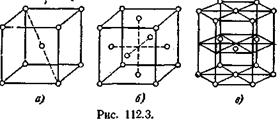
Большинство металлов имеет решетки одного из трех типов: кубическую объемно-центрированную (рис. 112.3, а), кубическую гранецентрированную (рис. 112.3, б) и так называемую плотную гексагональную (рис. 112.3, в). Последняя представляет собой гексагональную решетку с отношением с/а, равным 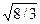 . Кубическая гранецентрированная и плотная гексагональная решетки соответствуют наиболее плотной упаковке одинаковых шаров.
. Кубическая гранецентрированная и плотная гексагональная решетки соответствуют наиболее плотной упаковке одинаковых шаров.
4. Молекулярные кристаллы. В узлах кристаллической решетки помещаются определенным образом ориентированные молекулы. Силы связи между молекулами в кристалле имеют ту же природу, что и силы притяжения между молекулами, приводящие к отклонению газов от идеальности. По этой причине их называют ван-дер-ваальсовскими силами. Молекулярные решетки образуют, например, следующие вещества: Н2, N2, О2, СО2, Н2О. Таким образом, обычный лед, а также так называемый сухой лед (твердая углекислота) представляют собой молекулярные кристаллы.