Адсорбция на твердых (неподвижных) поверхностях
A-лактоза
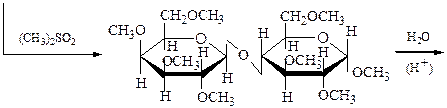
октаметиллактоза
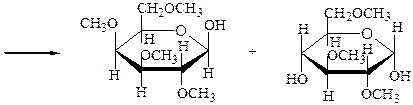
2,3,4,6-тетра-О-метил-b,D- 2,3,6-три-О-метил-a,D-
-галактопираноза -глюкопираноза
Под адсорбцией на твердых поверхностях подразумевается поглощение газов и компонентов жидких растворов на этих поверхностях.
Явление поглощения газов на границе твердое тело – газ (адсорбция газов твердыми телами) было открыто в конце XVIII в. независимо шведским химиком и фармацевтом К. Шееле (1773) и итальянским проф. Ф. Фонтана (1777). Фонтана обнаружил, что свежепрокаленный древесный уголь обладает способностью поглощать различные газы в объемах, значительно превосходящих его собственный объем. К. Шееле установил, что в ряде случаев этот процесс обратим: при изменении условий поглощенный газ может выделяться. Адсорбцию из растворов случайно открыл фармацевт Т. Ловиц (1785). Термин адсорбция ввел Г. Кайзер в 1881 г.
У адсорбции на твердых поверхностях совсем иная область применения, чем у адсорбции на подвижных поверхностях. Там главное значение имеет снижение поверхностного натяжения. С помощью адсорбции на твердой поверхности производится очистка газов и растворов, разделение и анализ смесей (хроматография), изучение пористой структуры материалов.
Твердое вещество, на поверхности которого идет адсорбция, называется адсорбент. Вещество, которое адсорбируется на твердой поверхности, называется адсорбат.
Адсорбент должен иметь большую удельную поверхность, без чего не возможно его эффективное действие. Это материалы, состоящие из мелких частиц (силикагель, каолин), или пористые и пронизанные трещинами материалы (уголь, активированный уголь). Активированный уголь марки БАУ – расшифровывается как березовый активированный уголь.
Принципиально важные для адсорбции особенности твердых поверхностей – это их шероховатость, наличие трещин, пор, царапин. Идеально гладкие твердые поверхности это редкость, и в процессах адсорбции они не применяются. Непосредственно измерить истинную площадь твердой поверхности невозможно, и для ее определения применяются сложные методы, основанные на все той же адсорбции. Наблюдаемые неровности – микродефекты превышают атомные размеры в десятки и сотни раз (десятки нанометров). Наличие таких микродефектов обусловливает некоторый избыточный запас поверхностной энергии Гиббса системы.
Адсорбция а на твердой поверхности выражается не количеством адсорбированного вещества на единицу площади, а количеством вещества на единицу массы адсорбента:
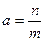
Адсорбция обусловлена силами, действующими на поверхности адсорбента. Эти силы имеют ту же природу, что и силы молекулярного притяжения (ван-дер-ваальсовы силы), обусловливающие, например, конденсацию пара в жидкость.
Силовое поле частиц адсорбента, расположенных на его поверхности, компенсированы частично. Поэтому на поверхности адсорбента действуют остаточные силы, способные притягивать молекулы веществ, находящихся в контакте с поверхностью адсорбента. В энергетическом отношении участки поверхности твердого тела неравноценны. Адсорбция в первую очередь происходит на участках поверхности с наибольшим локальным запасом поверхностной энергии Гиббса.
В зависимости от характера действующих сил различают физическуюи химическуюадсорбцию. Для физической адсорбции характерны небольшая теплота ( ∆H от –4 до –40 кДж/моль) и обратимость процесса. Адсорбция газов твердыми телами протекает с большой скоростью, поэтому адсорбционное равновесие устанавливается практически мгновенно:
А X АХ
 Адсорбент + Адсорбат Адсорбционный комплекс.
Адсорбент + Адсорбат Адсорбционный комплекс.
Теплоты химической адсорбции находятся в пределах от –40 до –400 кДж/моль и по своему характеру процесс является необратимым.
При взаимодействии газа с адсорбентом наряду с адсорбцией, представляющей собой типично поверхностный процесс, может происходить поглощение газа или пара всем объемом твердого тела, а также их конденсация в узких порах (капиллярная конденсация).
В реальных условиях эти процессы протекают совместно. Разделить или идентифицировать их в большинстве случаев трудно. Поэтому для характеристики взаимодействия адсорбента с адсорбтивом применяется более общий термин – сорбция. Под сорбцией понимаются все виды поглощения вещества на адсорбенте.
Особенности адсорбции на твердых поверхностях (теории И. Ленгмюра и М. Поляни):
1. Адсорбция происходит на активных центрах поверхности

Рис. 1. Поглощенные частицы на активных центрах
2. Процесс адсорбции динамический. Одновременно происходит десорбция.
3. Радиус действия адсорбционных (межмолекулярных) сил мал.