Две теории саморастворения кремния
План
Химическое травление кремния. Кинетика травления кремния
Лекция 2 .
Основы технологии электронной компонентной базы
Модуль 2
Лекции 2-3. Физико-химические методы обработки поверхности
1. Химическое травление кремния
2. Кинетика травления кремния
3. Две теории саморастворения кремния
4. Зависимость скорости травления от свойств
используемых материалов
5. Химико-динамическая полировка
6. Промывка пластин в воде
Процесс травления состоит из нескольких этапов: реагент должен приблизиться к поверхности пластины, адсорбироваться на ней, вступить с кремнием в химическое взаимодействие. Образовавшимся продуктам реакции необходимо в свою очередь десорбироваться с поверхности, а затем удалиться в объем раствора.
Время травления является суммой времен протекания каждого из этих этапов. Причем если какой-либо этап оказывается наиболее длительным, то он будет определять (лимитировать) весь процесс травления. В начальный момент времени концентрация травителя во всем объеме одинакова. Однако по истечении некоторого времени та часть раствора, которая находится вблизи поверхности кремния, вступает с ним во взаимодействие. Концентрация молекул травителя у поверхности кремния из-за протекания химической реакции уменьшается, так что образуется слой, обедненный молекулами травителя с концентрацией C¢. Для дальнейшего протекания реакции необходимо, чтобы из объема травителя, где его концентрация С, молекулы травителя подошли к поверхности кремния. Доставка молекул из объема травителя к поверхности пластины - диффузионный процесс, скорость которого равна
vд = kд(C – C¢),
где kд - коэффициент диффузии молекул травителя.
В первый момент, когда концентрация травителя везде одинакова, скорость травления кремния максимальна и равна
vр = kр C exp (–E/kТ),
где kр - константа скорости химической реакции; E - энергия активации процесса травления; k - постоянная Больцмана; T - температура. Очевидно, что скорость химической реакции существенно зависит от энергии активации и температуры. Если поверхность полупроводника энергетически неоднородна, например имеются выходы дислокаций или другие дефекты, то в таких местах энергия активации может быть значительно меньше, скорость травления выше, травление становится селективным.
Через некоторый промежуток времени диффузия реагента к
поверхности и скорость химической реакции становятся одинаковыми:
kд(C – C¢) = kр C exp(–E/kТ).
Тогда скорость травления можно определить следующим образом:
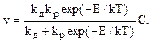
Характер травления кремния зависит от того, какая из стадий травления является самой медленной: диффузия реагента к поверхности или химическая реакция. Скорости каждой из этих стадий определяются величинами единичных скоростей диффузии kд или химической реакции kрexp(–E/kT).
Если kд>>kрexp(–E/kT), то
v = kрC exp(–E/kT). (1.1)
Скорость травления определяется скоростью химической реакции и зависит от энергии активации травления. Следовательно, травление будет селективным, как в первый момент. Такой процесс используется для выявления структурных дефекерхности полупроводника, кристаллографической ориентации поверхности.
Если kд << kр exp(–E/kT), то
v @ kдC.
Скорость травления в этом случае мало зависит от энергии активации и определяется лишь диффузионными процессами. Травление будет полирующим. Полировка происходит следующим образом. Если на поверхности пластины имеется рельеф, то после образования у поверхности обедненного травителем слоя оказы-вается, что толщина последнего около выступов несколько меньше (рис.1.4), чем его средняя толщина, поэтому к выступам реагент подходит быстрее и происходит их сглаживание.
Кремний является довольно инертным материалом, что объясняется наличием окисной пленки на его поверхности. Поэтому в состав травителя для кремния вводят плавиковую кислоту, растворяющую окисел. Для объяснения саморастворения кремния существуют две теории: химическая и электрохимическая.
Простейшее объяснение процесса травления дает химическая теория: травитель должен содержать два компонента - окислитель, которым обычно является азотная кислота, и растворитель окисла, которым служит плавиковая кислота. Эта теория оказалась очень успешной для подбора основных составов травителей и объяснения эффекта полировки, однако с ее помощью нельзя объяснить процесс селективного травления.
Электрохимическая теория предполагает, что поверхность полупроводника является энергетически неоднородной, в результате чего на ней могут возникать пространственно разделенные участки микрокатодов и микроанодов.
На анодных участках протекает реакция:
Si + 2H2O + ne+ ® SiO2 + 4H+.
Образовавшийся окисел переводится в растворимый комплекс с помощью плавиковой кислоты:
SiO2 + 6HF ® H2SiF6 + 2H2O.
Суммарная реакция может быть записана как:
Si + ne+ + 2H2O ® SiO2 + 4H+ + (4 – n)e–
¯
6HF
® H2SiF6 + 2H2O
Основными катодными реакциями на кремнии являются выделение водорода и восстановление молекул окислителей. При катодных реакциях могут создаваться гидриды кремния.
Реакция восстановления окислителей, например азотной кислоты, протекает гораздо легче, чем реакция выделения водорода. Процесс может идти с захватом электрона из зоны проводимости или валентной зоны, что равносильно инжекции дырок на поверхности кремния.
Восстановление азотной кислоты происходит с участием двух электронов и образованием азотистой кислоты:
HNO3 + 2H+ ® HNO2 + H2O – 2e+
или с участием трех электронов (восстановление до окиси азота):
HNO3 + 3H+ ® NO + 2H2O + 3e+.
В последнем случае при восстановлении одной молекулы кислоты выделяются три дырки, что приводит к увеличению скорости растворения кремния. Суммарная реакция травления для этого случая имеет вид:
3Si + 4HNO3 + 18HF ® 3H2SiF6 + 4NO + 8H2O.
Согласно этой реакции соотношение HNO3:HF = 1:4,5 молярных процентов, что соответствует максимальной скорости травления кремния.
Анодный процесс определяется разрывом связей кристаллической решетки, поэтому на разных участках поверхности он происходит с различной скоростью. В местах выхода дислокаций и других нарушений решетки анодный процесс протекает более интенсивно.
Таким образом, селективное травление наблюдается в тех случаях, когда используется травитель с анодным контролем. Для получения полированной поверхности должен применяться травитель с катодным контролем.