Выходы промежуточных продуктов.
Если радиолиз воды и разбавленных водных растворов действительно описывается в рамках изложенных выше представлений, то можно использовать измерения химических превращений в облученных растворах для вычисления выходов первичного разложения воды. Большая часть многочисленных и имеющих важное значение работ была выполнена с использованием излучения с низкой ЛПЭ, главным образом γ-излучения 60Со и быстрых электронов.
Необходимо, во-первых, заметить, что на основании принципа сохранения заряда первичный выход G(H3O+) должен быть равен первичному выходу гидратированных электронов:
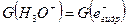 .
.
Аналогично выходу окислительных частиц должен соответствовать эквивалентный выход восстановительных частиц:
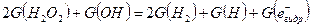 .
.
Из величин, входящих в уравнение, непосредственно может быть измерен выход молекулярного водорода G(H2). Для его измерения необходимо облучить раствор, выбранный таким образом, чтобы ни атомы Н, ни гидратированные электроны при взаимодействии с растворенным веществом не давали бы молекулярного водорода. Растворенное вещество должно также реагировать с радикалами ОН, чтобы предотвратить разложение водорода по реакции
ОН + Н2 → Н2О + Н.
Первичный выход молекулярного водорода, образующегося при облучении чистой воды излучениями с низкой ЛПЭ, равен G(H2)=0,45.
Первичный выход перекиси водорода может быть определен путем исследования ее накопления при облучении воды, содержащей растворенный кислород. В этом растворе все гидратирозанные электроны и атомы Н будут реагировать с кислородом:
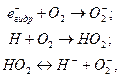
поскольку концентрация кислорода в этой системе значительно выше концентрации перекиси водорода, образующейся при облучении. Радикалы НО2 (или 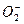 ) рекомбинируют и дают H2O2 и кислород, а радикалы OH взаимодействуют с перекисью водорода с образованием воды и HO2
) рекомбинируют и дают H2O2 и кислород, а радикалы OH взаимодействуют с перекисью водорода с образованием воды и HO2
ОН + Н2O2 → Н2О + НO2.
Радикалы ОН также могут реагировать с водородом, но, если в системе присутствует небольшое количество бромида, ОН будет реагировать преимущественно с ним, давая радикалы, не способные реагировать с водородом, но способные взаимодействовать с перекисью водорода так же эффективно, как и гидроксильные. Учитывая все перечисленные реакции, измеренный выход перекиси водорода в облученном растворе кислорода и бромида должен быть равен
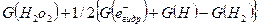
или, используя уравнение баланса.
2G(H2O2) – G(H2).
Так как G(H2) известен, то легко вычислить G(H2O2). Подобно выходу первичного молекулярного водорода, выход перекиси водорода часто уменьшается при увеличении концентрации растворенного вещества. Выход при бесконечном разведении может быть найден экстраполяцией. При изучении радиолиза описанной выше системы и других систем было найдено, что «первичный» выход перекиси водорода G(H2O2) =0,71 для случая действия излучения с малой ЛПЭ на чистую воду.
Первичный выход атомов водорода может быть оценен из данных по радиолизу систем, подобных той, при изучении которой впервые было доказано образование атомарного водорода при радиолизе.
Количество водорода, образующегося при облучении водного раствора изопропанола с добавкой ацетона, складывается из первичного водорода и водорода, выделяющегося в реакции. Так как выход первичного молекулярного водорода G = 0,45, то G(H) может быть найден по разности. При радиолизе многих систем излучениями с малой ЛПЭ найдено, что G(H)=0,55.
G(OH) и С(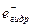 ) могут быть получены при изучении действия излучения на водные растворы, содержащие слабые восстановители, например формиат и растворенный кислород из воздуха. Радикалы ОН будут реагировать с восстановителем, например:
) могут быть получены при изучении действия излучения на водные растворы, содержащие слабые восстановители, например формиат и растворенный кислород из воздуха. Радикалы ОН будут реагировать с восстановителем, например:
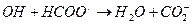 ,
,
а образовавшийся радикал будет взаимодействовать с кислородом:
 .
.
Как гидратированные электроны, так и атомы Н будут давать также 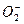 (НО2), которые будут диспропорционировать с образованием перекиси водорода и кислорода. Выход образующейся перекиси водорода G(F) будет равен
(НО2), которые будут диспропорционировать с образованием перекиси водорода и кислорода. Выход образующейся перекиси водорода G(F) будет равен
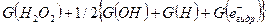 .
.
Используя уравнение баланса, получаем
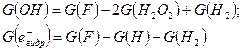 .
.
Значения выходов, стоящих в правой части этих уравнений, известны, так что можно определить G(OH) и G(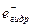 ). В случае действия излучений с малой ЛПЭ на чистую воду наиболее надежным значением является G(OH) = G(
). В случае действия излучений с малой ЛПЭ на чистую воду наиболее надежным значением является G(OH) = G(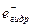 ) = 2,7. Первичные выходы радиолиза воды, приведенные в таблице, слабо или вовсе не зависят от температуры.
) = 2,7. Первичные выходы радиолиза воды, приведенные в таблице, слабо или вовсе не зависят от температуры.
Выходы промежуточных продуктов радиолиза чистой нейтральной воды при облучении коротковолновым рентгеновским, γ-излучением или быстрыми электронами
| Частица | 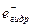
| ОН | H | Н2 | Н202 | Н2O+ |
| G | 2,7 | 2,7 | 0,55 | 0,45 | 0,71 | 2,7 |
Высокие концентрации кислоты оказывают малое влияние на выходы радикальных и молекулярных продуктов. В растворах рН = 0÷1 общий выход восстановительных радикалов для излучений с малой ЛПЭ равен 3,7 (здесь не имеет смысла проводить различие между атомами водорода и гидратированными электронами, так как последние реагируют с ионами водорода по реакции). Выход перекиси водорода повышается до G = 0,8, а выход радикала ОН – до G = 2,9. Выход молекулярного водорода изменяется очень мало. В щелочных растворах выходы также несколько увеличиваются. Эти явления, без сомнения, обусловлены в основном реакциями предшественников первичных частиц. Например, в нейтральных растворах может протекать реакция гидратированных электронов с перекисью водорода в шпорах, когда же концентрация кислоты велика, гидратированные электроны в шпорах будут реагировать также и с ионами Н+, давая атомы Н, которые, как известно, реагируют с перекисью водорода гораздо медленнее, чем гидратированные электроны.
Попытки измерить первичные выходы радиолиза при действии излучения с высокой ЛПЭ (например, α-частиц 210Ро) привели к результатам, намного более зависящим от природы растворенного вещества и от его концентрации, чем в случае радиолиза излучениями с малой ЛПЭ. Это, по-видимому, связано с тем, что треки частиц с высокой ЛПЭ настолько коротки, что радикалы правильнее могут рассматриваться первоначально располагающимися в цилиндрах, а не в изолированных группах. Поэтому, когда радикалы диффундируют из трека, существует заметная конкуренция между реакциями этих радикалов с другими первичными продуктами и реакциями с растворенным веществом, в то время как при действии излучения с малой ЛПЭ радикалы вряд ли реагируют с другими радикалами после того, как они продиффундируют даже на очень малое расстояние от места своего рождения.
Одним из последствий увеличивающегося взаимодействия первичных продуктов при действии излучения с высокой ЛПЭ является то, что некоторые из радикалов ОН должны обязательно реагировать с перекисью водорода. Реакция между ОН и HО2 может иметь место и в случае излучений с малой ЛПЭ, но, если в системе присутствуют вещества, способные реагировать с ОН, вероятность ее настолько мала, что этой реакцией можно пренебречь. Однако при действии излучений с высокой ЛПЭ подобным взаимодействием пренебрегать нельзя, и продукт этой реакции – радикал НО2 (или 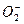 ) может рассматриваться почти как первичный продукт. При действии α-частиц 210Ро (одного из наиболее изученных излучений с высокой ЛПЭ) на воду найдено, что G(HO2)=0,25. Если рассматривать радикал НО2 как первичный продукт, то уравнение приобретает вид
) может рассматриваться почти как первичный продукт. При действии α-частиц 210Ро (одного из наиболее изученных излучений с высокой ЛПЭ) на воду найдено, что G(HO2)=0,25. Если рассматривать радикал НО2 как первичный продукт, то уравнение приобретает вид
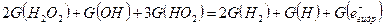 .
.
Для α-частиц 210Ро первичный выход молекулярного водорода равен G = 1,6÷1,8, перекиси водорода–1,1÷1,7 и радикалов ОН – 0,5÷0,7. Большинство работ с α-излучением проводилось до открытия гидратированного электрона, и во всех случаях облучались кислые растворы: общий выход восстановительных радикалов равен G = 0,4÷0,5.