Волновые функции, описывающие электрон в атоме водорода.
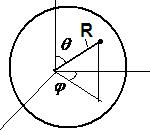
Потенциальная энергия сферически симметрична, поэтому оператор Лапласа в уравнении Шредингера обычно записывается в сферических координатах и при решении (13-1в) требуется использование сферических координат, в которых ψ =ψ(r,θ,φ).
Оператор Лапласа в сферических координатах представляется в виде двух частей – радиальной и угловой.

Поэтому:
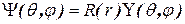 ,
,
где  - радиальная функция,
- радиальная функция,  - угловая функция,
- угловая функция,
 . (13-2)
. (13-2)
Уравнение Шредингера вследствие сферической симметрии распадается на 3 уравнения, каждое из которых зависит только от одной переменной – радиальной r, меридиональной θ и азимутальной φ.
Волновая функция ψ должна удовлетворять 3 условиям (см. выше),а также условиюнормировки.
 , (13-3)
, (13-3)
где модуль ψ2 определяет плотность вероятности найти данную частицу в объеме dV. Поэтому, уравнение (13-3) – есть условие достоверности нахождения частицы во всем пространстве.
Решение для угловой части волновой функции
А). Из условия сферической симметрии, а также условия однозначности волновой функции следует:
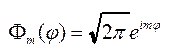
являются функциями целочисленного аргумента m который может принимать значения m=0,±1,±2…
Б). Функция Θ - непрерывная и однозначная является специальной функцией – присоединенным полиномом Лежандра. При подстановке этой функции в (13-1б) получается уравнение, которое имеет однозначные и конечные решения только при целочисленных значениях l, которые:
- могут быть отрицательными
- связаны с числом m: m=-l,…,0,…l .
В).Угловая функция Y= ΘФ зависит от l , и при решении уравнения Шредингера дает квантование момента импульса электрона в атоме:
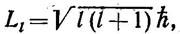 (13-4)
(13-4)
и проекцию момента импульса на выделенное направление
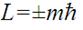 . (13-5)
. (13-5)
С точки зрения графического решения угловая функция определяет форму электронного облака и его ориентацию.
Решение для радиальной части волновой функции
Радиальная функция R выражается через шаровые функции и полиномы Лагерра. Частное решение имеет вид:

(13-6)
Где
 ,
,
А). Подстановка функции R в исходное уравнение (13-1в) дает характеристическое уравнение, из решения которого следует, что при W < 0 (электрон «связан» в атоме) энергия электрона определяется выражением:
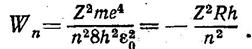 (13-7)
(13-7)
которое описывает энергетические уровни электрона в водородоподобной системе и является аналогичным выражению в теории Бора:
Таким образом, последовательное решение уравнения Шредингера для электрона в водородоподобной системе приводит к энергетическим уровням типа Бальмера - Ридберга без использования каких-либо постулатов.
б). Найдем вероятность того, что электрон в основном состоянии атома водорода находится на расстоянии r от ядра (n=1,l=0) в интервале расстояний от r до r+dr, т. е. в шаровом слое с объемом dV=4πr2dr.Вероятность обнаружить электрон в элементе объема dV:
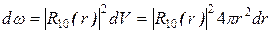
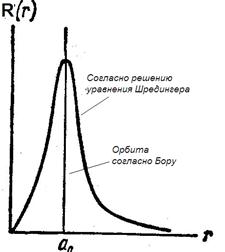
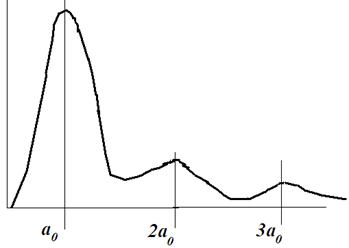
Если подставить в эту формулу выражение (13-6), то получим зависимости плотности вероятности обнаружения электрона от расстояния. Максимумы этих зависимостей дают те расстояния rnот ядра атома, на которых электрон может быть обнаружен с наибольшей вероятностью(рис.13-1 а и б).
 А)
А)
|  Б)
Б)
|
Рис.13-1
В частности, при n=1 исследование выражения dw/dr на максимум дает r1=а0. Этот результат является частным случаем более общего вывода: боровские орбиты электрона представляют собой геометрические места точек, в которых электрон может быть обнаружен с наибольшей вероятностью.
Например, по теории Бора, вероятность обнаружить электрон в состоянии с n =1 отлична от нуля только для r1=а0. . Согласно же квантовой механике, эта вероятность лишь достигает максимума при r1=а0 , но она отлична от нуля во всем пространстве.
На рис. 13-1 сопоставлены вероятности обнаружить электрон на различных расстояниях от ядра по теории Бора и по квантовой механике.