Суммарная реакция, протекающая в ходе работы гальванического элемента, имеет вид
Реакция обеспечивающая проводимость во внутренней цепи
Реакции на аноде и катоде
А) Zn – 2е = Zn+2, К) Cu+2 +2е = Cu.
Zn+2 + SО4-2 = ZnSО4.
Zn + CuSО4 = Cu + ZnSО4.
Электродвижущая сила гальванического элемента (ЭДС) равна разности электродных потенциалов двух полуэлементов.
Например, для элемента Даниеля-Якоби
E = φ0(Cu2+/Cu) - φ0(Zn2+/Zn) = +0,34 - (-0,76) = 1,1 В.
В общем виде электродвижущая сила (ЭДС) гальванического элемента находится по формуле
Eгальван. эл- та = Е катода – Е анода. 9.1)
3 Водородный электрод сравнения. Электрохимический ряд
Абсолютные значения электродных потенциалов в настоящее время не известны, поэтому на практике применяют относительные значения.
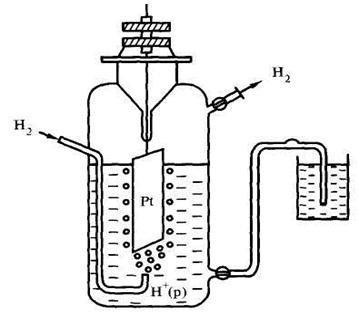
В качестве электрода сравнения был выбран «водородный электрод». Устройство этого электрода показано на рисунке 9.2.
|
 |
.
Для получения сравнимых результатов измерения проводятся при следующих стандартных условиях: Т = 298 К, р = 1 атм., С(соли) = 1 моль/л.
Электродный потенциал измеряется в вольтах (В). Для водородного электрода стандартный потенциал условно приняли равным нулю.
В соответствии с уменьшением восстановительных свойств металлы располагаются в следующий электрохимический ряд:
Li K Na Mg Al Ti Mn Zn Fe Pb H Bi Cu Ag Pt Au.
В электрохимическом ряду левее водорода расположены металлы стандартные электродные потенциалы которых имеют отрицательные значения, а правее водорода – металлы стандартные электродные потенциалы которых имеют положительные значения.
Например, φ0(Zn2+/Zn) = -0,76 В,φ0(Cu2+/Cu) = +0,34 В.
4 Уравнение Нернста
Если условия отличаются от стандартных, то величину электродного потенциала рассчитывают по уравнению Нернста.
φ = φ0 +  (9.2)
(9.2)
где R – универсальная газовая постоянная (8,31 Дж/моль·К),
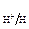 .
.