Выразим текущее количество теплоты, которой обмениваются внешний источник и рабочее тело, в виде
 , (1)
, (1)
где  - общее количество теплоты, участвующей в процессе, х – характеристика теплообмена.
- общее количество теплоты, участвующей в процессе, х – характеристика теплообмена.
Рассмотрим задачу определения х в общем виде.
Параметры газа находятся путём решения уравнения первого закона термодинамики, выраженного в дифференциальной форме:
 . (2)
. (2)
Здесь: dQ, dV и dT – дифференциалы, соответственно, теплоты, объёма и температуры газа, М – количество молей газа,  – истинная мольная теплоёмкость, p – давление.
– истинная мольная теплоёмкость, p – давление.
Введём понятие относительного объёма v и удельной теплоты процесса  , полученных путём отнесения абсолютных объёма V и теплоты Q0 к какому-либо объёму
, полученных путём отнесения абсолютных объёма V и теплоты Q0 к какому-либо объёму  , например, к начальному, конечному или промежуточному, являющемуся характерным для данного процесса.
, например, к начальному, конечному или промежуточному, являющемуся характерным для данного процесса.
Достаточным условием для решения (2) в элементарных функциях является выражение относительной интенсивности теплообмена w = dx/dv в виде ряда  . Интегрируя выражение w при к = 1, получим искомую величину х.
. Интегрируя выражение w при к = 1, получим искомую величину х.
Текущее значение характеристики теплообмена равно
 . (3)
. (3)
Индексы 1 и 2 соответствуют относительным объёмам в начале и конце процесса, отсутствие индекса - текущему объёму.
Интенсивность теплообмена
 . (4)
. (4)
Зависимость протекания характеристик х от относительного объёма для разных значений показателя характеристики m приведена на рис. 3.
Формы кривых определяются величиной и знаком показателя m, а также направленностью процесса – сжатием или расширением.
В обоих случаях при m = 0 значение х линейно зависит от объёма. Подвод теплоты осуществляется мгновенно при объёме v1 для m = + при расширении и для
при расширении и для  при сжатии. В случае противоположных знаков показателя m мгновенный подвод теплоты осуществляется при объёме v2.
при сжатии. В случае противоположных знаков показателя m мгновенный подвод теплоты осуществляется при объёме v2.
Однонаправленный термотропный процесс для идеального газа рассматривается при постоянном отношении теплоёмкостей k и только для процессов сжатия или расширения.
Параметры процесса. Запишем дифференциальное уравнение первого закона термодинамики в виде
 , (5)
, (5)
где q0 = Q0 / Vхар - удельная теплота процесса, отнесённая к характерному для данного процесса объёму Vхар, k – отношение истинных теплоёмкостей газа при постоянных давлении и температуре газа (коэффициент адиабаты), 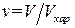 - относительный объём, р – давление.
- относительный объём, р – давление.
Зависимости (3) и (4) справедливы для однонаправленных процессов, представляющих собой только сжатие или только расширение.
Подстановка (4) в (2) и последующее интегрирование позволяет получить выражения текущего давления однонаправленного процесса для случая постоянного отношения теплоёмкостей (коэффициента адиабаты) k
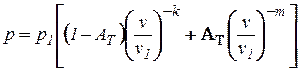 , (6)
, (6)
где безразмерный параметр  , (7) Здесь
, (7) Здесь  - коэффициент использования теплоты процесса, равный доле теплоты топлива, используемой на изменение внутренней энергии и работу.
- коэффициент использования теплоты процесса, равный доле теплоты топлива, используемой на изменение внутренней энергии и работу.
Текущие температуры здесь определяются по уравнению состояния
 ,
,
Относительные объёмы, при которых наступают максимальные значения давления и температуры процесса равны:
 , (8)
, (8)

 . (9)
. (9)
Текущая удельная работа процесса, отнесённая к базовому объёму,
 . (10)
. (10)
В ДВС максимальные температуры и давления при сгорании располагаются на линии расширения, при этом для реальных процессов 1,5 < m < 7.