Адиабатный процесс (закон Пуассона, 1823 г.).
(французский физик и математик Симеон Дени Пуассон,1781-1840).
Процесс, происходящий без теплообмена с окружающей средой, называется адиабатным, т. е. q = 0. Для того чтобы осуществить такой процесс, следует либо теплоизолировать газ, т. е. поместить его в адиабатную оболочку, либо провести процесс настолько быстро, чтобы изменение температуры газа, обусловленное его теплообменом с окружающей средой, было пренебрежимо мало по сравнению с изменением температуры, вызванным расширением или сжатием газа. Как правило, это возможно, ибо теплообмен происходит значительно медленнее, чем сжатие или расширение газа.
Параметры адиабатного процесса находятся путём решения дифференциального уравнения первого закона термодинамики, которое для адиабатного процесса принимает вид:
cv dT + pdv = 0.
Преобразовав и проинтегрировав, получаем
p1 v1 k = p2 v2 k.
Это и есть уравнения адиабаты идеального газа при постоянном отношении теплоемкостей (k = const).
Величина
k = cp / cv
называется показателем адиабаты. Согласно классической кинетической теории теплоемкость газов не зависит от температуры, поэтому можно считать, что величина k также не зависит от температуры и определяется числом степеней свободы молекулы. Для одноатомного газа k = 1,66, для двухатомного k = 1,4, для трех- и многоатомных газов k =1,33.
|
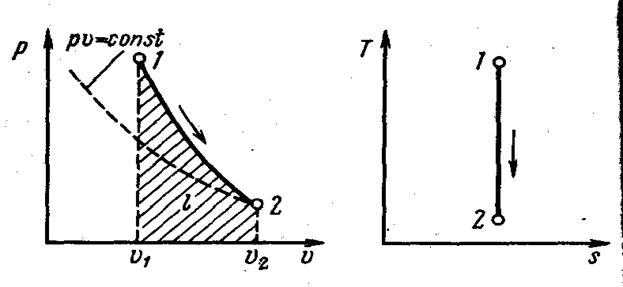
| Рис. 4.4. Изображение адиабатного процесса в р, v- и Г, «-координатах |
Поскольку k > 1, то в координатах р- v (рис. 4.4) линия адиабаты идет круче линии
изотермы, таким образом при адиабатном расширении давление понижается быстрее, чем при изотермическом, так как в процессе расширения уменьшается температура газа.
В адиабатном процессе Δq = сад = 0.