Теплоемкость газов и их смесей
Литература
Контрольные вопросы и домашнее задание
| № | Содержание | Литература |
| Какой процесс, происходящий в синхронном генераторе, называется холостым ходом? | 2, § 4-4 | |
| Что является критерием для оценки синусоидальности кривой ЭДС, индуцируемой в обмотке якоря синхронного генератора (указать формулу расчёта) | 2, § 4-4 | |
| Способы улучшения формы кривой ЭДС в явнополюсной и неявнополюсной синхронной машине? | 2, § 4-4 | |
| Что понимают под характеристикой холостого хода электромашинного генератора? | 2, § 4-4; 3, §33-2 | |
| Что такое нормальная характеристика холостого хода? | 2, § 4-4 | |
| Что такое реакция якоря? | 3, §33-1 | |
| Как изменяется реакция якоря синхронного генератора при емкостном, активном и индуктивном характере нагрузки? | 3, §32-2 | |
| Как зависят магнитные потоки реакции якоря явнополюсной и неявнополюсной синхронной машины от МДС обмотки якоря? | 3, §32-2 | |
| В чем заключается метод двух реакций? | 3, §32-2 | |
| Определить продольную и поперечную составляющие МДС якоря трехфазного синхронного генератора при номинальной мощности Sном = 150 кВА; U1ном = 6,3 кВ; cosψ = 0,8, если его четырехполюсная обмотка статора с обмоточным коэффициентом kw1 = 0,92 содержит в каждой фазе по w1 =312 последовательно соединенных витков, а нагрузка генератора – номинальная | 1, §33-1 |
1. Токарев Б.Ф. Электрические машины.– М.: Энергоатомиздат, 1990, 624 с.
2. Копылов И.П. Электрические машины – М.: Логос, 2000, 607с.
3. Вольдек А.И. Электрические машины. – Л.: Энергия, 1978. – 832с.
Отношение количества теплоты dQ, полученного телом при бесконечно малом изменении его состояния, к связанному с этим изменению температуры тела dT называется теплоемкостью тела в данном процессе:
C = dQ/ dT.
Обычно величину теплоемкости относят к единице количества вещества и в зависимости от выбранной единицы различают:
1) удельную массовую теплоем-кость с, отнесенную к 1 кг газа и измеряемую в Дж/(кг∙К);
2) удельную объемную теплоем-кость с', отнесенную к количеству газа, содержащегося в 1 м3 объема при нормальных физических условиях, и измеряемую в Дж/(м3∙К);
3) удельную мольную теплоемкость mс, отнесенную к одному киломолю и измеряемую в Дж/ (кмоль∙К).
Зависимость между удельными теплоемкостями устанавливается очевидными соотношениями:
с = mс/ m; с' = mс/22,4; с' = сrн. (2.13)
Здесь 22,4 м3 и rн – объем одного киломоля и плотность газа при нормальных условиях.
Изменение температуры тела при одном и том же количестве сообщаемой теплоты зависит от характера происходящего при этом процесса, поэтому теплоемкость является функцией процесса. Это означает, что одно и то же рабочее тело в зависимости от процесса требует для своего нагревания на один градус различного количества теплоты. Численно величина с изменяется в пределах от +¥ до – ¥.
В термодинамических расчетах большое значение имеют:
- теплоемкость при постоянном давлении
cp = dqp/ dT, (2.14)
равная отношению удельного количества теплоты dqp, сообщенной телу в процессе при постоянном давлении, к изменению температуры тела dT;
- теплоемкость при постоянном объеме
cv = dqv/ dT, (2.15)
равная отношению удельного количества теплоты dqv, подведенной к телу в процессе при постоянном объеме, к изменению температуры тела dT.
В соответствии с первым законом термодинамики для закрытых систем
dq= du + pdv.
С учетом соотношения (2.1)

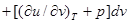 .(2.16)
.(2.16)
Для изохорного процесса (v = const) это уравнение принимает вид:
 ,
,
и, учитывая (2.15), получаем, что
 ,(2.17)
,(2.17)
т.е. теплоемкость тела при постоянном объеме равна частной производной от его внутренней энергии по температуре и характеризует темп роста внутренней энергии в изохорном процессе с ростом температуры.
С учетом (2.2) для идеального газа
cv = du/ dT. (2.18)
Для изобарного процесса (р = const) из уравнений (2.16) и (2.14) получаем:

 ,
,
или 
 .(2.19)
.(2.19)
Это уравнение показывает связь между теплоемкостями ср и сv. Для идеального газа оно значительно упрощается. Действительно, внутренняя энергия идеального газа определяется только его температурой и не зависит от объема, поэтому (ди/дv)T = 0 и, кроме того, из уравнения состояния (1.3) следует р(дv/дТ)р = R, откуда
ср = сv + R. (2.20)
Соотношение (2.20) называется уравнением Майера и является одним из основных в технической термодинамике.
В процессе v = const теплота, сообщаемая газу, идет лишь на изменение его внутренней энергии, тогда как в процессе p = const теплота расходуется и на увеличение внутренней энергии и на совершение работы против внешних сил. Поэтому ср больше сv на величину этой работы. Следовательно, газовая постоянная R численно равна работе расширения одного килограмма газа при нагревании его при постоянном давлении на один кельвин.
Для реальных газов ср – сv > R, поскольку при расширении реальных газов (при p = const) совершается работа не только против внешних сил, но и против сил притяжения, действующих между молекулами, что вызывает дополнительный расход теплоты.
Обычно теплоемкости определяются экспериментально, но для многих веществ их можно рассчитать методами статистической физики.
Поскольку теплоемкость газа зависит от температуры, в термодинамике различают истинную и среднюю теплоемкости.
Средней теплоемкостью сm данного процесса в интервале температур от t1 до t2называется отношение количества теплоты, сообщаемой газу, к разности конечной и начальной температур (t2 – t1):
 . (2.21)
. (2.21)
Выражение c = dq/ dT (2.22)
определяет теплоемкость при данной температуре, или так называемую истинную теплоемкость.
Из (2.22) следует, что
 , (2.23)
, (2.23)
поэтому  .
.
Для практических расчетов теплоемкости всех веществ сводят в таблицы, причем с целью сокращения объема таблиц средние теплоемкости приводят в них для интервала температур от 0 до t ˚C [2, 3].
Среднюю теплоемкость в интервале температур от t1 до t2 находят по формуле:
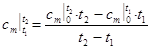 . (2.24)
. (2.24)
Тогда, учитывая (2.21),

 . (2.25)
. (2.25)
Все изложенное относится также к мольным и к объемным теплоемкостям.
Для приближенных расчетов при невысоких температурах можно принимать следующие значения мольных теплоемкостей:

Теплоемкость смесей идеальных газов
Если смесь газов задана массовыми долями, то ее массовая теплоемкость определяется как сумма произведений массовых долей на массовую теплоемкость каждого компонента:
 ,
,  . (2.26)
. (2.26)
При задании смеси объемными долями объемная теплоемкость смеси
 ,
,  . (2.27)
. (2.27)
Аналогично мольная теплоемкость смеси равна сумме произведений объемных долей на мольные теплоемкости составляющих смесь газов:
 ,
,
 . (2.28)
. (2.28)