Лекция 8. Растворы электролитов
По способности проводить электрический ток в водном растворе или в расплаве вещества делятся на электролиты и неэлектролиты. Электролитами называются вещества, растворы или расплавы которых проводят электрический ток. К электролитам относятся соли, кислоты, основания. В молекулах этих веществ имеются ионные или ковалентные сильно полярные химические связи.
Неэлектролитами называются вещества, растворы или расплавы которых не проводят электрический ток. К ним относятся, например, кислород, водород и многие органические вещества (сахар, эфир, бензол и др.). В молекулах этих веществ существуют ковалентные неполярные или малополярные связи.
Для объяснения электропроводности растворов и расплавов солей, кислот и оснований шведский ученый С. Аррениус создал теорию электролитической диссоциации (1887).
1. Молекулы электролитов при растворении или расплавлении распадаются на ионы (электролитическая диссоциация). Ионы – это атомы или группы атомов, имеющие положительный или отрицательный заряд.
2. В растворе или расплаве электролитов ионы движутся хаотически. При пропускании через раствор или расплав электрического тока положительно заряженные ионы движутся к отрицательно заряженному электроду (катоду), а отрицательно заряженные ионы движутся к положительно заряженному электроду (аноду). Поэтому положительные ионы называются катионами, отрицательные ионы – анионами. К катионам относятся: ион водорода Н+, ион аммония NH4+, ионы металлов Na+, K+, Fe2+, А13+, катионы основных солей CuOH+, А1(ОН)2+, FeOH2+ и т.д. К анионам относятся: гидроксид-ион ОН–, ионы кислотных остатков Сl– NO3–, SO42–, Сг2О72–, анионы кислых солей НСО3–, Н2РО4– и т.д.
3. Диссоциация – процесс обратимый. Это значит, что одновременно идут два противоположных процесса: распад молекул на ионы (ионизация, или диссоциация) и соединение ионов в молекулы (ассоциация, или моляризация).
Диссоциацию молекул электролитов выражают уравнениями, в которых вместо знака равенства ставят знак обратимости (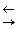 ). В левой части уравнения записывают формулу молекулы электролита, в правой – формулы ионов, которые образуются в процессе электролитической диссоциации. Например:
). В левой части уравнения записывают формулу молекулы электролита, в правой – формулы ионов, которые образуются в процессе электролитической диссоциации. Например:
 .
.
Каждая молекула гидроксида аммония диссоциирует на ион аммония и ион гидроксида. Следовательно, в результате диссоциации одной молекулы образуется два иона. Общая сумма зарядов катионов равна общей сумме зарядов анионов и противоположна по знаку (т.к. растворы электролитов электронейтральны).
Механизм электролитической диссоциации. Гидратация ионов.Причины и механизм диссоциации электролитов объясняются химической теорией растворов Д. И. Менделеева и природой химической связи. Растворители, в которых происходит диссоциация, состоят из полярных молекул (вода). Химическая теория растворов основана на представлении об определяющей роли явления сольватации при растворении веществ. Сольватация – процесс химического взаимодействия частиц растворенного вещества с молекулами растворителя, приводящий к образованию сольватов (гидратов, если растворителем является вода). Диссоциация электролитов с ионной и полярной связями протекает не одинаково. В растворах электролитов все ионы находятся в гидратированном состоянии. Растворение электролита можно представить в виде процесса, включающего следующие стадии:
1) ориентация вокруг частиц растворенного вещества полярных молекул растворителя;
2) поляризация молекул (частиц) растворенного вещества под действием полярных молекул растворителя;
3) разрыв связей между частицами растворенного вещества с образованием сольватированных ионов.