Лекция 14. Гидролиз солей. Буферные растворы
Контрольные вопросы
1. Произведение растворимости.
2. Растворимость и ее связь с произведением растворимости.
3. Условия образования и растворения осадков.
4. Ионно-обменные реакции.
5. Направление протекания ионно-обменных реакций.
6. Реакции нейтрализации.
Рекомендуемая литература
1. Глинка Н.Л. Общая химия: Учебное пособие для вузов / Н.Л. - Глинка. М.: КНОРУС, 2009. - с. 252 - 258.
2. Коровин Н.В. Общая химия. Учебник для технических направ. и спец. Вузов – 7-е изд., испр. – М.: Высшая школа, 2006 – с. 232 - 234.
А.Т. Чанышева
Ключевые слова: гидролиз, гидролиз по катиону, гидролиз по аниону, гидролиз по катиону и аниону, константа гидролиза(Кг),степень гидролиза(h),рH растворов солей, буферные растворы, буферная емкость, расчет рH буферных смесей.
Гидролиз солей -это ионно-обменное взаимодействие соли с водой. Реакция протекает, если в продуктах образуется слабая кислота и/или слабое основание. Она основана на поляризующем действии ионов соли на молекулы воды, в результате, которого нарушается равновесие диссоциации воды: Н2О Н+ + ОН-.Гидролиз - это реакция обратная нейтрализации, и следовательно идет с поглощением тепла, процесс эндотермический.
Н+ + ОН-.Гидролиз - это реакция обратная нейтрализации, и следовательно идет с поглощением тепла, процесс эндотермический.
Соли, образованные сильными основаниями и сильными кислотами (NаСl, КNO3, Rb2SO4), не содержат ионов, способных к взаимодействию с водой, поэтому гидролизу не подвергаются. Реакция среды в растворе таких солей нейтральная (рH=7).
Гидролиз по катионухарактеризует соли, образованные сильной кислотой и слабым основанием (NH4Cl, ZnSO4, Al(NO3)3). В результате катион соли связывает ионы ОН- из воды. В растворе увеличивается концентрация ионов Н+ и реакция среды становится кислой (рH<7).Например:
NH4+ + HOH  NH4OH + H+ (уравнение в краткой ионной форме)
NH4OH + H+ (уравнение в краткой ионной форме)
NH4Cl + HOH  NH4OH + HCl (полное молекулярное уравнение)
NH4OH + HCl (полное молекулярное уравнение)
Количественно гидролиз характеризуется константой гидролиза (Кг) и степенью гидролиза (h). Константа гидролиза соли сильной кислоты и слабого основания рассчитывается по формуле:
Кг = [Кв ∕ Косн], где Кв – ионное произведение воды, Косн – константа диссоциации слабого основания.
Расчет рН в растворе соли слабого основания и сильной кислоты осуществляют по формуле:
рН = 7 + ½ lgKосн - ½ lgСсоли, где Ссоли – молярная концентрация соли.
Гидролиз по анионухарактеризует соли, образованные слабой кислотой и сильным основанием (NаF, Na2CO3, Rb3PO4). Анион соли связывает катион Н+ воды и в растворе накапливаются ионы ОН-, среда щелочная (рH > 7).
F- + H2O  H+ + OH- (уравнение в краткой ионной форме)
H+ + OH- (уравнение в краткой ионной форме)
NaF + HOH  HF + NaOH (полное молекулярное уравнение)
HF + NaOH (полное молекулярное уравнение)
Константа гидролиза соли сильного основания и слабой кислоты рассчитывается по формуле:Кг=[Кв ∕ Ккисл], где Ккисл – константа диссоциации слабой кислоты.
Расчет рН в растворе соли сильного основания и слабой кислоты осуществляют по формуле: рН = 7 - ½ lgKкисл + ½ lgСсоли.
Гидролиз по катиону и аниону протекает в растворах солей, образованных слабой кислотой и слабым основанием (NH4CN, NH4СH3COO). Реакция среды в растворах таких солей близка к нейтральной. Может быть слабокислой или слабощелочной и определяется способностью к диссоциации продуктов гидролиза: слабой кислоты и слабого основания.
NH4F + HOH  NH4OH + HF (полное молекулярное уравнение)
NH4OH + HF (полное молекулярное уравнение)
Константа гидролиза соли слабого однокислотного основания и слабой одноосновной кислоты:Кг = [Кв /(Ккисл∙Косн)].
Расчет рН в растворе соли слабого основания и слабой кислоты:
рН=7 - ½ lgKкисл + ½ lgКосн.
Соли, образованные слабым основанием и слабой кислотой (Al2S3, Cr2S3, Al2(СО3)3) могут подвергаться необратимому разложению водой, если в продуктах образуются осадки или выделяется газ. Водные растворы таких солей не существуют. Например: Al2S3 + 6 HOH  2 Al(ОН)3 + 3H2S↑
2 Al(ОН)3 + 3H2S↑
Степень гидролиза соли (h)- это отношение количества вещества соли, подвергшегося гидролизу, к общему количеству вещества соли. Константа гидролиза (Кг) и степень гидролиза (h) связаны соотношением:
Кг=Ссоли.h2/(1-h), где Ссоли- молярная концентрация соли в растворе.
Если h<<1, то Кг = Ссоли.h2; 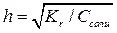 .
.