Электрическое производство алюминия
Вследствие высокой прочности оксид алюминия не восстанавливается водородом и металлами. Углерод начинает восстанавливать его только при 2500ºС, но при этой температуре образуется карбид алюминия. Поэтому оксид алюминия можно восстановить только на катоде и в отсутствие ионов, имеющих меньшие потенциалы разряда по сравнению с алюминием.
Ввиду высокой температуры плавления 2050ºС электролитическому восстановлению подвергаются только его растворы. Из большого количества изученных растворителей наиболее подходящим оказался расплавленный криолитNa3AlF6 (3NaF∙AlF3). Это вещество:
1)хорошо растворяет оксид алюминия в расплаве;
2)не содержит ионов, более электроположительных, чем Al3+;
3)имеет сравнительно высокую электрическую проводимость.
Теоретически смесь, содержащая 10% Al2O3 и 90% Na3AlF6, плавится при температуре 962ºС. В производственных условиях исходная смесь (шихта) содержит 8-10% Al2O3 и 90-92% Na3AlF6. Температура плавления шихты находится в приделах 980-1000ºС. Для повышения электрической проводимости и компенсации диссоциировавшего AlF3 в составе криолита в электролит добавляют AlF3 и фториды кальция и магния.
Электролиз реализуется на инертных электродах из углеродистых материалов. При растворении Al2O3 происходит диссоциация оксида алюминия на ионы:
Al2O3 → Al3+ + AlO33-
вплоть до ионов Al3+ и O2-, которые, возможно частично соединяются в ионы AlO2- и AlO+.
На угольном катоде, в первую очередь, происходит разряд ионов алюминия Al3+ с нормальным потенциалом -1,66 В (на электродах разряжаются в первую очередь ионы, обладающие наименьшим потенциалом разряда):
Al3+ +3e = Al0
Выделившийся на катоде алюминий имеет более высокую плотность
ρ = 2,73 г/см, чем расплав ρ = 2,35 г/см, поэтому опускается на дно ванны.
На угольном аноде наиболее вероятен разряд ионов AlO2- и AlO33-:
2AlO33- - 6e = Al2O3 + 1,5O2
2AlO2- - 2e = Al2O3 + 0,5O2
На аноде кислород реагирует с углеродом (сжигает анод) с образованием оксида углерода (IV).
Производство алюминия можно считать совмещённым электрохимическим и электротермическим процессом, так как электролизёр работает и как электрохимическая печь. Расплавление электролита и поддерживание необходимой температуры обеспечивается электронагревом, т. е. часть энергии электрического тока превращается в необходимую для процесса теплоту.
Электрохимическое производство алюминия осуществляется на алюминиевых заводах, расположенных большей частью вблизи крупных электростанций, производящих большое количество дешёвой электрической энергии
В промышленности применяют электролизёры с обожжёнными или самообжигающимися анодами (Рис. 8.4).
Электролизёр состоит из катодного и анодного устройств. Катодное устройство представляет собой металлический кожух прямоугольной формы с огнеупорной изоляцией 1, футерованный изнутри огнеупорным кирпичом 2 и поверх его угольными блоками 3.
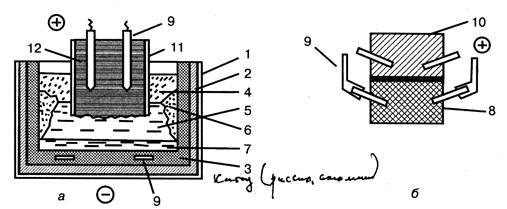
Рис. 8.4. Схема электролизёра: а – ванна с самообжигающимися анодами; б – блок с предварительно обожжённым анодом
1 - кожух, 2 – огнеупорная футеровка, 3 – футеровка из огнеупорных плит, 4 – глинозём, 5 – слой расплавленного электролита, 6 – гарнисаж, 7 – слой алюминия, 8 – рабочий блок обожжённого анода, 9 – токопроводы, 10 – наращиваемый блок, 11 – кожух анодной массы, 12 – анодная масса.
Нижние (подовые) блоки являются одновременно токоподводами 9 (к которым подводится ток, с помощью медного токопровода) для расплавленного алюминия, играющего роль катода.
Электролизёр снабжён:
1) системой газоулавливания;
2) системой дожигания оксида углерода (II);
3) устройством для непрерывной подачи глинозёма;
4) системой откачивания металлического алюминия.
Анодное устройство состоит из угольных анодов, частично погружённых в расплавленный электролит, и запрессованных в них токопроводов 9.
Так как материал анода участвует в процессах электролиза, то они непрерывно обгорают, что приводит к изменению расстояния между электродами и к нарушению режима процесса. Для устранения этого явления применяют непрерывные аноды различной конструкции. В электролизёрах используют аноды двух типов: самообжигающиеся и предварительно обожжённые.
В современных электролизёрах высокой мощности применяют предварительно обожжённые аноды, которые состоят из блоков, наращиваемых сверху по мере их обгорания. Токопроводы впрессованы с боку в готовые блоки.
Плотность криолита, алюминия и глинозёма в твёрдом состоянии равны, соответственно: 2,95; 2,70 и 3,90 т/м3.
При температуре электролиза плотность расплавленного алюминия составляет 2,3 т/м3, а электролита – около 2.0 т/м3. Вследствие разности плотностей жидкий алюминий отделяется от криолито-глинозёмного расплава и собирается на дне ванны.
В процессе электролиза в результате охлаждения ванны наружным воздухом на поверхности расплава образуется твёрдый слой электролита (горнисаж), который утепляет ванну и тем самым снижает расход энергии.
Для извлечения из ванны расплавленного алюминия используются вакуумные ковши или сифоны, засасывающая труба которых вводится в жидкий алюминий через слой горнисажа.
Глинозём непрерывно подаётся в электролизёр пневматического штокового устройства, позволяющего пробивать корку горнисажа и дозировать глинозём.
Из верхнего пространства ванны – электролизёра, снабжённого вентиляционной установкой оттягиваются анодные газы (CO2, CO, HF), пыль глинозёма и криолита. Токсичные газы перед выбросом в атмосферу очищаются, соединения фтора улавливаются.