При электролизе, чтобы протекали рассмотренные реакции надо создать такое напряжение.
Процессы, протекающие на электродах, препятствуют протеканию тока от внешнего источника. В связи с этим, приложенное извне напряжение для осуществления электролиза не должно быть меньше ∆E0поляр.
Разница между значениями напряжения разложения и поляризации называется перенапряжением.
Электрохимическим реакциям, протекающим на электродах могут препятствовать более медленные предшествующие или последующие реакции (процессы переноса частиц в растворе - подход к электроду частиц, которые будут окисляться или восстанавливаться, удаление продуктов реакции или восстановления с поверхности электродов). Кроме того, медленно протекает процесс разрушения гидратной оболочки ионов (без ее разрушения катион, подошедший к катоду, не сможет восстановиться), а также последующий процесс объединения атомов в двухатомные молекулы таких газов – Н2, О2, Cl2.
Все эти процессы препятствуют электролизу, поэтому напряжение, при котором начнется выделение конечных продуктов, должно быть больше теоретически рассчитанного значения. Повышение напряжения, необходимого для развития процесса электролиза, называется перенапряжением. (Оно обусловлено суммарным влиянием различных причин.)
При наличии перенапряжения потенциал катода сдвигается в сторону меньших значений, а потенциал анода сдвигается в сторону больших значений(тем самым реальное напряжение оказывается выше, чем теоретическое значение).
Значение перенапряжения зависит от природы электролита, (т.е. химической природы ионов, которые должны разряжаться), и от природы электрода и состояния его поверхности. Особое значение имеет перенапряжение Н2 и О2.
7.2.2. Теория электролиза основана на законах Фарадея:
1-й закон Фарадея - количество вещества, выделяющееся на электродах, прямо пропорционально количеству электричества,прошедшему черезэлектролит;
m = k∙Q = m = M∙I∙τ/n∙F
где k-электрохимический эквивалент вещества (масса вещества, выделившаяся или растворившаяся с электрода, при прохождении одного кулона электричества) k = мг/Кл. Q - количество электричества = I∙τ; (А∙с). τ - время (с), F – число Фарадея Кл/моль (F = Ne∙e = 6,022045∙1023 моль-1, е = 1,6021892∙10-19 Кл).
2-й закон Фарадея - при прохождении одного и того же количества электричества через разные электролиты, количества веществ, выделившиеся на электродах, пропорциональны химическим эквивалентам этих веществ:
m1:m2 = k1:k2 = 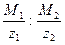 .
.
Из 2-го закона Фарадея следует, что для выделения эквивалента любого вещества требуется израсходовать одно и то же количество электричества. Это количество электричества называется числом Фарадея и равно 96500 Кл/моль.
(эквивалентом называется некая реальная или условная частица, которая может присоединять, высвобождать или быть каким-либо другим образом эквивалентна одному иону водорода в кислотно-основных реакциях или одному электрону в окислительно-восстановительных реакциях).
Основными технологическими показателями электролиза и критериями рационального использования энергии служат:
выход по току;
степень использования энергии;
напряжение, приложенное к электролизёру.
1. Выходом по току η (% или доли единицы) называется отношение массы продукта, фактически полученной при электролизе, Gпр., к теоретической массе, Gт., которая должна получиться по законам Фарадея:
η = Gпр/Gт. · 100
Gт = I · τ · k
(k = E/3600)
2. Степенью использования энергии µ (%), называется отношение количества энергии Wт., теоретически необходимого для выделения единицы продукта, к практически затраченному количеству энергии, Wпр.:
µ = Wт./Wпр. ∙ 100
Wт = vт∙I∙τ/Gт, Wпр. = v пр.∙I∙τ/G пр.
где vт и vпр. – теоретическое и практическое напряжение разложения, В.
vпр. = (φар – φкр) + φконц. + (φапер. – φкпер.) + ∑I∙R
φар и φкр - равновесные потенциалы; [φкон + (φапер. – φкпер.)] перенапряжение за счет концентрационной поляризации, анодное и катодное перенапряжение; ∑I∙R - преодоление омических сопротивлений электролита, электродов, контактов и т.п.