Области применения серной кислоты
Товарные сорта серной кислоты
Производство серной кислоты
В технике под серной кислотой понимают любые смеси триоксида серы с водой, собственно безводную серную кислоту Н2SO4 называют моногидратом, раствор SO3 в 100 % H2SO4 называют олеумом.
Физические свойства.Безводная серная кислота (моногидрат) – бесцветная маслянистая жидкость с Ткр = 10,37 ºС, Тк = 296,2 ºС, ρ = 1,85 г/см3, не дымит, не имеет цвета и запаха, смешивается с водой и серным ангидридом в любых соотношениях. При смешении образуется ряд соединений с различными температурами кристаллизации.
Современная промышленность выпускает несколько товарных сортов серной кислоты и олеум, отличающихся концентрацией и чистотой:
Сорт кислоты Содер-е Содер-е tкристалл. ºС H2SO4% SO3%Купоросное масло 92-93% 0,0 -22,0Башенная кислота 75-76% 0,0 -29,5(нитрозный способ)Контактная кислота 92,5-94% 0,0 -22,0Олеум 104,5% 20% +2,0Высокопроцентныйолеум 114% 65% -0,35
Эти составы сортов товарной серной кислоты выделены как обладающие наименьшими температурами кристаллизации, это сделано для того, чтобы избежать кристаллизации серной кислоты при ее перевозке и хранении.
Среди минеральных кислот, производимых химической промышленностью, серная кислота по объему производства и потребления занимает первое место: мировое производство серной кислоты составляет в настоящее время 160 млн. тонн в год.
Концентрированная серная кислота не разрушает черные металлы. В то же время, серная кислота относится к числу самых сильных минеральных кислот.
1) Серная кислота широко используется в производстве фосфорных минеральных удобрений, различных солей и кислот. На производство минеральных удобрений расходуется до 50% всей вырабатываемой серной кислоты.
2) Большое количество (до 10%) серной кислоты используют для очистки нефтепродуктов и цветных металлов.
3) В металлообрабатывающей промышленности серную кислоту используют для снятия ржавчины с поверхности чёрных металлов перед защитным покрытием их лаками и цветными металлами.
4) Разбавленную серную кислоту и её соли применяют при производстве красителей (до 15%), лаков; лекарственных, моющих и взрывчатых веществ, в текстильной промышленности и производстве химических волокон.
5) В качестве катализатора в гидролизном производстве
6) Водоотнимающее вещество при осушке газов

Сырье для производства серной кислоты.
Историческая справка. До середины XVIII века серную кислоту в незначительных количествах получали термическим разложением железного купороса FeSO4∙7Н2О, поэтому и сейчас один из сортов серной кислоты называется купоросным маслом. В настоящее время серная кислота производится двумя способами:1) нитрозным (башенным), существующем более 200 лет, 2) контактным, освоенным в промышленности в конце ХIХ и начале ХХ века.Контактный способ является более эффективным, что и послужило причиной вытеснения нитрозного способа из промышленности. 3.2. Сырьё.Сырьё. Сырьём для производства серной кислоты могут быть свободная сера, и различные серосодержащие соединения (рисунок). Из них в дальнейшем после обработки могут быть получены сера или непосредственно оксид серы (IV). Природные залежи самородной серы невелики. Чаще всего сера находится в природе в сульфидов и сульфатов металлов, а также входит в состав нефти, каменного угля, природных и попутных газов. Значительные количества серы содержатся в виде оксида веры в топочных газах цветной металлургии и в виде сероводорода, выделяющихся при очистке горючих газов. 1) Железный колчедан.Наиболее распространённым сульфидом серы является пирит или железный колчедан. Природный железный колчедан представляет собой сложную породу, состоящую из сульфида железа и сульфидов других металлов (меди, цинка, свинца, кобальта, никеля). Содержание серы в колчедане колеблется от 35до 50%. Процесс подготовки рядового колчедана к производству ставит целью извлечение из него ценных цветных металлов и повышение концентрации дисульфида железа. Схема подготовки рядового колчедана представлена на рисункеПеред использованием железного колчедана для производства серной кислоты его подвергают обработке методом флотации с целью извлечения из него ценных металлов и повышения концентрации сульфида железа. Железный колчедан поступает на заводы по производству серной кислоты в виде порошка - флотационного колчедана.
1) Железный колчедан.Наиболее распространённым сульфидом серы является пирит или железный колчедан. Природный железный колчедан представляет собой сложную породу, состоящую из сульфида железа и сульфидов других металлов (меди, цинка, свинца, кобальта, никеля). Содержание серы в колчедане колеблется от 35до 50%. Процесс подготовки рядового колчедана к производству ставит целью извлечение из него ценных цветных металлов и повышение концентрации дисульфида железа. Схема подготовки рядового колчедана представлена на рисункеПеред использованием железного колчедана для производства серной кислоты его подвергают обработке методом флотации с целью извлечения из него ценных металлов и повышения концентрации сульфида железа. Железный колчедан поступает на заводы по производству серной кислоты в виде порошка - флотационного колчедана. Необходимо подчеркнуть, что при переработке сульфидовцветных металлов образуется большое количество оксида серы (IV) (до 10%), который можно непосредственно использовать для производства серной кислоты.

 Источником газовой серы являются газо-конденсатные месторождения и месторождения попутного газа.Из самородных руд серу выплавляют в печах, автоклавах или непосредственно в подземных залежах (метод Фраша). Для этого серу расплавляют непосредственно под землей, нагнетая в скважину перегретую воду, и выдавливают расплавленную серу на поверхность сжатым воздухом.На рисунке представлены схема подготовки самородной серы.
Источником газовой серы являются газо-конденсатные месторождения и месторождения попутного газа.Из самородных руд серу выплавляют в печах, автоклавах или непосредственно в подземных залежах (метод Фраша). Для этого серу расплавляют непосредственно под землей, нагнетая в скважину перегретую воду, и выдавливают расплавленную серу на поверхность сжатым воздухом.На рисунке представлены схема подготовки самородной серы.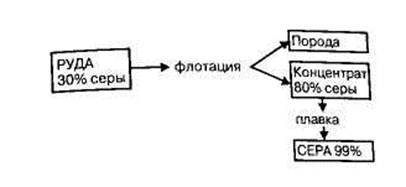 Получение газовой серы из сероводорода, извлекаемого при очистке горючих и технологических газов, основано на процессе неполного окисления его над твердым катализатором. При этом протекают реакции:H2S + 1,5О2 = SO2 + Н2О 2H2S + SO2 = 2H2O + 3S
Получение газовой серы из сероводорода, извлекаемого при очистке горючих и технологических газов, основано на процессе неполного окисления его над твердым катализатором. При этом протекают реакции:H2S + 1,5О2 = SO2 + Н2О 2H2S + SO2 = 2H2O + 3S 2H2S + O2 = 2H2O + 2S.Значительные количества серы могут быть получены из продуктов медеплавильного производства, содержащих различные соединения серы, в частности, пирит. При этом, в процессе плавки протекают реакции, приводящие к образованию элементарной серы: 2FeS2 = 2FeS + 2S, (4FeS + 7О2 = 2Fe2О3 + 4SО2↑ + Q) SO2 + С = S + СО2,CS2 + SO2 = 3S + CO2,2COS + SO2 = 3S + 2CO2.
2H2S + O2 = 2H2O + 2S.Значительные количества серы могут быть получены из продуктов медеплавильного производства, содержащих различные соединения серы, в частности, пирит. При этом, в процессе плавки протекают реакции, приводящие к образованию элементарной серы: 2FeS2 = 2FeS + 2S, (4FeS + 7О2 = 2Fe2О3 + 4SО2↑ + Q) SO2 + С = S + СО2,CS2 + SO2 = 3S + CO2,2COS + SO2 = 3S + 2CO2. 3) Сероводород. При переработке нефтепродуктов в качестве побочного продукта образуется сероводород. Источником сероводорода служат и другие горючие газы: коксовый, генераторный, попутный. Сероводород улавливают, концентрируют, а затем сжигают и получают оксид серы (IV), перерабатываемый в дальнейшем в серную кислоту.
3.3. ПРОИЗВОДСТВО СЕРНОЙ КИСЛОТЫПроизводство серной кислоты из серосодержащего сырья включает несколько химических процессов:1. Первой стадией любого производства серной кислоты является получение сернистого ангидрида SO2 путем обжига серосодержащего сырья. 2. Далее сернистый ангидрид тщательно очищается (особенно в случае контактного метода), окисляют до триоксида серы. 3. Абсорбция триоксида серы водой с образованием серной кислоты.Окисление SO2 в SO3 в обычных условиях протекает крайне медленно. Для ускорения этой стадии процесса применяют катализаторы.В контактном методе производства серной кислоты окисление SO2 до SO3 осуществляется на твердых контактных массах. При нитрозном способе катализаторами служат оксиды азота, окисление проводится в жидкой фазе в башнях с насадкой, поэтому нитрозный способ называется башенным. Загрязнение атмосферы отходящими газами (SO2,. SO3, NO2) башенных производств и низкое качество кислоты – это основная причина вытеснения нитрозного способа.