Замалеев А.
Заключение
В настоящем конспекте лекций представлены современные методы переработки нефти, которые отражают последние достижения нефтехимической и нефтеперерабатывающей промышленности.
Рассмотрены способы подготовки нефти к переработке, принципиальные технологические схемы установки ЭЛОУ, установки атмосферной и вакуумной разгонки мазута. Обсуждены основы термических превращений нефтяных фракций. Рассмотрены принципиальные технологические схемы термических процессов: установок термического крекинга, висбрекинга и замедленного коксования.
Даны основные понятия и закономерности термокаталитических процессов переработки нефтяных фракций. Описаны принципиальные технологические схемы каталитического крекинга и риформинга.
Рассмотрены основные закономерности гидрокаталитических процессов. Показаны важность этих процессов для углубления переработки нефти. Приведены принципиальные технологические схемы гидроочистки нефтяных фракций и гидрокрекинга вакуумных дистиллятов. Рассмотрены основные типы катализаторов гидрогенизационных процессов.
Обсуждены методы очистки и переработки нефтяных газов.
Достаточно подробно рассмотрены основные виды топливной продукции и способы ее получения. Приведена классификация топлив и основные требования к этому виду продукции.
Терминологический словарь
Алкадиены (диеновые углеводороды) - это непредельные углеводороды, содержащие две двойные углерод-углеродные связи. Общая формула алкадиенов СnН2n-2
Алканы (парафины) - это предельные углеводороды с открытой цепью, в которых атомы углерода соединены друг с другом простыми (одинарными) связями, а остальные свободные их валентности насыщены атомами водорода. Члены гомологического ряда предельных углеводородов отвечают общей формуле СnН2n+2
Алкены - это углеводороды, содержащие в молекуле одну двойную связь и имеющие общую формулу СnН2n, их также называют олефинами или этиленовыми углеводородами.
Алкины (ацетиленовые углеводороды) - это непредельные углеводороды, содержащие в молекуле одну тройную связь и имеющие общую формулу СnН2n-2. Родоначальником гомологического ряда этих углеводородов является ацетилен НС≡СН.
Ароматические углеводороды - это органические соединения, состоящие из углерода и водорода и содержащие бензольные ядра.
Асфальтены – твердые, аморфные вещества темно-бурого или черного цвета. При нагревании до 300оС не плавятся, а переходят в пластичное состояние. Асфальтены не растворяются в парафиновых углеводородах С5-С8. Молекулярная масса асфальтенов около 2000 а.е.м.
Валентный угол С-С - угол между линиями, соединяющими связываемые атомы. Для определения валентных углов используют экспериментальные методы изучения структуры химических соединений.
Гомогенный катализ - это ускорение химической реакции в присутствии катализатора, который находится в одной фазе с исходными реагентами (субстратами) в газовой фазе или растворе.
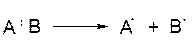
Гемолитические реакции - это реакции, протекающие с гемолизом химической связи, т.е. с таким ее разрывом, при котором электронная пара, осуществляющая связь, разделяется между образующимися фрагментами (свободными радикалами).
Длина химической связи - это межъядерное расстояние между химически связанными атомами. Расстояние между атомами существенно уменьшается при образовании кратных связей, чем выше кратность связи, тем короче межатомное расстояние.
Гетерогенный катализ - это изменение скорости химической реакции при воздействии катализаторов, образующих самостоятельную фазу и отделенных от реагирующих веществ границей раздела. Каталитическая реакция протекает обычно на поверхности твёрдого катализатора и обусловлена активацией молекул реагентов при взаимодействии с поверхностью.
Динамическая вязкость (Па·с) - это сопротивление, оказываемое жидкостью при перемещении относительно друг друга со скоростью 1 м/с двух ее слоев площадью 1 м2 каждый, находящихся на расстоянии 1 м, под действием приложенной силы в 1 Н.
Гетеролитические реакции - это реакции, протекающие с гетеролизом химической связи, т.е. с таким её разрывом, при котором электронная пара, осуществляющая связь, остается у одного из атомов и, как правило, образуются ионы:

Донорно-акцепторный механизм образования химической связи - это перекрывание пустых орбиталей менее электроотрицательного элемента и орбиталей более электроотрицательного элемента с находящимися на них парами электронов.
Ингибиторы - это вещества, тормозящие химические реакции. Ингибирование характерно для каталитических и цепных реакций, которые протекают с участием активных центров или активных частиц.
Карбениевый ион - это положительно заряженный карбкатион, образованный при потери атомом углерода одного электрона.
Катализ - изменение скорости химической реакции при воздействии веществ (катализаторов), которые участвуют в реакции, но не входят в состав продуктов.
Катализаторы - это вещества, изменяющие скорость химической реакции или вызывающие ее, но не входящие в состав продуктов.
Ковалентная химическая связь - химическая связь, которая возникает в результате обобщения неспаренных валентных электронов с противоположными спинами.
Неполярная ковалентная химическая связь - химическая связь, которая возникает между атомами, имеющими равные значения электроотрицательности (при образовании молекул из одинаковых атомов).
Полярная ковалентная химическая связь - химическая связь, которая возникает между любыми атомами, имеющими разные значения электроотрицательности.
Реакция полимеризации - это процесс образования высокомолекулярного соединения (полимера) путем соединения друг с другом молекул исходного низкомолекулярного соединения (мономера).
Свободный радикал - частица, имеющая один или несколько неспаренных электронов.
Смолы- это вязкие малоподвижные жидкости или аморфные вещества от коричневого до темно-бурого цвета. Смолы растворимы в насыщенных углеводородах. Имеют молекулярную массу от 700 до 1000 а.е.м. Смолы являются лабильными веществами, окисляются кислородом воздуха превращаясь в асфальтены.
Степень окисления - условное число, характеризующее заряд атома в соединении, рассчитанный исходя из предположения ионного строения вещества.
Транс-изомеры - это изомеры, заместители которых располагаются по разные стороны углеродного скелета, или плоскости кольца.
Углеводороды - самые простые органические соединения, состоящие из углерода и водорода. В зависимости от характера углеродных связей и соотношения между количеством атомов углерода и водорода они делятся на предельные (насыщенные) и непредельные (ненасыщенные) с одной или несколькими кратными связями. В зависимости от строения углеродной цепи углеводороды относятся к соединениям с открытой (незамкнутой) углеродной цепью и с замкнутой, т.е. к циклическим соединениям.
Циклоалканы (циклопарафины) - это предельные углеводороды, имеющие замкнутые цепи (циклы) и общей формулой гомологического ряда СnН2n.
Цис-изомеры - это изомеры, заместители которых располагаются по одну сторону углеродного скелета или плоскости кольца.
Электровалентная химическая связь - химическая связь, которая возникает за счёт передачи неспаренного электрона одного атома другому с образованием разноимённо заряженных ионов.
Электроотрицательность - условная величина, характеризующая способность атома в молекуле притягивать электроны.
Эмульсии представляют собой дисперсные системы из двух взаимно мало- или нерастворимых жидкостей, в которой одна диспергирована в другой в виде мельчайших капель (глобул). Жидкость, в которой распределены глобулы, называют дисперсионной средой, а диспергированную жидкость – дисперсной фазой.
Энергия связи - это энергия (Е0), необходимая для того, чтобы разъединить атомы и удалить их друг от друга на расстояние, на котором они не взаимодействуют. Для двухатомных молекул энергия связи определяется как энергия диссоциации молекулы на атомы.