Политропный процесс.
Политропным называется процесс, который описывается уравнением
pvn = const. (4.21)
Показатель политропы п может принимать любое численное значение в пределах от – ¥ до + ¥, но для данного процесса он является величиной постоянной.
Из уравнения (4.21) и уравнения Клапейронаполучим выражение, устанавливающие связь между р, v и Т в любых двух точках на политропе, аналогично адиабате:
p2/ p1 = (v1/ v2)n; T2/ T1 =(v1/ v2)n-1;
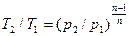 . (4.22)
. (4.22)
Работа расширения газа в политропном процессе
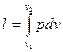 .
.
Т.к. для политропы в соответствии с (4.22) p = p1 (v1/ v)n,
То 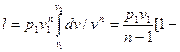
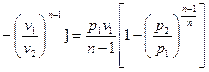 . (4.23)
. (4.23)
В случае идеального газа уравнения (4.23) можно преобразовать к виду
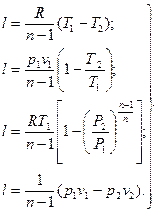 (4.24)
(4.24)
Количество подведенного (или отведенного) в процессе тепла можно определить с помощью уравнения первого закона термодинамики:
q = (u2 – u1) + l.
Поскольку
и2 – и1 = сv (Т2– Т1 ),
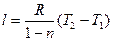 ,
,
то
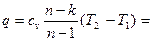
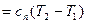 , (4.25)
, (4.25)
где
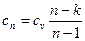 (4.26)
(4.26)
представляет собой теплоемкость идеального газа в политропном процессе. При cv, k и n = const cп = const, поэтому политропный процесс иногда определяют как процесс с постоянной теплоемкостью.
Изменение энтропии
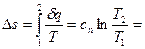
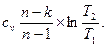 (4.27)
(4.27)
Политропный процесс имеет обобщающее значение, т.к. охватывает всю совокупность термодинамических процессов:
- для изохорного процесса n = ± ¥, cn=cv;
- для изобарного процесса п = 0, cп=cр,
- для изотермического процесса n = 1, cn = ¥;
- для адиабатного процесса n = k, cn = 0.
Все процессы начинаются в одной точке.
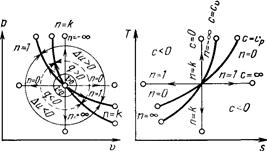
Изображение основных термодинамических процессов идеального газа в р,v – и Т,s – координатах.
Изохора (n = ±¥) делит поле диаграммы на две области: процессы, находящиеся правее изохоры, характеризуются положительной работой, так как сопровождаются расширением рабочего тела; для процессов, расположенных левее изохоры, характерна отрицательная работа.
Процессы, расположенные правее и выше адиабаты (n = k), идут с подводом теплоты к рабочему телу; процессы, лежащие левее и ниже адиабаты, протекают с отводом теплоты.
Для процессов, расположенных над изотермой (n = 1), характерно увеличение внутренней энергии газа; процессы, расположенные под изотермой, сопровождаются уменьшением внутренней энергии.
Процессы, расположенные между адиабатой и изотермой, имеют отрицательную теплоемкость, так как dq и du (а следовательно, и dT)имеют в этой области противоположные знаки. В таких процессах ½l½>½q½, поэтому на производство работы при расширении тратится не только подводимая теплота, но и часть внутренней энергии рабочего тела.