Алкилирование аминов галогенидами
N-алкилирование
В качестве алкилирующих агентов используют алкил- и арилгалогениды, непредельные соединения, спирты, эфиры, эпоксисоединения, диалкилсульфаты, эфиры аренсульфокислот. Поэтому чаще всего реакции N-алкилирования можно рассматривать как нуклеофильное замещение SN2.

а) Сопровождается выделением галогеноводорода, который образует аммониевые соли и затрудняет реакцию, поэтому добавляют вещества, связывающих кислоту. Ими могут быть сам амин, карбонаты натрия, калия, кальция или щелочи. Например, гидрокарбонат натрия для этих целей используют при получении N-бензиланилина (производство диазолина):

б) Скорость реакции алкилированияопределяетнуклеофильность амина. Скорость реакции увеличивается:
-SO2NH2 <-CONH2 <ArNH2 <C5H5N < NH3 < RNH2 < R2NH
- Алкилирование аммиака или алифатических аминовидет с образованием смеси соединений, т.к. введенная алкильная группа делает продукт более реакционноспособным, чем исходный амин:


Тем не менее, реакцию широко используют, т.к. многие лекарственные препараты выпускаются в виде четвертичных аммонийных солей:

- Алкилирование ароматических аминов, нуклеофильность которых в большей степени зависит от заместителей в ядре, чем у атома азота, идет селективнее, чем алкиламинов. Используя низкие температуры, избыток субстрата и другие приемы, можно получать смешанные аминосоединения:


- Алкилирование амидовкарбоновых и сульфоновых кислот идет намного труднее, чем аминов, но зато селективно, что позволяет синтезировать чистые первичные и вторичные амины.
в) Алкилирующий агенттакже влияет на скорость реакции. Быстрее всего реагируют аллильные, бензильные, метильные и первичные галогениды (см.механизм SN2).
В полигалогенидах замещается более хорошо уходящая группа.

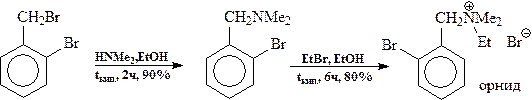
г) Условия реакции зависит от строения и свойств, как субстрата, так и галогенида. Так, температурав случае алкилгалогенидов обычно около 100°С, активированные арилгалогениды реагируют примерно при 150°С. Поэтому в большинстве случаев процесс можно вести при атмосферном давлении в аппарате с обратным холодильником. Однако при работе с низкокипящими веществами (CH3Cl, C2H5Cl) алкилирование ведут в автоклавах.
2. N-Алкилирование галогеноспиртами и эпоксисоединениями широко применяется в синтезе противораковых препаратов.:

Однако наряду с N-алкилированием идет и О-алкилирование.
Поэтому вместо этиленхлоргидрина часто используютокись этиленапри температуре обычно ниже 100°С и небольшом давлении.

Смесь окиси этилена с воздухом взрывается, поэтому синтез ведут при полном отсутствии воздуха, что достигается продувкой аппарата азотом.
3. Диметилсульфат широко используются в производстве целого ряда препаратов, например, в синтезе анальгина:
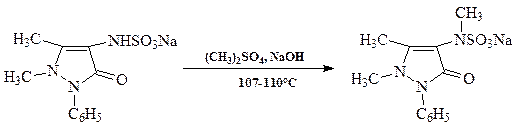
Механизм реакции SN2. В мягких условиях используется лишь одна метильная группа диметилсульфата. Для полного использования диметилсульфата необходимо проводить алкилирование при температуре около 100°С в щелочной среде.
Достоинства диметилсульфата: высокая реакционная способность, относительно дешев и позволяет работать при повышенных температурах при атмосферном давлении. (Температура кипения метилиодида ниже 40оС) Серьезным недостатком является его высокая токсичность.
4. Метиловые эфиры аренсульфокислот - менее токсичны.

5. Алкилирование непредельными соединениямиаминов и азотистых гетероциклов идет легко.
- Так, в синтезе анатруксония используют малоактивированный алкен - аллиловый спирт:

6. Метилирование аминов формальдегидомв среде муравьиной кислоты (по Эшвайлеру-Кларку) идет с высоким выходом, часто количественным, при температурах около 100оС. С помощью этого метода можно алкилировать разные амины.

Однако реакция идет медленно, метод «дорогой», используются агрессивные среды и токсичные вещества. Ароматические амины должны иметь заместители в орто- и пара-положениях. В связи с этим он используется тогда, когда другие способы не дают хороших результатов.

Выход продукта составляет около 90%, отсутствует продукты О-алкилирования.
7. N-Алкилирование спиртами.Обычно используют для алкилирования ароматических аминов. В жидкой фазе реакцию проводят в присутствии минеральных кислот в автоклавах при ~ 220°С и до 10 часов.

Каталитическая роль кислотызаключается в протонировании спирта и образовании хорошо уходящей группы -OÅH2. Вода либо вытесняется нуклеофилом (SN2-механизм), либо отщепляется (SN1-механизм), образуя карбкатион, который реагирует с ароматическим амином:
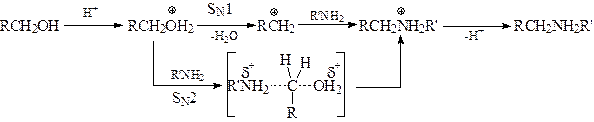
Спирт для алкилирования берется в избытке.
В паровой фазе алкилирование ароматических аминов спиртами проводят при температуре 300-400°С в присутствии окиси алюминия в качестве катализатора.
Алкилирование спиртами в синтезе химико-фармацевтических препаратов имеет меньшее значение.
О-алкилирование (получение простых эфиров)
В качестве алкилирующих агентов гидроксигруппы могут быть использованы алкилгалогениды, непредельные соединения, спирты, эфиры серной и сульфокислот.
1. Алкилгалогениды для О- алкилирования применяются чаще всего:

А) Особенно часто используют доступные и дешёвыеметил- и этилхлориды. Алкилирование ими ведут в автоклавах под давлением, поскольку эти вещества имеют низкую температуру кипения.
Так, метилирование гидрохинона проходит при нагревании водного раствора его натриевой соли с хлористым метилом при температуре 100°С и давлении 2 МПа:
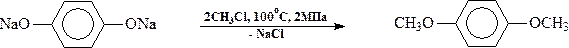
Б) Алкилгалогенид может иметь сложное строение:
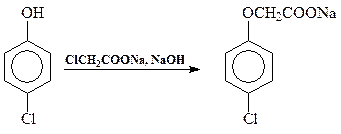
2. Непредельные соединения для О-алкилирования используются реже. Так, при получении b-этоксипропионитрила (для витамина В1) используют акрилонитрил:

3. О-Алкилирование спиртом в присутствии минеральной кислотыиспользуется довольно редко и применяется главным образом для получения диалкиловых эфиров и алкоксипроизводных нафталинового и антраценового ряда. Механизмы SN1 и SN2 (см.мех-зм алкилирования аминов спиртами):

4. О-Алкилированиеэфирами серной кислоты и ароматических сульфокислотимеет значительно большее значение.
Реакция метилирования диметилсульфатомпротекает в щелочной средев две стадии. Щелочь повышает нуклеофильность субстрата и нейтрализует выделяющуюся кислоту:

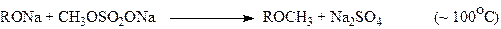
Первая стадия протекает легко при температуре ниже 50°С. Вторая стадия протекает в гораздо более жестких условиях (примерно 100°С) и
При метилировании феноловпри 100°С метильные группы диметилсульфата используются примерно на 90% .

Недостатком метода является токсичность диметилсульфата и неполное использование метильных групп.
Алкилирование фенолов эфирами ароматических сульфокислотпротекает гладко при кипячении с обратным холодильником смеси фенолята и соответствующего эфира аренсульфокислоты.:
