Строение карбоксильной группы
Дикарбоновые кислоты соли
НООС-СООН щавелевая оксалаты
НООС-СН2-СООН малоновая малоаты
НООС-СН2-СН2- СООН янтарная сукцинаты
НООС(СН2)3 СООН глутаровая глутараты
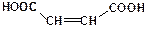 малеиновая (цис-)
малеиновая (цис-)
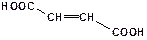
фумаровая (транс-) фумараты
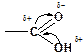 |
Наличие р,p-сопряжения и электроноакцептора (атома кислорода при двойной связи) определяют стабильность карбоксила и его аниона. Поэтому карбоновые кислоты наиболее сильные органические кислоты. Они образуют соли при взаимодействии с металлами, их оксидами, солями и гидроксидами. Пример:
R-COOH + NaOH = R-COONa + H2О
Карбоновые кислоты - важнейшие метаболиты, в организме они встречаются в виде солей. Характерные реакции карбоновых кислот это реакции нуклеофильного замещения (SN). Продукты этой реакции называются «функциональные производные карбоновых кислот». Для них также характерны реакции SN.