Высокая каталитическая активность наночастиц
Поверхностные состояния
Увеличение доли атомов, находящихся в поверхностных состояниях, приводит к:
- увеличению реакционной способности наночастиц,
- росту аморфизации структуры,
- увеличению потенциальной энергии системы,
- увеличению скорости диффузии,
- увеличению вклада поверхностных слоев в теплоемкость, спектр колебаний электронов, электро- и теплопроводность.
Как известно, катализаторы позволяют проводить химические реакции более эффективно, с большей скоростью и при более низких температурах. В качестве катализаторов обычно применяют малые частицы металлов или сплавов, расположенные на подложке с развитой поверхностью.
Высокая каталитическая активность наночастиц обусловлена, в частности, следующими причинами:
- большой долей атомов наночастиц, находящихся на поверхности и имеющих возможность взаимодействовать с внешней средой;
- высокой концентрацией реакционно активных мест (так, в случае золота реакционно активными местами для развития каталитических реакций являются вершины и ребра наночастиц, а в случае платины – грани наночастиц);
- соответствием разницы между энергетическими уровнями электронов тепловой энергии kT (в металлических нанокластерах, имеющих размер порядка 2 нм);
- отличием электронной конфигурации атомов, находящихся на поверхности частиц, по сравнению с внутренними атомами.
Эффект каталитических реакций усиливается за счет использования в качестве основы для нанесения металла нанопористых поверхностей, например, цеолитных, (металл-цеолитные катализаторы).
Катализ с использованием Мо-цеолитных катализаторов применяется в газо-нефтехимии, в частности для преобразования метана (CH4) в бензол (C6H6) с выделением водорода (H2). Реакция происходит в нанопористых каналах цеолита, близких по размерам молекуле бензола, что препятствует появлению нежелательных побочных продуктов и способствует высокой селективности в получении целевого продукта.
Разработаны технологии переработки растительных масел в дизельные топлива с низкой температурой загустевания при использовании наночастиц платины на силикоалюмофосфатной нанооснове.
Традиционно востребованным является катализ выхлопного угарного газа с его преобразованием в углекислый газ в автомобильных нейтрализаторах. Использование платины в наноструктурном состоянии позволяет уменьшить расход дорогого металлы и понизить концентрацию CO. Для этой же цели применяются наночастицы золота (рис.1) Катализ3.avi
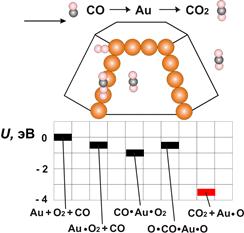
Рис.1. Нейтрализация угарного газа на наночастицах золота (модель). Наночастицы золота задерживают на своих ребрах и вершинах молекулы CO и O2, в результате чего успевает произойти реакция образования CO2. U – энергия системы, изменяющаяся в процессе реакции.