Стереохимия аминокислот
Все аминокислоты, кроме глицина (NH3+CH2COO-), имеют асимметрический (хиральный) атом Ca, поэтому могут существовать в виде двух энантиомеров (оптических изомеров):
H H








 Ca Ca
Ca Ca
 | |||||||
 | |||||||
 | |||||||
 | |||||||
COO – COO –
NH3+ R RNH3+
L-изомер D-изомер
α-Аминокислоты образуют два ряда оптических изомеров: если в проекционной формуле Фишера аминогруппа, по аналогии с глицериновым альдегидом, расположена справа, то это D-изомер, если слева –L-изомер.
По R,S-системе обозначений α-углеродный атом у всех α-аминокислот D-ряда имеет R-конфигурацию, у L-ряда – S-конфигурацию. У аминокислот L-ряда, если рассматривать хиральный атом со стороны атома H, группы NH3+, COO- и радикал R расположены по часовой стрелке, у аминокислот D-ряда – против часовой стрелки.

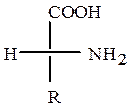
аминокислота L-ряда аминокислота D-ряда
(R-конфигурация) (S-конфигурация)
Треонин, изолейцин, гидроксипролин содержат два асимметрических С-атома. Эти аминокислоты могут образовывать четыре диастереомера, два из которых принадлежат к L-ряду:

L-треонин L-алло-треонин D-треонин D-алло-треонин
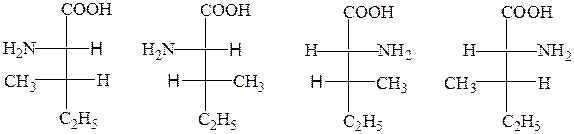
L-изолейцин L-алло-изолейцин D-изолейцин D-алло-изолейцин
Появление заместителя -ОН в пирролидиновом кольце пролина также приводит к образованию алло-форм, в которых гидроксильная и карбонильная группы находятся в цис-положении:

L-гидроксипролин L-алло- D-гидроксипролин D-алло-
гидроксипролин гидроксипролин
Почти все природные α-аминокислоты принадлежат L-ряду. Аминокислоты D-ряда входят в состав некоторых биологически активных олигопептидов, таких антибиотиков, как грамицидин, актиномицин. Д-изомеры, как правило, не усваиваются организмом человека.
Аминокислоты D- и L-рядов значительно отличаются и по вкусу. Так, D-глютаминовая кислота не имеет вкуса, а L-глютаминовая кислота обладает вкусом мяса. Получают ее из клейковины пшеницы и используют в качестве вкусовой добавки к пищевым концентратам. Другие аминокислоты L-ряда (валин, треонин, пролин, серин и т.д.), имея сладкий вкус, привлекают к себе внимание как заменители сахара в питании диабетиков.