Триггерная роль ионов двухвалентного железа
Проинтегрируем последнее уравнение *:
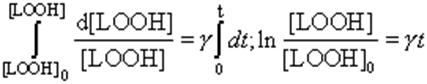 (33)
(33)
Из этого уравнения, а также из уравнения ** следует, что
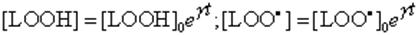
(34)
Последние уравнения показывают, что как концентрация гидроперекисей в системе, так и концентрация цепей окисления (которая равна концентрации радикалов, ведущих цепи) изменяется во времени по экспоненте. Будет ли реакция самоускоряющейся или затухающей, зависит от знака индекса в показателе степени. При g>0 процесс будет самоускоряющимся, при g<0 - самозатухающим. Когда g=0, скорость процесса будет постоянной во времени. От чего же зависит сам индекс? Это можно увидеть, вернувшись к уравнению (32). g=0 при

(35)
Эту концентрацию железа мы назвали "критической концентрацией" обозначили как [Fe2+]*. Из уравнений следует, что
g=0 при [Fe2+]=[Fe2+]* (стационарная реакция),
g>0 при [Fe2+]<[Fe2+]* (ускоряющаяся реакция),
g<0 при [Fe2+]>[Fe2+]* (затухающая реакция).
Вопросы для самоконтроля
- Кинетика реакций цепного окисления липидов. Основные стадии процесса.
- Кинетика реакций цепного окисления липидов. Полная схема химических реакций и пути её упрощения для анализа кинетики.
- Дифференциальные уравнения кинетики цепного окисления липидов. Принцип математического моделирования кинетики этих процессов.
- Аналитическое решение системы уравнений кинетики цепного окисления липидов. Триггерная роль ионов Fe2+.