Любая форма энергии может полностью перейти в теплоту, но теплота преобразуется в другие формы энергии лишь частично.
Т.о., можно условно принять, что внутренняя энергии системы состоит из двух составляющих: "свободной" X и "связанной" Y энергий, причем "свободная" энергия может быть переведена в работу, а "связанная" энергия может перейти только в теплоту.
 (3.11)
(3.11)
Величина связанной энергии тем больше, чем меньше разность температур, и при T = const тепловая машина не может производить работу. Мерой связанной энергии является новая термодинамическая функция состояния, называемая энтропией.
Введем определение энтропии, основываясь на цикле Карно. Преобразуем выражение (I.41) к следующему виду:
 (3.12)
(3.12)
Отсюда получаем, что для обратимого цикла Карно отношение количества теплоты к температуре, при которой теплота передана системе (т.н. приведенная теплота) есть величина постоянная:
 (3.13)
(3.13)  (3.14)
(3.14)
Это верно для любого обратимого циклического процесса, т.к. его можно представить в виде суммы элементарных циклов Карно, для каждого из которых
 (3.15)
(3.15)
Т.о., алгебраическая сумма приведённых теплот для произвольного обратимого цикла равна нулю:
 (3.16)
(3.16)
Выражение (3.16) для любого цикла может быть заменено интегралом по замкнутому контуру:
 (3.17)
(3.17)
Если интеграл по замкнутому контуру равен нулю, то подынтегральное выражение есть полный дифференциал некоторой функции состояния; эта функция состояния есть энтропия S:
 (3.18)
(3.18)
Выражение (3.18) является определением новой функции состояния – энтропии и математической записью второго начала термодинамики для обратимых процессов. Если система обратимо переходит из состояния 1 в состояние 2, изменение энтропии будет равно:
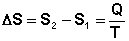 (3.19)
(3.19)
Подставляя в выражения для первого начала термодинамики (3.18., 3.19) получим совместное аналитическое выражение двух начал термодинамики для обратимых процессов:
 (3.20)
(3.20)
 (3.21)
(3.21)
Для необратимых процессов можно записать неравенства:
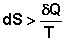 (3.22)
(3.22)
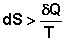 (3.23)
(3.23)
 (3.24)
(3.24)
Т.о., как следует из (I.57), работа обратимого процесса всегда больше, чем того же процесса, проводимого необратимо. Если рассматривать изолированную систему (δQ = 0), то легко показать, что для обратимого процесса dS = 0, а для самопроизвольного необратимого процесса dS > 0.