Примеры решения задач
Задача 1. Запишите уравнения реакций, при помощи которых можно осуществить следующие превращения: S  Na2SO3
Na2SO3  SO2
SO2  Na2S2O3
Na2S2O3  Na2SO4.
Na2SO4.
Решение:
При взаимодействии серы со щелочью образуется сульфид и сульфит:
3S + 6NaOH = Na2SO3 + 2Na2S + 3H2O
Сернистый газ выделяется при взаимодействии сульфита с сильной кислотой:
Na2SO3 + 2HCl = SO2 + 2NaCl + H2O
При одновременном пропускании сернистого газа и сероводорода через раствор щелочи образуется тиосульфат:
4SO2 + 2H2S + 6NaOH = 3Na2S2O3 + 5H2O
При взаимодействии раствора тиосульфата натрия с хлором образуется сульфат натрия:
Na2S2O3 + 4Cl2 + 5H2O = Na2SO4 + 8HCl + H2SO4
Задача 2. Вычислите объем сернистого газа (н. у.), которыйобразовался при обжиге 300 г цинковой обманки, содержащей 48,5 % (мас.) сульфида цинка.
Дано:
m (цинковой обманки) = 300 г
ω (ZnS) = 48,8 %
Найти:
V (SO2)
Решение:
Сернистый газ образуется в результате взаимодействия сульфида цинка с кислородом воздуха:
2ZnS + 3O2 = 2SO2 + 2ZnO
Вычислим массу сульфида цинка, содержащегося в 300 г цинковой обманки:
 , следовательно,
, следовательно,
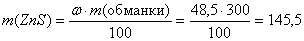 (г)
(г)
По уравнению реакции для образования 2 моль сернистого газа необходимо 2 моль сульфида цинка, то есть соотношение n (ZnS) : n (SO2) равно 1 : 1. Вычислим количество вещества сульфида цинка:
 (моль).
(моль).
Из 1,5 моль сульфида цинка образуется 1,5 моль сернистого газа. Определим его объем:
V = n · Vm = 1,5 · 22,4 = 33,6 (л).
Ответ: V (SO2) = 33,6 л.