СМЕСИ ИДЕАЛЬНЫХ ГАЗОВ
На практике в качестве рабочих тел часто используются смеси газов, состав которых не меняется в процессе смешения. При этом каждый компонент смеси, находясь в общем объеме Vс, имеет давление смеси pс и температуру смеси Tс. Согласно закону Дальтона
 , (2.1)
, (2.1)
где pi – парциальное давление i-го компонента (давление, которое имел бы газ, входящий в состав смеси, если бы он один занимал весь объем смеси при той же температуре).
Смесь газов задается массовыми, объемными или мольными долями, определяемыми соответственно как:
 , (2.2)
, (2.2)
где Mi , Мс, кг – массы i-го компонента и всей смеси;
Vi, м3 – приведенный объем компонента (объем, который бы он занимал при давлении и температуре смеси);
Ni, Nс – число молей i-го компонента и суммарное число молей смеси соответственно.
При этом объемные и мольные доли численно равны  , а также выполняются условия
, а также выполняются условия 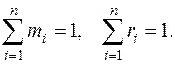
Для перевода массовых долей в объемные можно использовать выражение
 (2.3)
(2.3)
где  , кг/кмоль – молекулярная масса компонента и кажущаяся молекулярная масса смеси соответственно.
, кг/кмоль – молекулярная масса компонента и кажущаяся молекулярная масса смеси соответственно.
Объемные доли в массовые пересчитываются по формуле
 . (2.4)
. (2.4)
Кажущаяся молекулярная масса смеси находится как
 . (2.5)
. (2.5)
Газовая постоянная смеси
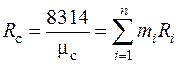 . (2.6)
. (2.6)
Плотность смеси
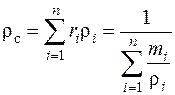 . (2.7)
. (2.7)
Парциальные давления компонентов
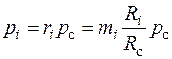 . (2.8)
. (2.8)
Задачи
2.1. В двух баллонах, соединенных трубой с вентилем, находятся: в первом, объемом 0,5 м3 – углекислый газ СО2 при температуре 27 оС и избыточном давлении 3 ат; во втором, объемом 1,2 м3 – кислород при температуре 57 оС и избыточном давлении 2 ат. Определить массовый и объемный состав смеси, газовую постоянную и молекулярную массу смеси, давление смеси и парциальные давления компонентов после открытия вентиля, если установившаяся температура смеси будет равна 43 оС. Барометрическое давление принять равным 1 ат.