Испарение жидкостей. Насыщенный пар
ГОРЕНИЕ ЖИДКОСТЕЙ
Горение жидкостей характеризуется двумя взаимосвязанными явлениями — испарением и сгоранием паровоздушной смеси над поверхностью жидкости. Испарению принадлежит исключительно важная роль, поскольку в конечном итоге оно определяет скорость сгорания жидкости.
Испарение является эндотермическим процессом. Если к жидкости не подводится извне тепло, то в результате испарения она охлаждается. Скорость испарения определяется количеством пара, образующегося за единицу времени на единице поверхности жидкости. Скорость испарения зависит от температуры жидкости. Это необходимо учитывать в производствах, связанных с применением, получением или переработкой легковоспламеняющихся жидкостей. Увеличение скорости испарения при повышении температуры приводит к более быстрому образованию взрывоопасных концентраций паров. Максимальная скорость испарения наблюдается при испарении в вакуум и в неограниченный объем.
Наблюдаемая скорость процесса испарения является суммарной скоростью процесса перехода молекул из жидкой фазы V1 и
скоростью конденсации V2. Суммарный процесс равен разности этих двух скоростей: V= V1 + V2. При постоянной температуре V1 не изменяется, а V 2 пропорциональна концентрации пара. При испарении в вакуум в пределе
V 2 = 0, т. е. суммарная скорость процесса максимальная.
Чем больше концентрация пара, тем выше скорость конденсации, следовательно, ниже суммарная скорость испарения. Жидкость, находящаяся в закрытом сосуде, испаряясь, образует насыщенный пар. Насыщенным называется пар, находящийся в динамическом равновесии с жидкостью. Динамическое равновесие при данной температуре наступает тогда, когда число испаряющихся молекул жидкости равно числу конденсирующихся молекул. Насыщенный пар, выходя из открытого сосуда в воздух, разбавляется им и становится ненасыщенным. Следовательно, в воздухе помещений, где находятся емкости с горячими жидкостями, имеется ненасыщенный пар этих жидкостей.
Давлением насыщенного пара называют давление пара, находящегося в равновесии с жидкостью при данной температуре. Давление насыщенного пара всегда выше, чем ненасыщенного. Оно не зависит от количества жидкости, величины ее поверхности, формы сосуда, а зависит только от температуры и природы жидкости. С повышением температуры давление насыщенного пара жидкости увеличивается; при температуре кипения давление пара равно атмосферному. Для каждого значения температуры давление насыщенного пара индивидуальной (чистой) жидкости постоянно. Давление насыщенного пара смесей жидкостей (нефти, бензина, керосина и др.) при одной и той же температуре зависит от состава смеси. Оно увеличивается с увеличением содержания в жидкости низкокипящих продуктов.
Для большинства жидкостей давление насыщенного пара при различной температуре известно. Эти данные сведены в справочные таблицы и номограммы.
Давление насыщенного пара жидкостей обусловлено числом молекул, ударяющихся о стенки сосуда, или концентрацией паров над поверхностью жидкости. Чем выше концентрация насыщенного пара, тем больше будет
его давление. Связь между концентрацией насыщенного пара и его парциальным давлением можно найти следующим образом.
Допустим, что удалось бы отделить пар от воздуха, причем давление в той и другой частях осталось бы равным общему давлению Робщ. Тогда объемы, занимаемые паром и воздухом, соответственно уменьшились бы. Согласно закону Бойля — Мариотта, произведение давления газа на его объем при постоянной температуре есть величина постоянная, т. е. для нашего гипотетического
случая получим

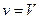 общ
общ
Если объем смеси принять за 100%, то содержание пара С, % (об.) можно найти из пропорции
V - 100 %
 - C
- C
откуда
С=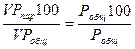
По этой формуле можно определить концентрацию паров жидкости в резервуарах, бочках, цистернах и других емкостях.