Продукты сгорания. Дым
Продуктами сгорания называют газообразные, жидкие и твердые вещества, образующиеся в результате соединения горючего вещества с кислородом в процессе горения. Состав их зависит от состава горящего вещества и условий его горения. При горении их в достаточном количестве воздуха и при высокой температуре образуются продукты полного сгорания: СО2, Н20, N2. При горении в недостаточном количестве воздуха или при низкой температуре кроме продуктов полного сгорания образуются продукты неполного сгорания: СО, С (сажа).
Продуктами сгорания - неорганические вещества, такие как сера, фосфор, натрий, калий, кальций, алюминий, титан, магний и др.
в большинстве случаев являются твердые вещества, например Р2О5, Nа2О2, СаО, МgО, Образуются они в дисперсном состоянии, поэтому поднимаются в воздух в виде плотного дыма. Продукты сгорания алюминия, титана и других металлов в процессе горения находятся в расплавленном состоянии.
Дым представляет собой дисперсную систему, состоящую из мельчайших твердых частиц, взвешенных в смеси продуктов сгорания с воздухом. Диаметр частиц дыма колеблется от 1 до 0,01 мкм.
В составе дыма содержатся продукты термоокислительного разложения горючих веществ. Образуются они при нагреве еще негорящих горючих веществ, находящихся в среде воздуха или дыма, содержащего кислород.
Продукты неполного сгорания и термоокислительного разложения, в большинстве случаев являются токсичными веществами, поэтому тушение пожаров в помещениях производят только в кислородных изолирующих противогазах.
Горючее вещество — индивидуальное химическое соединение.
В этом случае расчет ведут, исходя из уравнения реакции горения. Объем влажных продуктов сгорания единицы массы (кг) горючего вещества при нормальных условиях рассчитывают по формуле
Vп..с. =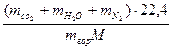 (9)
(9)
где Vп..с. — объем влажных продуктов сгорания, м3/кг; mсо2, mн2о, mN2, mгор — число киломолей диоксида углерода, паров воды, азота и горючего вещества в уравнении реакции горения; М — масса горючего вещества, численно равная молекулярной массе, кг.
Горючее вещество — сложная смесь химических соединений.
Если известен элементный состав сложного горючего вещества, то состав и количество продуктов сгорания 1 кг вещества можно определить по уравнению реакции горения отдельных элементов. Для этого
составляют уравнения реакции горения углерода, водорода, серы и определяют объем продуктов сгорания, приходящийся на 1 кг горючего вещества. Уравнение реакции горения углерода имеет вид
С + О2 + 3,76 = СО2 + 3,76 N2
При сгорании 1 кг углерода получается 22,4/12=1,86 м3
СО2 и 22,4 ·3,76/12 = 7,0 м3 N2.
При горении углерода, водорода и серы кислород поступает из воздуха. Однако в состав горючего вещества может входить кислород, который также принимает участие в горении. В этом случае воздуха на горение вещества расходуется соответственно меньше.
В составе горючего вещества могут находиться азот и влага, которые в процессе горения переходят в продукты сгорания. Для учета их необходимо знать объем 1 кг азота и паров воды при нормальных условиях. Объем 1 кг азота равен 0,8 м3, а паров воды 1,24 м3.
В воздухе при 0°С и давлении 101325 Па на 1 кг кислорода приходится 3,76 ·22,4/32 = 2,63 м3 азота.
На основании приведенных данных определяют состав и объем продуктов сгорания 1 кг горючего вещества
Горючее вещество — смесь газов.
Количество и состав продуктов сгорания для смеси газов определяют по уравнению реакции горения компонентов, составляющих
смесь. Затем определяют состав и количество продуктов сгорания смеси газов.
Анализ продуктов сгорания, взятых на пожарах в различных помещениях, показывает, что в них всегда содержится значительное количество кислорода. Если пожар возникает в помещении с закрытыми оконными, дверными или другими проемами, то пожар при наличии горючего может продолжаться до тех пор, пока содержание кислорода в смеси воздуха с продуктами сгорания в помещении не снизится до 14—16% (об.). Следовательно, на пожарах в закрытых помещениях содержание кислорода в продуктах сгорания может быть в пределах от 21 до 14% (об.).
По содержанию кислорода в продуктах сгорания на пожарах можно судить о коэффициенте избытка воздуха, при котором происходило горение.