Механизм действия буферной системы
Буферные растворы
Лекция 5
Буферные растворы – растворы, которые поддерживают практически постояным рН раствора при добавлении к ним небольших количеств сильных кислот или щелочей, а также при разбавлении.
Примеры буферных растворов.
Компоненты находятся в соотношении 1:1
НСООН, НСООNa
Формиатная буфернвая смесь
рН = 3,7
Ацетатная буферная смесь.
СН3СООН, СН3СООNа
рН= 4,7
Фосфaтная буферная смесь
NaH2PO4, Na2HPO4
pH = 6,8
Аммонийная буферная смесь
NH4OH, NH4CI
pH = 9,3
Индивидуальные вещества
Бура: Na2B4O7 10H2O
Концентрированные растворы кислот и щелочей.
В организме человека присутствуют: гидрокарбонатная, фосфатная, аминокислотная, белковая буферные растворы.
Гидрокарбонатная : H2CO3; NaHCO3 рН = 7,4
Мощная буферная система крови.
Длительное смешение рН даже на десятые доли приводит к смерти.
Фосфатная буферная смесь – основа буферной системы тканей и некоторых биологических жидкостей.
Белковая буферная смесь.
R-COOH
R-COONa
Белки плазмы, гемоглобин, оксигемоглобин
Нв НвО2
КНв КНвО2
Свойство буферной смеси сохранять постоянным рН основано на взаимодействии компонентов буферной смеси с добавленой сильной кислотой или сильным основанием с образованием малодиссоциированных соединений.
В результате этого взаимодействия происходит связывание вводимых Н+ или ОН- ионов в молекулы слабых электролитов.
В кровь попала кислота, рН должен понизиться.
HCI + NaHCO3 = NaCI + H2CO3
H+ + HCO3- = H2CО3
В кровь попала щелочь, рН должен увеличиться.
NaOH + H2CO3 = H2O + NaHCO3
OH- + H2CO3 = H2O + HCO3-
Добавленные ОН- ионы связались в малодиссоциированное соединение – молекулу воды.
рН = рК кислоты – lg 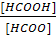
При разбавлении рН не меняется,так как знаменатель и числитель изменяются в одно и тоже число раз.