Химические свойства
Способы получения аминокислот
1. Гидролиз белков (invitro).
2. Аминирование α–галогенкарбоновых кислот:
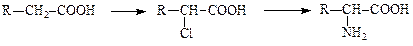
3. Синтез Штреккера:
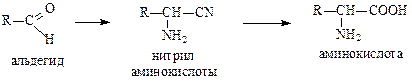
4. Восстановление производных α-кетокислот (восстановительное аминирование):
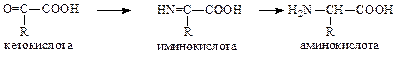
1.Кислотность-основность

неионизированная форма цвиттер-ион
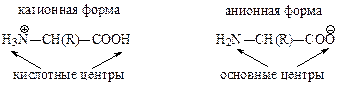
Кислотно-основные свойства аминокислот количественно характеризуют значениями рКа кислотной группы (в том числе и боковых радикалов) и рI – изоэлектрической точкой (см. учебник Н.А. Тюкавкиной «Биоорганическая химия»).
Изоэлектрическая точка соответствует значению рН, при котором концентрация диполярных ионов максимальна, а минимальные концентрации катионной и анионной форм равны. В изоэлектрической точке суммарный заряд молекулы равен 0.
Три группы аминокислот дают разные равновесные системы:
- нейтральные – три формы
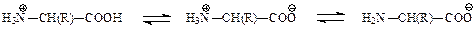
катион цвиттер-ион анион
- кислые (анионогенные) содержат в радикале дополнительно карбоксильную группу и образуют равновесные системы из 4-х форм:
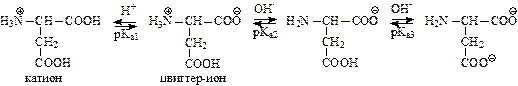
- основные (катионогенные) содержат в радикале дополнительно NН2- группу и образуют равновесные системы из 4-х форм:
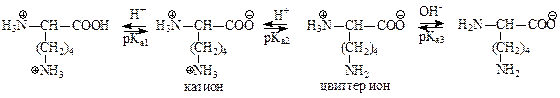
Аминокислоты – амфолиты:
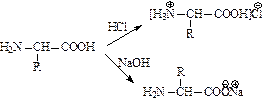
2.Нуклеофильные и электрофильные свойства аминокислот.
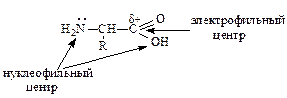
а) Реакции по аминогруппе:
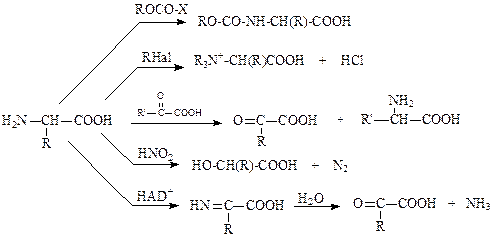
б) Реакции по карбоксильной группе
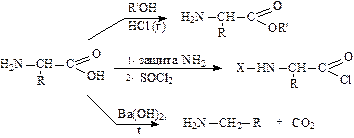
В организме синтез биогенных аминов протекает поддействием пиридоксальфосфата.
|
|
| ||||||


 ДОФА Дофамин Норадреналин Адреналин
ДОФА Дофамин Норадреналин Адреналин
 5-Гидрокситриптофан Серотонин
5-Гидрокситриптофан Серотонин
 Гистидин Гистамин
Гистидин Гистамин
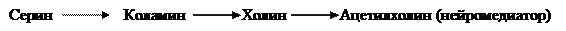 | ||
|
3. Реакции по другим группам:
- гидроксилирования – введение в боковой радикал аминокислоты гидроксильной группы.
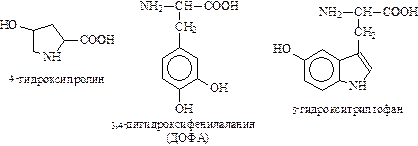
- окисления SH-связей
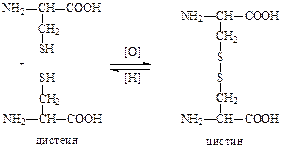
- карбоксилирования – введение карбоксильной группы
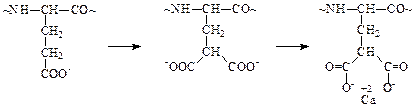
- иодирования – введение атомов иода с образованием иодтиронинов – гормонов щитовидной железы:
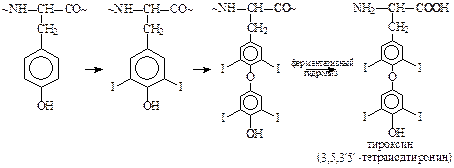
4. Качественные реакции аминокислот.
а) Реакция с нингидрином:
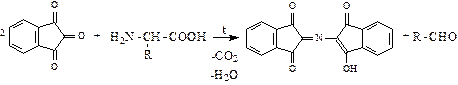
б) Биуретовая реакция
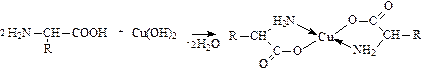
в) Ксантопротеиновая реакция (на Phe, Tyr, Trp, His):
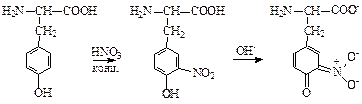
г) реакция на серусодержащие аминокислоты:
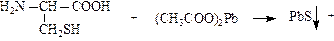
4. Образование пептидов:
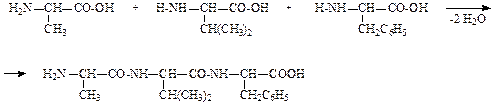
Валиллейцилтриптофан (Val-Leu-Trp)
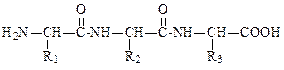
Синтез пептидов осуществляют в несколько стадий:
- защита NH2-группы в первой аминокислоте алкилированием
- защита СООН-группы во второй аминокислоте этерификацией
- активация СООН-группы в первой фосфорилированием
- синтез пептида
- снятие защитных групп
Иначе возможно образование смесей пептидов. Например:
 Ala + Val Ala-Ala + Val-Val + Ala-Val + Val-Ala
Ala + Val Ala-Ala + Val-Val + Ala-Val + Val-Ala
Из 3 разных аминокислот получается трипептидов
из 4 разных аминокислот – тетрапептидов
из 20 разных аминокислот – полипептидов
 g-аминомасляная кислота (ГАМК)(нейромедиатор, транквилизатор)
g-аминомасляная кислота (ГАМК)(нейромедиатор, транквилизатор)