Растворы, их общая характеристика.
ЛЕКЦИЯ 5
Растворы, их общая характеристика, способы выражения состава растворов. Растворимость твердых веществ и газов в жидкостях. Идеальные растворы, законы Вант-Гоффа, Рауля и Генри. Криоскопия и эбулиоскопия. Диаграммы состояния раствор — пар для бинарных систем. Законы Коновалова, азеотропные смеси. Ограниченная взаимная растворимость жидкостей. Взаимно нерастворимые жидкости. Распределение вещества в двух несмешивающихся растворителях. Закон распределения Нернста-Шилова.
Раствором можно назвать гомогенную систему, состоящую из двух или большего числа компонентов, состав которой в определенных пределах может непрерывно изменяться.
Компонент– составная часть раствора, которая может быть выделена из раствора в индивидуальном виде, т. е. в виде чистого вещества.
Растворы классифицируют:
1) по степени дисперсности:
— истинные (молекулярные или атомные смеси компонентов);
— коллоидные (микрогетерогенные);
— тонкие механические взвеси (суспензии и эмульсии).
2) по агрегатному состоянию:
— газовые;
— жидкие;
— твёрдые.
3) с термодинамических позиций:
— идеальные;
— предельно разбавленные (С2 → 0);
— реальные.
Физическая химия изучает термодинамические и другие свойства растворов. Коллоидные растворы и тонкие механические взвеси являются предметом исследования коллоидной химии. Мы будем подробно рассматривать только жидкие растворы.
В жидких растворах обычно различают растворитель и растворенное вещество, хотя с термодинамической точки зрения эти составляющие раствора равноценны. Свойства растворителя обычно обозначаются индексом (1), а свойства растворенных веществ – индексами (2), (3) и т. д.
Растворителем считают то вещество, которое имеется в растворе в большем количестве. Растворенные вещества – остальные компоненты, присутствующие в растворе в меньших количествах.
Существуют различные способы выражения концентраций компонентов.
1) молярная (мольная) доля  – безразмерная величина; (1)
– безразмерная величина; (1)
или 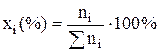 .
.
Здесь ni – количество i-ого компонента (моль).
При этом  или
или  .
.
2) молярность, т.е. количество i-ого компонента в молях, содержащееся в 1 литре раствора.
 , (2)
, (2)
V – объем раствора в литрах, [ci] = моль/л.
3) массовая доля (W) или массовое содержание данного компонента, выраженное в %
 , или
, или  (3)
(3)
Здесь Mi – масса i-ого компонента.
4) объемная доля ji или ji(%)
 , или
, или  , (4)
, (4)
где Vi – объем i-ого компонента, V – объем всей системы.
5) моляльность (mi) или моляльная концентрация – количество i-ого компонента в молях, приходящееся на 1000 г растворителя.
 , моль/1000 г растворителя, (5)
, моль/1000 г растворителя, (5)
где ni – число молей i-ого компонента, М – масса растворителя в граммах.
Уравнение Гибса-Дюгема.
Известно, что в химической термодинамике одной из важнейших величин является химический потенциал (парциальная мольная энергия Гиббса), определяемая по уравнению:
 .
.
При постоянных р и Т справедливо:
 (6)
(6)
С другой стороны, суммарная энергия Гиббса системы равна
 . (7)
. (7)
Продифференцируем уравнение (7):
 . (8)
. (8)
Сравнивая (6) и (8), получаем
 . (9)
. (9)
вводим мольную долю разделив все слагаемые суммы на åni
åxidmI=0 (10)
Уравнение (9) получило название уравнение Гиббса-Дюгемаи широко используется в термодинамике растворов.