Идеальным газом называется такой газ, у которого отсутствуют силы взаимного притяжения и отталкивания между молекулами и пренебрегают размерами молекул.
Уравнение состояния идеального газа
Любой реальный газ тем ближе к идеальному, чем меньше его давление. Равновесное состояние идеального газа как термодинамической системы определяется параметрами 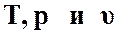 .
.
Между этими термодинамическими параметрами существует связь, которая выражается термически уравнением состояния. Уравнение состояния идеального газа было получено Клайпероном и имеет вид
 , (9)
, (9)
где  ─ газовая постоянная, Дж/(кг×К).
─ газовая постоянная, Дж/(кг×К).
Уравнение (9) записано для массы идеального газа равной 1 кг и носит название уравнения Клайперона.
Для массы газа  уравнение Клайперона примет вид
уравнение Клайперона примет вид
 . (10)
. (10)
Газовая постоянная связана с универсальной газовой постоянной  выражением вида
выражением вида
 , (11)
, (11)
где  ─ молярная масса газа, кг/моль.
─ молярная масса газа, кг/моль.
В теплотехнике гораздо чаще приходиться иметь дело не с однородным газом, а со смесью нескольких газов, например, воздуха, природного газа, продуктов сгорания топлива и др.).
Под смесью идеальных газов понимается механическая смесь различных газов при условии отсутствия в них химических реакций, т.е. химически между собой не взаимодействующих. Смесь идеальных газов тоже подчиняется всем законам, относящимся к идеальным газам.
Для удобства решения практических задач со смесями газов введено понятие о кажущейся молекулярной массе смеси газов, под которой понимается средняя масса из действительных молекулярных масс отдельных компонентов, составляющих смесь.
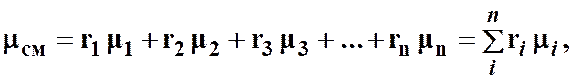 (12)
(12)
где 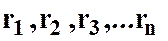 ─ объёмные доли компонентов.
─ объёмные доли компонентов.
Уравнение состояния смеси газов выводится на основании уравнений состояния отдельных компонентов смеси и имеет вид
 , (13)
, (13)
где  ─ газовая постоянная смеси.
─ газовая постоянная смеси.
Если известны массовые доли отдельных компонентов смеси, то газовая постоянная смеси может быть определена по уравнению
 (14)
(14)
где 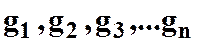 ─ объёмные доли компонентов.
─ объёмные доли компонентов.
Газовую постоянную смеси можно найти также по формуле
 . (15)
. (15)