Понятие об электроотрицательности химических элементов. Заряды ионов и степени окисления химических элементов в соединениях
Способы образования ковалентной связи. Длина и энергия связи. Образование ионной связи
Задания для самостоятельной работы
2.6. Образование химической связи в ионе аммония осуществляется:
1) по донорно-акцепторному механизму;
2) из-за электростатического притяжения ионов азота и водорода;
3) в результате образования общей электронной пары азота и водорода;
4) вследствие обмена электронами между молекулой и ионом.
2.7. Максимальное число ковалентных связей, образуемых атомом азота, равно:
1) 3 2) 4 3) 5 4) 6.
2.8. Длина полярной связи увеличивается в ряду:
1) PCl5, PF5 2) ClF3, BrF3 3) SnCl4, SiCl4 4) C2H6, C2H4.
2.9. Вещество, в узлах кристаллической решетки которого находятся частицы Mg+2 и Cl–, образовано ___ связью.
Степень окисления– это условный заряд атома в соединении, вычисленный исходя из предположения, что атом полностью отдал или принял электроны.
Правила определения степени окисления
1). Степень окисления атомов в простом веществе равна 0.
2). В бинарных соединениях степень окисления у элементов с большей электроотрицательностью отрицательна, а с меньшей – положительна.
3). Общая сумма степеней окисления в молекуле или соединении равна 0, а в ионе – заряду иона.
4). Фтор в соединениях проявляет лишь степень окисления –1. Степень окисления водорода в соединениях обычно равна +1 (кроме гидридов); степень окисления кислорода в соединении обычно равна –2 (кроме фторида кислорода ОF2, где его степень окисления равна +2, пероксидов, где она равна –1 и некоторых других веществ).
5). В ионных соединениях степень окисления элементов равна заряду их ионов, в ковалентных полярных соединениях – числу оттянутых или притянутых электронов.
Степень окисления может быть и дробным числом. Например:  ,
, 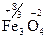 .
.
Задания для самостоятельной работы
2.10. Степень окисления +5 азот имеет в соединении:
1) HNO2 2) N2O3 3) N2O5 4) NH4NO2.
2.11. Установите соответствие между символами химического элемента и возможными значениями его степеней окисления.
СИМВОЛ ЭЛЕМЕНТА СТЕПЕНИ ОКИСЛЕНИЯ
1) Br А) –2, –1, 0, +2
2) O Б) –2, 0, +4, +6
3) As В) –3, 0, +3, +5
4) N Г) –3, 0, +2, +3, +4, +5
Д) –1, 0, +1, +3, +5, +7
Е) –4, –2, 0, +2, +4.
2.12. Наибольшая степень окисления атома серы в соединении:
1) K2S 2) Na2SO4 3) K2SO3 4) S
2.13. Степень окисления азота в ионе NO2– равна:
1) –1 2) –3 3) +3 4) +5
2.14. Степень окисления –1 кислород имеет в соединении:
1) H2O; 2) N2O5; 3) NaOH; 4) Na2O2.