Для полного сжигания 1кг горючего
Определение потребного количества окислителя
РАСЧЕТ ПРОЦЕССОВ ГОРЕНИЯ
Основные цели расчета процесса горения сводятся к определению следующих величин.
1. Определение потребного количества окислителя для полного сжигания 1кг горючего.
2. Определение количества и состава продуктов сгорания.
3. Определение температуры конца сгорания продуктов сгорания.
4. Определение теплосодержания (энтальпии) продуктов сгорания.
Расчет ведут обычно на 1 кг рабочей массы сжигаемого топлива. В основу положены уравнения баланса, использование которых можно понять на примере окисления горючих элементов, входящих в состав рабочей массы топлива.
Рассмотрим стехиометрические реакции окисления горючих веществ, входящих в состав горючего.
Окисление водорода рабочей массы топлива
2H2 + O2 = 2H2O (1.1)
4кг H2 +32кг O2 = 36кгH2O
1кг H2+ 8кг O2 = 9кгH2O
Из этого уравнения следует, что каждый килограмм сжигаемого водорода требует 8 кг кислорода, при этом образуется 9 кг воды. Если в рабочей массе сжигаемого топлива содержится Hp % водорода, то для окисления водорода, входящего в 1 кг такого топлива, необходимо иметь массу кислорода (в кг), равную
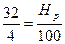 .
.
Аналогично можно определить потребное количество кислорода для окисления углерода и серы.
С + O2 = СO2 (1.2)
12кг С + 32кг O2 = 44кг СО2
1кг С + 8/3кгO2 = 11/3кгСО2
S + O2 = SO2 (1.3)
32кг S + 32кгO2 = 64кг SО2
1кг S + 1кг O2 = 2кг SО2
Если вычесть уже содержащийся в топливе кислород, то его потребность (в кг) на каждый килограмм сжигаемого топлива выразится соотношением
 кгкислорода/кгтоплива.
кгкислорода/кгтоплива.
В этом соотношении сумма величин, стоящих в числителе, показывает потребное количество кислорода необходимое для полного окисления рабочей массы горючих элементов топлива. Рабочая масса кислорода Ор горючего входит в состав горючего в виде соединений и участвует в реакции окисления, поэтому она вычитается.