Этих факторов множество, поэтому и способы защиты от них многообразны -- от физиологических свойств до структурных приспособлений, позволяющих преодолевать их пагубное действие.
Вирусные болезни широко распространены среди насекомых, поэтому для борьбы с насекомыми-вредителями можно использовать природные вирусы насекомых, препараты которых называют вирусными пестицидами. В отличие от ядохимикатов они обладают узким спектром действия, не убивают полезных насекомых, они быстро разрушаются во внешней среде и не опасны для растений и животных. Наряду с вирусами насекомых используются как биопестициды некоторые грибы, поражающие насекомых-вредителей. Применяемые сейчас биопестициды являются природными штаммами энтомопатогенных вирусов и грибов, однако не исключена возможность создания в будущем методами генетической инженерии новых эффективных биопестицидов.
К числу наиболее распространенных гербицидов, используемых при обработке зерновых культур, относится атразин. Он подавляет фотосинтез, связываясь с одним из белков фотосистемы II и прекращая транспорт электронов. Устойчивость к гербициду возникает в результате точечных мутаций в этом пластохинон связывающем белке (замена серина на глицин), вследствие чего он теряет способность взаимодействовать с гербицидом. В ряде случаев удалось осуществить перенос гена мутантного белка в чувствительные к атразину растения с помощью Ti-плазмиды. Интегрированный в хромосому растений ген устойчивости был снабжен сигнальной последовательностью, которая обеспечивала транспорт синтезируемого белка в хлоропласты. Химерные растения проявляли значительную устойчивость к таким концентрациям атразина, которые вызывали гибель контрольных растений с геном белка дикого типа. Некоторые растения способны инактивировать атразин путем отщепления остатка хлора ферментом глутатион-S-трансфераза. Этот же фермент инактивирует и другие родственные гербициды триазинового ряда (пропазин, симазин и др.).
Приложение 7. Инструкция по применению препарата-модификатора эМПи-1
Приложение 6. Образец удостоверения на право проведения полной ревизии букс с роликовыми подшипниками
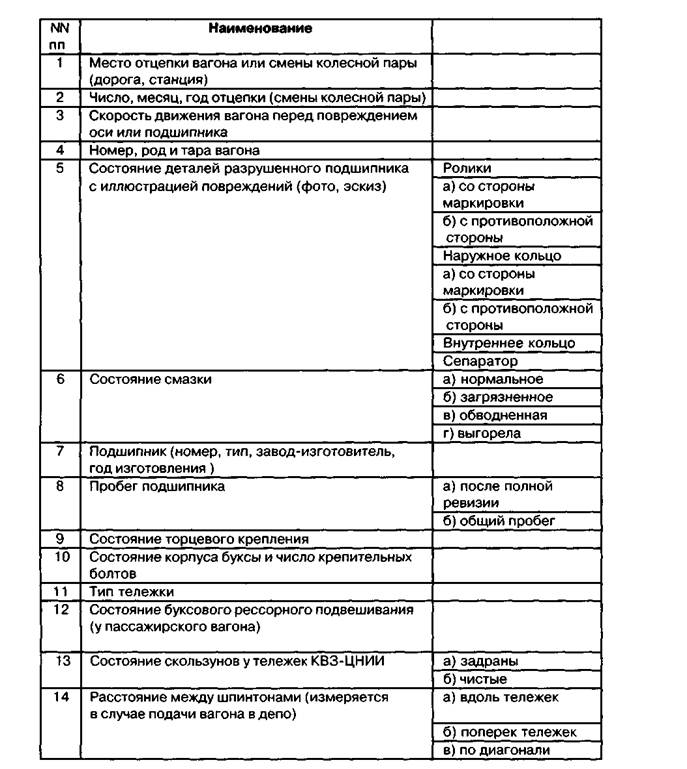
Приложение 5. План расследования причин излома шейки оси роликовой колесной пары или разрушения буксового узла.
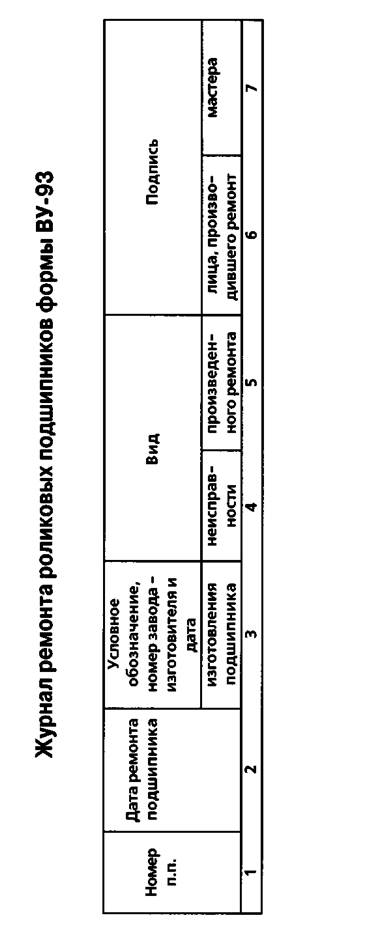
Приложение 4. Журнал ремонта роликовых подшипников формы ВУ-93
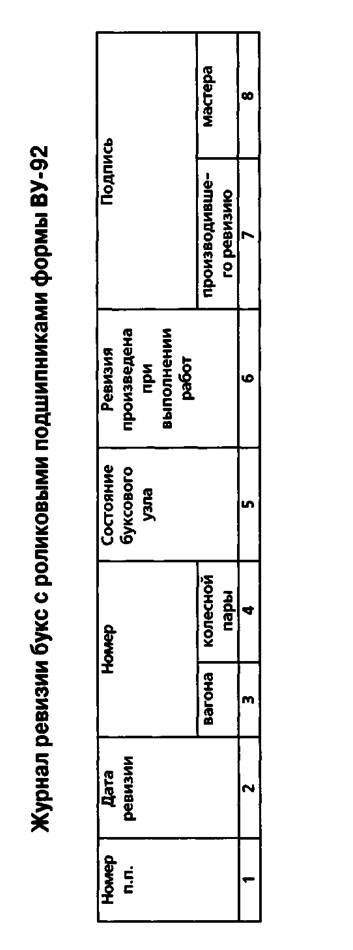
Приложение 3. Журнал ревизии букс с роликовыми подшипниками формы ВУ-92
Приложение 2. Журнал осмотра роликовых подшипников и корпусов букс формы ВУ-91
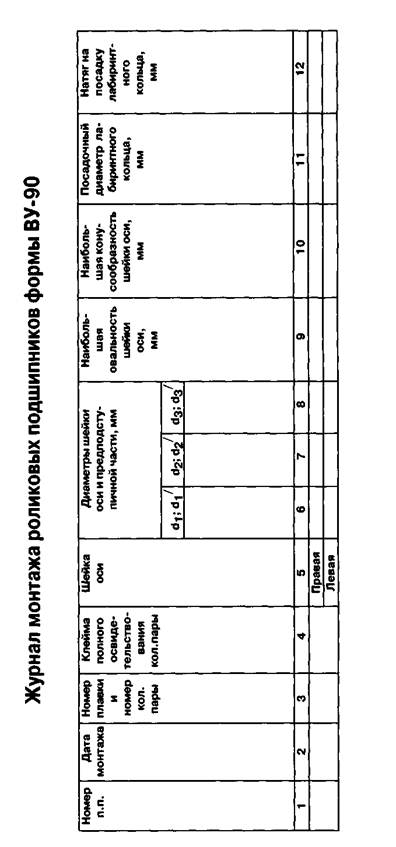
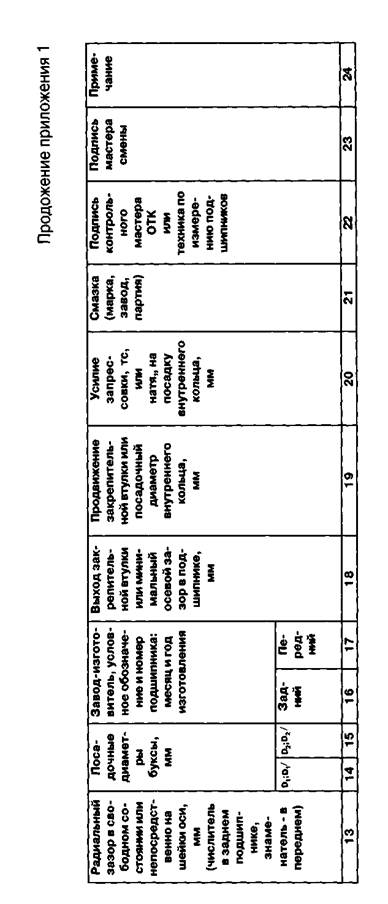
Приложение 1. Журнал монтажа роликовых подшипников формы ВУ-90.



1. Препарат-модификатор эМПи-1 предназначен для снижения износа, коэффициента трения и предотвращения задиров на трущихся поверхностях буксовых роликовых подшипников. ЭМПи-1 представляет собой присадку.
2. Препарат-модификатор эМПи-1 изготавливается по ТУ 0253-001 -25887352-97 на 000 «Фактория Л С» и поставляется на вагоноремонтные предприятия и вагоностроительные заводы по их заявкам.
3. Препарат-модификатор эМПи-1 используется на вагоноремонтных предприятиях МПС РФ и вагоностроительных заводах для смазывания буксовых подшипников колесных пар грузовых и пассажирских вагонов и применяется при полных ревизиях буксовых узлов для смазывания вместо индустриальных, веретенного и авиационного масел подшипников перед постановкой их в корпуса букс. Перед применением препарат-модификатор эМПи-1 необходимо взбалтывать для образования однородной смеси. Расход эМПи-1 на один подшипник составляет 35-40 мл. При смазывании проводится многократное проворачивание сепаратора с роликами в наружном кольце подшипника.
4. Заполнение подшипников консистентной смазкой и монтаж буксовых узлов производятся в установленном порядке.
Существуют растения, естественная устойчивость которых к гербицидам основана на детоксикации. Так, устойчивость растений к хлорсульфурону может быть связана с дезактивацией молекулы гербицида путем его гидроксилирования и последующего гликозилирования введенной гидроксильной группы. Создание растений, устойчивых к патогенам и вредителям Устойчивость растений к тем или иным патогенам чаще всего является сложным мультигенным признаком.
Одновременная передача нескольких локусов трудна даже методами генной инженерии, не говоря о классических методах селекции. Более простым является другой путь. Известно, что у устойчивых растений при атаке патогенов изменяется метаболизм. Накапливаются такие соединения, как Н2О2, салициловая кислота, фитоаллексины. Повышенный уровень этих соединений способствует противостоянию растения в борьбе с патогенами.
Вот один из примеров, доказывающий роль салициловой кислоты в иммунном ответе растений. Трансгенные растения табака, которые содержат бактериальный ген, контролирующий синтез салицилат гидролазы (этот фермент разрушает салициловую кислоту), были неспособны к иммунному ответу. Поэтому изменение генно-инженерным путем уровня салициловой кислоты или выработки в растениях в ответ на патоген Н2О2 может быть перспективным для создания устойчивых трансгенных растений.
В фитовирусологии широко известен феномен индуцированной перекрестной устойчивости растений к вирусным инфекциям. Сущность этого явления состоит в том, что заражение растения одним штаммом вируса предотвращает последующую инфекцию этих растений другим вирусным штаммом. Молекулярный механизм подавления вирусной инфекции пока неясен. Показано, что для иммунизации растений достаточно введения отдельных вирусных генов, например генов капсидных белков. Так, ген белка оболочки вируса табачной мозаики перенесли в клетки табака и получили трансгенные растения, у которых 0,1% всех белков листьев был представлен вирусным белком. Значительная часть этих растений при инфицировании вирусом не проявляла никаких симптомов заболевания. Возможно, что синтезирующийся в клетках белок оболочки вируса мешает вирусной РНК нормально функционировать и формировать полноценные вирусные частицы.Установлено, что экспрессия капсидного белка вируса табачной мозаики, вируса мозаики люцерны, вируса огуречной мозаики, Х-вируса картофеля в соответствующих трансгенных растениях (табак, томаты, картофель, огурцы, перцы) обеспечивает высокий уровень их защиты от последующей вирусной инфекции. Причем у трансформированных растений не отмечалось снижения фертильности, нежелательного изменения ростовых и физиологических характеристик исходных экземпляров и их потомства. Полагают, что индуцированная устойчивость растений к вирусам обусловлена особым антивирусным белком, очень похожим на интерферон животных. Представляется возможным методом генетической инженерии усилить экспрессию гена, кодирующего этот белок, путем его амплификации или подстановки под более сильный промотор.
Следует отметить, что использование генетической инженерии для защиты растений от различных патогенных микроорганизмов в значительной мере сдерживается недостаточностью знаний о механизмах защитных реакций растений. Для борьбы с насекомыми-вредителями в растениеводстве используются химические средства -- инсектициды. Однако они оказывают вредное влияние на млекопитающих, убивают и полезных насекомых, загрязняют окружающую среду, дороги, и кроме того, насекомые довольно скоро приспосабливаются к ним. Известно более 400 видов насекомых, устойчивых к используемым инсектицидам. Поэтому все большее внимание привлекают биологические средства борьбы, обеспечивающие строгую избирательность действия и отсутствие адаптации вредителей к применяемому биопестициду.
Уже довольно давно известна бактерия Bacillus thuringiensis, продуцирующая белок, являющийся очень токсичным для многих видов насекомых, в то же время безопасный для млекопитающих. Белок (дельта-эндотоксин, CRY-белок) продуцируется различными штаммами В. thuringiensis. Взаимодействие токсина с рецепторами строго специфично, что усложняет подбор комбинации токсин--насекомое. В природе найдено большое количество штаммов В. thuringiensis, чьи токсины действуют только на определенные виды насекомых. Препараты В. thuringiensis в течение десятилетий использовали для контроля насекомых на полях. Безопасность токсина и его составных белков для человека и других млекопитающих полностью доказана. Встраивание гена этого белка в геном растений дает возможность получить трансгенные растения, не поедаемые насекомыми.
Кроме видоспецифичности по действию на насекомых встраивание прокариотических генов дельта-токсинов в геном растений даже под контролем сильных эукариотических промоторов не привело к высокому уровню экспрессии. Предположительно такое явление возникло в связи с тем, что эти бактериальные гены содержат значительно больше адениновых и тиминовых нуклеотидных оснований, чем растительная ДНК. Эта проблема была решена путем создания модифицированных генов, где из природного гена вырезали и добавляли те или иные фрагменты с сохранением доменов, кодирующих активные части дельта-токсина. Так, например, с помощью таких подходов был получен картофель, устойчивый к колорадскому жуку. Получены трансгенные растения табака, способные синтезировать токсин. Такие растения были нечувствительны к гусеницам Manduca sexta. Последние погибали в течение 3 суток контакта с токсинпродуцирующими растениями. Токсинообразование и обусловленная им устойчивость к насекомым передавалась по наследству как доминантный признак.
В настоящее время так называемые Bt-растения (от В. thuringiensis) хлопка и кукурузы занимают основную долю в общем объеме генетически модифицированных растений этих культур, которые выращивают на полях США.
В связи с возможностями генной инженерии конструировать энтомопатогенные растения на основе токсина микробного происхождения еще больший интерес к себе вызывают токсины растительного происхождения. Фитотоксины являются ингибиторами белкового синтеза и осуществляют защитную функцию, направленную против насекомых-вредителей микроорганизмов и вирусов. Лучше всех среди них изучен рицин, синтезируемый в клещевине: его ген клонирован и установлена нуклеотидная последовательность. Однако высокая токсичность рицина для млекопитающих ограничивает генноинженерные работы с ним только техническими культурами, не используемыми в пищу человека и на корм животным. Токсин, вырабатываемый фитолаккой американской, эффективен против вирусов и безвреден для животных. Механизм его действия заключается в инактивации собственных рибосом при проникновении в клетки различного рода патогенов, в том числе фитовирусов. Пораженные клетки некротизируются, предотвращая размножение патогена и его распространение по растению. В настоящее время проводятся исследования по изучению гена этого белка и передаче его в другие растения.
· Повышение устойчивости растений к стрессовым условиям
Растения очень часто подвергаются воздействию различных неблагоприятных факторов окружающей среды: высокие и низкие температуры, недостаток влаги, засоление почв и загазованность среды, недостаток или, напротив, избыток некоторых минеральных веществ и т. д.
Устойчивость растений к тому или иному стрессовому фактору является результатом воздействия множества разных генов, поэтому говорить о полной передаче признаков толерантности от одного вида растения другому генноинженерными методами не приходится. Тем не менее у генетической инженерии имеются определенные возможности для повышения устойчивости растений. Это касается работы с отдельными генами, контролирующими метаболические ответы растений на стрессовые условия, например сверхпродукцию пролина в ответ на осмотический шок, на действие засоления, синтез особых белков в ответ на тепловой шок и т. д. Дальнейшее углубленное изучение физиологической, биохимической и генетической основы ответной реакции растения на условия среды, несомненно, позволит применять методы генетической инженерии для конструирования устойчивых растений.
Пока можно отметить лишь косвенный подход для получения морозоустойчивых растений, основанный на генноинженерных манипуляциях с Pseudomonas syringae. Этот микроорганизм, сосуществующий с растениями, способствует их повреждению ранними заморозками Механизм явления связан с тем, что клетки микроорганизма синтезируют особый белок, локализующийся во внешней мембране и являющийся центром кристаллизации льда. Известно, что формирование льда в воде зависит от веществ, которые могут служить центрами образования льда. Белок, вызывающий формирование кристаллов льда в различных частях растения (листья, стебли, корни), является одним из главных факторов, ответственных за повреждение тканей растений, чувствительных к ранним заморозкам. Многочисленные эксперименты в строго контролируемых условиях показали, что стерильные растения не повреждались заморозками вплоть до -- 6 -- 8° С, тогда как у растений, имеющих соответствующую микрофлору, повреждения возникали уже при температурах -- 1,5 -- 2° С. Мутанты этих бактерий, потерявшие способность синтезировать белок, вызывающий формирование кристаллов льда, не повышали температуру образования льда, и растения с такой микрофлорой были устойчивы к заморозкам. Штамм таких бактерий, распыленный над клубнями картофеля, конкурировал с обычными бактериями, что приводило к повышению морозоустойчивости растений. Возможно, такие бактерии, созданные с помощью методов генной инженерии и используемые в качестве компонента внешней среды, будут служить для борьбы с заморозками.
· Повышение эффективности биологической азотфиксации
Хорошо изучен фермент ответственный за восстановление молекулярного азота до аммония. -- нитрогеназа. Структура нитрогеназы одинакова у всех азотфиксирующих организмов. При фиксации азота непременным физиологическим условием является защита нитрогеназы от разрушения под действием кислорода. Лучше всех среди азотфиксаторов изучены ризобии, образующие симбиоз с бобовыми растениями, и свободноживущая бактерия Klebsiella pneumoniae. Установлено, что у этих бактерий за фиксацию азота ответственно 17 генов -- так называемых nif-генов. Все эти гены сцеплены друг с другом и расположены в хромосоме между генами ферментов биосинтеза гистидина и генами, определяющими усвоение шикимовой кислоты. У быстрорастущей ризобии nif-гены существуют в форме мегаплазмиды, содержащей 200--300 тысяч пар нуклеотидов.
Среди генов азотфиксации выявлены гены, контролирующие структуру нитрогеназы, белковый фактор, принимающий участие в транспорте электронов, регуляторные гены. Регуляция генов азотфиксации довольно сложна, поэтому генноинженерный перенос азотфиксирующей функции от бактерий непосредственно высшим растениям в настоящее время уже не обсуждается. Как показали эксперименты, даже в самом простом эукариотическом организме -- дрожжах не удалось добиться экспрессии nif-генов, хотя они и сохранялись в течение 50 генераций.
Эти опыты показали, что диазотрофность (азот-фиксация) свойственна исключительно прокариотическим организмам, и nif-гены не смогли преодолеть барьер, разделяющий прокариоты и эукариоты, из-за слишком сложной своей структуры и регуляции генами, расположенными вне nif-области. Возможно, более удачным окажется перенос nif-генов с помощью Ti-плазмид в хлоропласты, поскольку механизмы экспрессии генов в хлоропластах и в клетках прокариот близки. В любом случае нитрогеназа должна быть защищена от ингибирующего действия кислорода. Кроме того, фиксация атмосферного азота -- очень энергоемкий процесс. Вряд ли растение под влиянием nif-генов может так кардинально изменить свой метаболизм, чтобы создать все эти условия. Хотя не исключено, что в будущем методами генетической инженерии можно будет создать более экономно работающий нитрогеназный комплекс.
Более реально использование генноинженерных методов для решения следующих задач: повышение способности ризобии колонизировать бобовые растения, повышение эффективности фиксации и ассимиляции азота путем воздействия на генетический механизм, создание новых азотфиксирующих микроорганизмов путем введения в них nif-генов, передача способности к симбиозу от бобовых растений к другим.
Первостепенной задачей генетической инженерии для повышения эффективности биологической фиксации азота является создание штаммов ризобии с усиленной азотфиксацией и колонизирующей способностью. Колонизация бобовых растений ризобиями протекает очень медленно, лишь единичные из них дают начало клубенькам. Это происходит потому, что местом инвазии ризобии является только одна небольшая область между точкой роста корня и ближайшим к ней корневым волоском, находящимся на стадии формирования. Все остальные части корня и развившиеся корневые волоски растения нечувствительны к колонизации. В ряде случаев сформировавшиеся клубеньки оказываются неспособными фиксировать азот, что зависит от многих растительных генов (выявлено не менее пяти), в частности от неблагоприятного сочетания двух рецессивных генов.
Традиционными методами генетики и селекции удалось получить лабораторные штаммы ризобий с более высокой колонизирующей способностью. Но они в полевых условиях испытывают конкуренцию со стороны местных штаммов. Повышение их конкурентоспособности, видимо, можно осуществить генноинженерными методами. Повышение эффективности процесса азотфиксации возможно применением генноинженерных приемов, основанных на увеличении копий гена, усилении транскрипции тех генов, продукты которых образуют «узкое» место в каскадном механизме азотфиксации, путем введения более сильных промоторов и т. п. Важно повышение коэффициента полезного действия самой нитро-геназной системы, осуществляющей непосредственное восстановление молекулярного азота в аммиак.
· Повышение эффективности фотосинтеза
С4-растения характеризуются высокими темпами роста и скоростью фотосинтеза, у них практически отсутствует видимое фотодыхание. У большинства сельскохозяйственных культур, относящихся к С3-растениям, высокая интенсивность фотодыхания. Фотосинтез и фотодыхание -- тесно связанные процессы, в основе которых лежит бифункциональная активность одного и того же ключевого фермента -- рибулозобисфосфат-карбоксилазы (РуБФК). РуБФ-карбоксилаза может присоединять не только С02, но и 02, то есть осуществляет реакции карбоксилирования и оксигенирования. При оксигенировании РуБФ образуется фосфогликолат, который служит основным субстратом фотодыхания -- процесса выброса С02 на свету, в результате чего теряется часть фотосинтетических продуктов. Низкое фотодыхание у С4-растений объясняется не отсутствием ферментов гликолатного пути, а ограничением оксигеназной реакции, а также реассимиляцией С02 фотодыхания.
Одной из задач, стоящих перед генетической инженерией, является исследование возможности создания РуБФК с преобладающей карбоксилазной активностью.
Получение растений с новыми свойствами
В последние годы ученые используют новый подход для получения трансгенных растений с "antisense RNA" (перевернутой или антисмысловой РНК), который позволяет управлять работой интересуемого гена. В этом случае при конструировании вектора копию ДНК (к-ДНК) встраиваемого гена переворачивают на 180°. В результате в трансгенном растении образуется нормальная молекула мРНК и перевернутая, которая в силу комплементарности нормальной мРНК образует с ней комплекс и закодированный белок не синтезируется.
Такой подход использован для получения трансгенных растений томатов с улучшенным качеством плодов. Вектор включал к-ДНК гена PG, контролирующего синтез полигалактуроназы - фермента, участвующего в разрушении пектина, основного компонента межклеточного пространства растительных тканей. Продукт гена PG синтезируется в период созревания плодов томатов, а увеличение его количества приводит к тому, чтотоматы становятся более мягкими, что значительно сокращает срок их хранения. Отключение этого гена в трансгенах позволило получить растения томатов с новыми свойствами плодов, которые не только значительно дольше сохранялись, но и сами растения были более устойчивы к грибным заболеваниям.
Такой же подход можно применить для регулирования сроков созревания томатов, а в качестве мишени в этом случае используют ген EFE (ethylene-forming enzyme), продуктом которого является фермент, участвующий в биосинтезе этилена. Этилен - это газообразный гормон, одной из функций которого является контроль за процессом созревания плодов.
Cтратегия антисмысловых конструкций широко применима для модификации экспрессии генов. Эта стратегия используется не только для получения растений с новыми качествами, но и для фундаментальных исследований в генетике растений. Следует упомянуть еще об одном направлении в генной инженерии растений, которое до недавнего времени в основном использовали в фундаментальных исследованиях - для изучения роли гормонов в развитии растений. Суть экспериментов заключалась в получении трансгенных растений с комбинацией определенных бактериальных гормональных генов, например только iaaM или ipt т.д. Эти эксперименты внесли существенный вклад в доказательство роли ауксинов и цитокининов в дифференцировке растений.
В последние годы этот подход стали использовать в практической селекции. Оказалось, что плоды трансгенных растений с геном iaaM, находящимся под промотором гена Def (ген, который экспрессируется только в плодах), являются партенокарпическими, то есть сформировавшимися без опыления. Партенокарпические плоды характеризуются либо полным отсутствием семян, либо очень небольшим их количеством, что позволяет решить проблему "лишних косточек", например в арбузе, цитрусовых и т.д. Уже получены трансгенные растения кабачков, которые в целом не отличаются от контрольных, но практически не содержат семян.
Обезоруженную, лишенную онкогенов Ti-плазмиду ученые активно используют для получения мутаций. Этот метод носит название Т-ДНК-инсерционного мутагенеза. Т-ДНК, встраиваясь в геном растения, выключает ген, в который она встроилась, а по утрате функции можно легко отбирать мутанты (явление сайлесинга - замолкания генов). Этот метод замечателен также тем, что позволяет сразу обнаружить и клонировать соответствующий ген. В настоящее время таким способом получено множество новых мутаций растений и соответствующие гены клонированы. М. А. Раменской на основе Т-ДНК мутагенеза получены растения томатов с неспецифической устойчивостью к фитофторозу. Не менее интересен и другой аспект работ - получены трансгенные растения с измененными декоративными свойствами.