Вычисление массы вещества по известному количеству другого вещества, участвующего в реакции.
Пример: Вычислите массу алюминия, необходимого для получения оксида алюминия количеством вещества 8 моль.
| Последовательность выполнения действий | Оформление решения задачи |
| 1. Записать условие задачи | Дано: ν(Al2O3)=8моль ___________ Найти: m(Al)=? |
| 2. Вычислить молярные массы веществ, о которых, идёт речь в задаче | М(Al)=27г/моль M(Al2O3)=102г/моль |
| 3. Запишем уравнение реакции и расставим коэффициенты | 4 Al + 3O2 = 2Al2O3 |
| 4. Над формулами веществ запишем количества веществ из условия задачи, а под формулами – стехиометрические коэффициенты, отображаемые уравнением реакции | 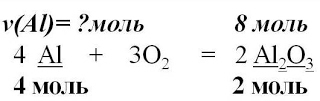
|
| 5. Вычислим количества вещества, массу которого требуется найти. Для этого составим соотношение. | 
|
| 6. Вычисляем массу вещества, которую требуется найти | m=ν∙M, m(Al)=ν(Al)∙M(Al)=16моль∙27г/моль=432г |
| 7. Записываем ответ | Ответ: m (Al)=432г. |
III. Используя алгоритм, решите самостоятельно следующие задачи:
1. Вычислите количество вещества сульфида натрия, если в реакцию с натрием вступает сера массой 12,8 г (2Na+S=Na2S).
2. Вычислите количество вещества образующейся меди, если в реакцию с водородом вступает оксид меди (II) массой 64 г (CuO + H2 =Cu + H2O).