Химические свойства моносахаридов.
Углеводы: моносахариды и их производные; дисахариды; полисахариды.
План
- Классификация углеводов.
- Циклические полуацетали моносахаридов ( пиранозы и фуранозы). Проэкционные формулы Фишера. Таутомерные формы моносахаридов. Мутаротация.
- Стереохимические ((D и L) ряды моносахаридов. Формулы Фишера.
- Реакционная способность моносахаридов. Препаративные методы идентификации моносахаридов и некоторых олиго- и полисахаридов.
- Образование гликозидов, их роль в образовании олиго- и полисахаридов, нуклеозидов, нуклеотидов и нуклеиновых кислот. Производные моносахаридов: дезоксисахариды и аминосахариды.
- Аскорбиновая кислота как производное гексоз, биологическая роль витамина С.
- Классификация дисахаридов по способности к ОВР. Сахароза и лактоза, мальтоза и целобиоза. Два типа связи между остатками моносахаридов и их влияние на реакционную способность дисахаридов.
- Строение (амилоза и амилопектин), гидролиз, биологическая роль и применение крахмала.
- Углеводный обмен в организме.
Углеводы (сахариды) – обширная группа соединений, которые входят в состав всех живых организмов и составляют по массе их основную часть. Они имеют значение как источник запасной энергии (крахмал, гликоген), как структурные элементы клеточных мембран (целлюлоза, хитин), как составная часть нуклеиновых кислот, витаминов, коферментов.
Классификация сахаридов. Все углеводы можно разделить по способности к гидролизу на простые (моносахариды) и сложные (полисахариды, олигосахариды и дисахариды).
Полисахариды подвергаются гидролизу и при этом образуются моносахариды. Моносахариды имеют обычно состав Сn(Н2O)n и являются гетерополифункциональными соединениями, в молекулах которых содержится одна карбонильная группа и несколько гидроксогрупп.
Моносахариды принято разделять на группы.
1) По длине углеродной цепи: пентозы, гексозы, триозы и т.д. Чаще всего встречаются С6(Н2О)6 или С5(Н2О)5
Например, глюкоза является гексозой, а рибоза – пентозой.
2) По расположению карбонильной группы: альдозы и кетозы. Составим структурные формулы для гексоальдозы и гексокетозы. Эти вещества являются структурными изомерами (по положению карбонильной группы). Например, глюкоза является гексоальдозой, а фруктоза – гескокетозой.
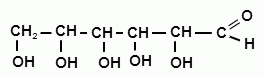
 Но гораздо чаще мы записываем формулы моносахаридов в виде вертикальных формул, которые принято называть формулами Фишера. Д
Но гораздо чаще мы записываем формулы моносахаридов в виде вертикальных формул, которые принято называть формулами Фишера. Д  ело в том, что для моносахаридов характерна оптическая изомерия, это еще один вид пространственной изомерии. Вы помните, что существуют пространственные изомеры (стереоизомеры) у веществ с двойной связью (цис- и транс-изомеры).
ело в том, что для моносахаридов характерна оптическая изомерия, это еще один вид пространственной изомерии. Вы помните, что существуют пространственные изомеры (стереоизомеры) у веществ с двойной связью (цис- и транс-изомеры).
3) Оптические изомеры (энантиомеры) относятся друг к другу как предмет и его зеркальное изображение. Они обладают центром ассиметрии – атомом углерода, который связан с четырьмя разными заместителями, и через молекулу нельзя провести плоскость симметрии. Все физические свойства оптических изомеров одинаковы, кроме одного: они вращают плоскость поляризованного света, проходящего через слой вещества, на один и тот же угол, но в противоположных направлениях. Правое вращение обозначают знаком (+) , а левое знаком (-).
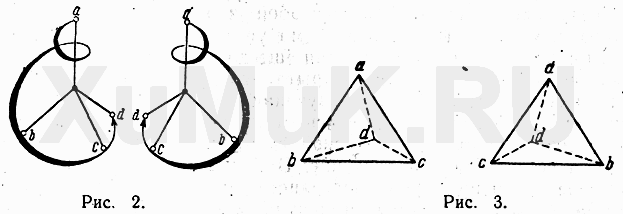 При обычном излучении колебания векторов электрического поля происходит в разных направлениях, перпендикулярно направлению распространения светового луча. При прохождении света через поляризатор (специальная призма, которая пропускает только определенные волны) свет становиться поляризованным (т.е. вектор электрического поля колеблется только в одной плоскости). При прохождении такого света через оптически активное вещество у лучей возникает разность фаз, и в результате на выходе плоскость поляризации будет отклонена от своего первоначального положения на определенный угол. Величину и направление отклонения (вправо или влево) нельзя предсказать, они определяются экспериментально.
При обычном излучении колебания векторов электрического поля происходит в разных направлениях, перпендикулярно направлению распространения светового луча. При прохождении света через поляризатор (специальная призма, которая пропускает только определенные волны) свет становиться поляризованным (т.е. вектор электрического поля колеблется только в одной плоскости). При прохождении такого света через оптически активное вещество у лучей возникает разность фаз, и в результате на выходе плоскость поляризации будет отклонена от своего первоначального положения на определенный угол. Величину и направление отклонения (вправо или влево) нельзя предсказать, они определяются экспериментально.
Химические свойства стереоизомеров тоже одинаковы, но в реакциях с другими оптически активными соединениями оптические изомеры могут вести себя по-разному. Это явление называется стереоспецифичностью, именно с этим явлением связана высокая избирательность действия ферментов и др. биоорганических соединений.К таким оптически активным веществам относятся многие липиды, все α –аминокислоты, все моносахариды и т.д..
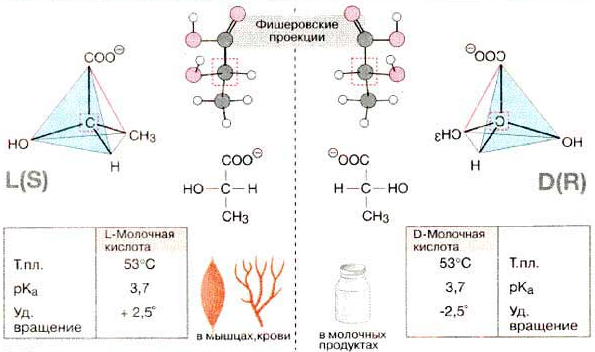 Например, все реакции в организме протекают с участием ферментов. Все ферменты имеют белковую природу и построены из L- α –аминокислот. Поэтому ферментативные биохимические процессы обладают высокой стереоспецифичностью. Например: Замена D –глюкозы на L-глюкозу приводит к невозможности процесса спиртового брожения с участием дрожжей. Или при скисании молока образуется D-молочная кислота, которая является «зеркальным отражением» той молочной кислоты, которая образуется при гликолизе в организме человека.
Например, все реакции в организме протекают с участием ферментов. Все ферменты имеют белковую природу и построены из L- α –аминокислот. Поэтому ферментативные биохимические процессы обладают высокой стереоспецифичностью. Например: Замена D –глюкозы на L-глюкозу приводит к невозможности процесса спиртового брожения с участием дрожжей. Или при скисании молока образуется D-молочная кислота, которая является «зеркальным отражением» той молочной кислоты, которая образуется при гликолизе в организме человека.

 Если в молекуле есть центр асимметрии (оптический центр), то чтобы отличить оптические изомеры, их изображают с помощью формул Фишера. Для этого углеродная цепь записывается вертикально, причем главная функциональная группа должна быть как можно выше. Счет атомов идет сверху. Слева и справа от атомов углерода пишут атом водорода или заместитель (гидроксогруппу, аминогруппу), причем для экономии времени и места атомы углерода и водорода могут не изображаться. Договорились ориентиром в мире стереизомеров выбрать глицериновый альдегид. У него только один оптический центр и два оптических изомера. Принято считать, что если заместитель находится у ассиметричного атома справа, то оптический изомер принадлежит к D –оптическому ряду, если слева – то к L. Для глицеринового альдегида D- изомер (+) – вращает поляризованный луч света вправо. Отсюда и обозначение. Но знак вращения поляризованного света не связан с принадлежностью к тому или другому ряду. Он определяется экспериментально. А относительная конфигурация всех веществ определяется по глицериновому альдегиду. Например, природные α-аминокислоты принадлежат к L-ряду.
Если в молекуле есть центр асимметрии (оптический центр), то чтобы отличить оптические изомеры, их изображают с помощью формул Фишера. Для этого углеродная цепь записывается вертикально, причем главная функциональная группа должна быть как можно выше. Счет атомов идет сверху. Слева и справа от атомов углерода пишут атом водорода или заместитель (гидроксогруппу, аминогруппу), причем для экономии времени и места атомы углерода и водорода могут не изображаться. Договорились ориентиром в мире стереизомеров выбрать глицериновый альдегид. У него только один оптический центр и два оптических изомера. Принято считать, что если заместитель находится у ассиметричного атома справа, то оптический изомер принадлежит к D –оптическому ряду, если слева – то к L. Для глицеринового альдегида D- изомер (+) – вращает поляризованный луч света вправо. Отсюда и обозначение. Но знак вращения поляризованного света не связан с принадлежностью к тому или другому ряду. Он определяется экспериментально. А относительная конфигурация всех веществ определяется по глицериновому альдегиду. Например, природные α-аминокислоты принадлежат к L-ряду.
К D- ряду относятся моносахариды у которых группа ОН у хирального углерода с наибольшим номером находится справа, к L- ряду - слева. Молекулы моносахаридов обычно содержат несколько ассиметричных атомов (центров хиральности), что может служить причиной существования большого числа стереоизомеров, соответствующих одной и той же структурной формуле. Например, у гексоальдозы четыре асимметричных атома углерода, и число стереоизомеров будет 24. Если мы напишем все возможные варианты расположения водорода и гидроксогруппы относительно углеродной цепи альдогексозы, мы получим те 16 стереоизомеров, о которых говорилось выше. Причем среди них можно выделить 8 пар, которые являются зеркальными отражениями друг друга. Например, D- и L-глюкоза. Каждой альдогексозе одного оптического ряда соответствует энантиомер другого ряда. Подавляющее большинство природных моносахаридов принадлежит к D- ряду. Например, живые организмы «не узнают» и «не работают» с L-глюкозой.
3) По числу атомов в цикле: пиранозы (6) и фуранозы (5)
return false">ссылка скрытаВ пространстве молекулы моносахаридов могут принимать различную форму (свободное вращение вокруг одинарных связей) и замыкаться в циклы за счет взаимодействия карбонильной группы и одной из гидроксогрупп, Цикл обычно содержит 5 или 6 атомов.
Формулы Фишера неудобны для изображения циклов, поэтому пользуются формулами Хеуорса. В них циклы изображаются в виде плоских многоугольников, лежащих перпендикулярно плоскости рисунка. Атом кислорода в пиранозном цикле находится в дальнем правом углу, в фуранозном – за плоскостью рисунка. Символы углерода в цикле обычно не пишут. Все заместители, которые были слева в формуле Фишера, рисуют в формуле Хеуорса под плоскостью цикла, те, которые были справа – над плоскостью. У альдоз D- ряда группу СН2ОН располагают над плоскостью,
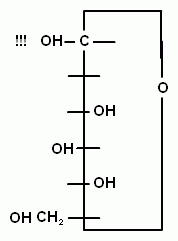 Циклические формы моносахаридов по химической природе являются циклическими полуацеталями (вспомните реакции присоединения спирта к альдегиду) .При замыкании цикла возможно образование еще двух оптических изомеров (аномеров), т.к. хиральных центров становится не 4, а 5.Та группа ОН, которая образовалась из карбоксильной группы при замыкании цикла, может оказаться либо над плоскостью молекулы (по одну сторону с шестым атомом углерода), либо под плоскостью. Если в формуле Хеуорса гидроксогруппа у первого атома углерода нарисована под плоскостью – это α-изомер, если над плоскостью – β. Образовавшуюся группу ОН называют гликозидной, она отличается по своим свойствам от других групп ОН. Счет атомов идет от атома кислорода по часовой стрелке.
Циклические формы моносахаридов по химической природе являются циклическими полуацеталями (вспомните реакции присоединения спирта к альдегиду) .При замыкании цикла возможно образование еще двух оптических изомеров (аномеров), т.к. хиральных центров становится не 4, а 5.Та группа ОН, которая образовалась из карбоксильной группы при замыкании цикла, может оказаться либо над плоскостью молекулы (по одну сторону с шестым атомом углерода), либо под плоскостью. Если в формуле Хеуорса гидроксогруппа у первого атома углерода нарисована под плоскостью – это α-изомер, если над плоскостью – β. Образовавшуюся группу ОН называют гликозидной, она отличается по своим свойствам от других групп ОН. Счет атомов идет от атома кислорода по часовой стрелке.


Важнейшие моносахариды: D-рибоза, D-глюкоза, D-маноза, D-галактоза, D - фруктоза.

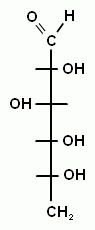


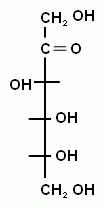
В твердом состоянии D- глюкоза имеет циклическое строение (либо α, либо β ), и эти аномеры отличаются углом вращения поляризованого света (+112о для α, и +19о для β ). При растворении любого из аномеров через некоторое время угол вращения становится равен +52,5о . Это явление называется «мутаротация». И причиной его является таутомерия, т.е. существование в растворе равновесной смеси всех возможных форм молекулы. И это означает, что в растворе циклы размыкаются и опять могут замыкаться, но иначе.
 В пространстве цикл может принимать разную форму. (Ведь в шестиграннике углы должны быть 1200, а в нашей молекуле они 109!) Ренгеноструктурным анализом установлено, что для глюкопиранозы наиболее выгодным является конформация «кресло», поэтому молекула глюкоза в реальности выглядит это приблизительно так:
В пространстве цикл может принимать разную форму. (Ведь в шестиграннике углы должны быть 1200, а в нашей молекуле они 109!) Ренгеноструктурным анализом установлено, что для глюкопиранозы наиболее выгодным является конформация «кресло», поэтому молекула глюкоза в реальности выглядит это приблизительно так:
Свойства моносахаридов, производные моносахаридов. Моносахариды представляют собой твердые вещества, легко растворимые в воде. Большинство (но не все!) имеют сладкий вкус. В свободном состоянии в природе встречается преимущественно D-глюкоза, кроме того, она входит в состав многих сложных сахаридов. В большом количестве глюкоза содержится в плодах, фруктах, но, кроме того, она является обязательным компонентом крови и тканей животных. Уровень глюкозы в крови постоянен (~0,1%), т.е. в крови взрослого человека содержится приблизительно 5-6 г глюкозы, этого достаточно на 15 мин его жизнедеятельности. Определенная концентрация глюкозы в крови поддерживается за счет нескольких процессов: синтез и гидролиз гликогена, глюконеогенез, окисление глюкозы, гидролиз полисахаридов пищи и организма и т.д. При некоторых заболеваниях нарушается обмен углеводов. При этом концентрация глюкозы в крови может превысить 10%. Другие моносахариды в основном известны как компоненты сложных 
 сахаридов.
сахаридов.
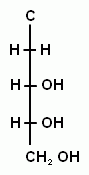
Дезоксисахара – это производные моносахаридов, у которых одна или две гидроксогруппы заменены на атом водорода. Например: D- рибоза и 2- дезоксирибоза.
Эти моносахариды входят в состав нуклеозидов.
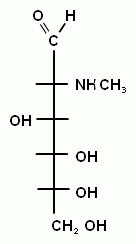 Аминосахара содержат вместо одной из гидроксогрупп – аминогруппу. Аминогруппа в свою очередь может быть ацилирована (водород замещен на остаток кислоты) или алкилирована (водород замещен на углеводородный радикал). Например, N-метил-L-глюкозамин, который входит в состав стрептомицина.
Аминосахара содержат вместо одной из гидроксогрупп – аминогруппу. Аминогруппа в свою очередь может быть ацилирована (водород замещен на остаток кислоты) или алкилирована (водород замещен на углеводородный радикал). Например, N-метил-L-глюкозамин, который входит в состав стрептомицина.
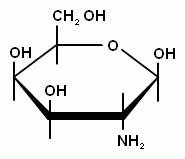
N-метил-D-глюкозамин D-галактозамин


Среди аминосахаров важное место занимает нейраминовая кислота и ее производные – сиаловые кислоты.
Эти кислоты содержатся в свободном состоянии в спинномозговой жидкости, являются компонентами специфических веществ крови, входят в состав ганглиозидов мозга.
 Аскорбиновая кислота (витамин С) структурно близка к моносахаридам. Она содержится во фруктах, цитрусовых, ягодах, овощах, молоке. Ее недостаток в пище вызывает различные заболевания, например, цингу. Суточная потребность составляет более 30 мг. Она относится к водорастворимым витаминам. В промышленности ее получают из глюкозы. Аскорбиновая кислота сильная (рК 4,2), обладает восстановительными свойствами. Этот процесс окисления-восстановления аскорбиновой кислоты протекает в организме, обеспечивая антиоксидантную роль этого витамина.
Аскорбиновая кислота (витамин С) структурно близка к моносахаридам. Она содержится во фруктах, цитрусовых, ягодах, овощах, молоке. Ее недостаток в пище вызывает различные заболевания, например, цингу. Суточная потребность составляет более 30 мг. Она относится к водорастворимым витаминам. В промышленности ее получают из глюкозы. Аскорбиновая кислота сильная (рК 4,2), обладает восстановительными свойствами. Этот процесс окисления-восстановления аскорбиновой кислоты протекает в организме, обеспечивая антиоксидантную роль этого витамина.
Химические свойства моносахаридов.
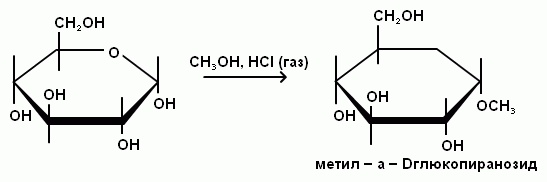 I. При взаимодействии гидроксогруппы моносахаридов со спиртами и фенолами образуются гликозиды. Механизм реакции похож на образование простых эфиров. Гликозиды легко подвергаются гидролизу разбавленными кислотами. Ферментативный синтез и гидролиз гликозидов очень специфичен. Эти реакции имеют важное значение в углеводном обмене, т.к. лежат в основе образования и гидролитического расщепления полисахаридов в организме человека. Легче всего эта реакция проходит для первого атома углерода.
I. При взаимодействии гидроксогруппы моносахаридов со спиртами и фенолами образуются гликозиды. Механизм реакции похож на образование простых эфиров. Гликозиды легко подвергаются гидролизу разбавленными кислотами. Ферментативный синтез и гидролиз гликозидов очень специфичен. Эти реакции имеют важное значение в углеводном обмене, т.к. лежат в основе образования и гидролитического расщепления полисахаридов в организме человека. Легче всего эта реакция проходит для первого атома углерода.
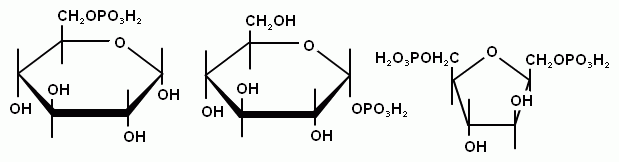 П. Моносахариды легко образуют сложные эфиры с кислотами с участием всех гидроксогрупп. Эти сложные эфиры подвергаются гидролизу в кислой и щелочной среде. Наибольшее значение для организма человека имеют эфиры фосфорной кислоты и глюкозы – глюкозофосфаты. Они содержаться во всех живых организмах, являются структурными элементами нуклеиновых кислот и коферментов. Метаболизм углеводов в организме, фотосинтез, брожение и другие биологические процессы осуществляются с участием фосфатов моносахаридов. Эфиры
П. Моносахариды легко образуют сложные эфиры с кислотами с участием всех гидроксогрупп. Эти сложные эфиры подвергаются гидролизу в кислой и щелочной среде. Наибольшее значение для организма человека имеют эфиры фосфорной кислоты и глюкозы – глюкозофосфаты. Они содержаться во всех живых организмах, являются структурными элементами нуклеиновых кислот и коферментов. Метаболизм углеводов в организме, фотосинтез, брожение и другие биологические процессы осуществляются с участием фосфатов моносахаридов. Эфиры 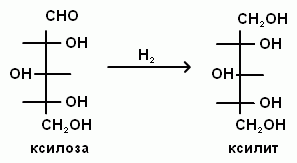 серной кислоты являются, структурными элементами соединительной ткани (хондроитинсульфаты).
серной кислоты являются, структурными элементами соединительной ткани (хондроитинсульфаты).
Ш. При восстановлении карбонильной группы из моносахаридов образуются многоатомные спирты. Например, глюкоза легко восстанавливается водородом (катализатор никель) до шестиатомного спирта сорбита:
СН2ОН-СНОН-СНОН-СНОН-СНОН-СН=О + Н2  СН2ОН-СНОН-СНОН-СНОН-СНОН-СН2ОН
СН2ОН-СНОН-СНОН-СНОН-СНОН-СН2ОН
Эти спирты - кристаллические вещества, легко растворимые и имеющие сладкий вкус. Они используются их как заменители сахара и для создания питательных сред в микробиологии (сорбит, маннит, ксилит и т.д.).
IV. Очень важной реакцией в химии моносахаридов является реакция окисления. В зависимости от условий при окислении моносахаридов образуются различные продукты.
А) Полное окисление заканчивается образованием углекислого газа и воды. Т.е. глюкоза может гореть, как и любое органическое вещество. И при этом выделяется значительное количество энергии.
В живых организмах глюкоза медленно окисляется под действием ферментов организма с участием кислорода (аэробное окисление) или без участия кислорода (анаэробное окисление или гликолиз).Это один из основных источников энергии для животных.
С6Н12О6 + О2 → СО2 + Н2О + Q
С6Н12О6 →  СН3-СНОН-СООН (молочная кислота) + Q
СН3-СНОН-СООН (молочная кислота) + Q
Б) Окисление в щелочной среде, как правило, сопровождается разрушением углеродной цепи. Например: альдозы могут в щелочной среде могут восстанавливать металлы из их соединений. В клинической практике для обнаружения альдоз пользуются реакциями Толленса («серебрянное зеркало») или Фелинга. При этом образуются различные продукты окисление углеводов и характерные продукты восстановления.
Глюкоза + Ag2O → Ag↓+ продукты окисления
Глюкоза + Cu(OH)2 → Cu2O↓ + продукты окисления
В) Окисление в нейтральной или кислой среде позволяет сохранить углеродный скелет моносахарида. В зависимости от условий реакции получают различные кислоты:
 1) если окислитель слабый – можно окислить альдегидную группу, не затрагивая концевую спиртовую, образуются гликоновые (альдоновые) кислоты.
1) если окислитель слабый – можно окислить альдегидную группу, не затрагивая концевую спиртовую, образуются гликоновые (альдоновые) кислоты.
2) если окислитель сильный, то окисляется и альдегидная группа и концевая спиртовая, образуются гликаровые (сахарные ) кислоты.
3) Если защитить альдегидную группу и окислить спиртовую у шестого атома углерода – образуются гликуроновые (уроновые) кислоты. Уроновые кислоты имеют очень важное значение для организма. Они входят в состав полисахаридов (гепарина, пектина). Уроновые кислоты выводят из организма посторонние и токсичные вещества через почки.
Г) Кроме того, возможен и процесс брожения – это окисление с помощью ферментов, которые вырабатываются микроорганизмами(грибками, бактериями). Различают спиртовое, молочнокислое и т.д. брожение. Например, спиртовое брожение происходит под действием ферментов, которые вырабатывают грибки дрожжи:
С6Н12О6  С2Н5ОН+ СО2
С2Н5ОН+ СО2
2) Как многоатомный спирт глюкоза вступает в реакции:
А) с гидроксидом меди (П), образуя растворимое соединение синего цвета. Эту реакцию вместе с реакцией Фелинга (окисление карбонильной группы) используют для определения глюкозы.
Получение глюкозы:
1) обычно – при гидролизе полисахаридов, например, крахмала (при кипячении в кислой среде);
2) в природе образуется в процессе фотосинтеза (в растениях) или глюконеогенеза (в животных).
СО2 + Н2О → С6Н12О6 + О2
V. Дегидратацияпроисходит при нагревании моносахаридов с сильными неорганическими кислотами (например, с серной концентрированной кислотой), происходит отщепление 3-х молекул воды от молекулы глюкозы. При этом образуются гетероциклические соединения, которые потом используют для получения лекарственных препаратов.
Применение глюкозы:
- в медицине при истощении, после болезни или операции (раствор глюкозы внутривенно);
- в текстильной промышленности как восстановитель при крашении тканей;
- в пищевой промышленности процессы брожения при производстве молочнокислых продуктов, пива, квашении овощей;
- силосование кормов в сельском хозяйстве.
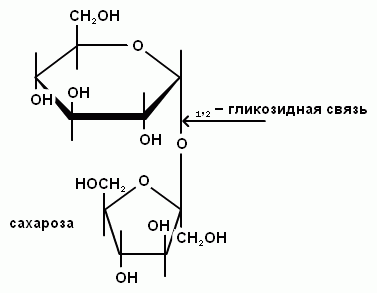 Дисахариды.Эти вещества состоят из двух моносахаридных звеньев. Между двумя молекулами моносахаридов образуется гликозидная связь. (см. первое хим. свойство моносахаридов). Образовавшаяся связь очень непрочная и, поэтому важнейшим химическим свойством дисахаридов является способность к гидролизу при нагревании в кислой среде с образованием моносахаридов.
Дисахариды.Эти вещества состоят из двух моносахаридных звеньев. Между двумя молекулами моносахаридов образуется гликозидная связь. (см. первое хим. свойство моносахаридов). Образовавшаяся связь очень непрочная и, поэтому важнейшим химическим свойством дисахаридов является способность к гидролизу при нагревании в кислой среде с образованием моносахаридов.
Например: сахароза + Н2О = α(D)глюкоза + (D)фруктоза
Другие распространенные дисахариды:
Мальтоза = α(D)глюкоза + α(D)глюкоза
Целлобиоза = β(D)глюкоза + β(D)глюкоза
Лактоза (молочный сахар) = α(D)глюкоза +(D)галактоза
Кроме свободных дисахаридов широко распространены дисахаридные фрагменты, входящие в состав множества гликозидов растительного и бактериального происхождения.
Существуют два типа связывания моносахаридных остатков:
1) за счет гликозидной ОН-группы одного и спиртовой группы другого (восстанавливающие сахара);
2) за счет гликозидных ОН-групп обоих моносахаридов (невосстанавливающие сахара).
К первой группе относятся мальтоза, лактоза, целлобиоза. Ко второй – сахароза. Сахароза не имеет альдегидной группы, поэтому для нее нехарактерны реакции ОВР. Она образует с гидроксидом меди раствор синего цвета (характерная реакция на многоатомные спирты), а в реакцию окисления с Cu(OH)2 не вступает.
 Сахароза(или сахар, как обычно называют это вещество), содержится во многих растениях. Больше всего ее в сахарной свекле (16-20%) и в сахарном тростнике (14-26%). Это бесцветное кристаллическое вещество, хорошо растворимое в воде. Температура плавления 1600С. Аморфная сахароза называется карамелью.
Сахароза(или сахар, как обычно называют это вещество), содержится во многих растениях. Больше всего ее в сахарной свекле (16-20%) и в сахарном тростнике (14-26%). Это бесцветное кристаллическое вещество, хорошо растворимое в воде. Температура плавления 1600С. Аморфная сахароза называется карамелью.
Применение: Пищевой продукт, пластификатор для пластмасс, производство лекарственных форм.
Полисахариды – высокомолекулярные вещества, представляющие собой продукты поликонденсации моносахаридов и их производных. По химической природе они являются полигликозидами, т.е. каждое звено моносахарида связано гликозидными связями с предыдущим и последующим звеном. Гликозидная природа обусловливает их легкий гидролиз в кислой среде и устойчивость в щелочной. Полный гидролиз приводит к образованию моносахаридов, неполный – к ряду промежуточных олигосахаридов и дисахаридов. Полисахариды имеют не только первичную структуру (т.е. последовательность мономерных остатков), но и вторичную – определенную форму макромолекулы в пространстве. Полисахариды могут быть гомополисахаридами (состоят из одинаковых остатков) и гетерополисахаридами (состоят из разных остатков). Гомополисахариды называют гликанами. К этой группе относятся многие полисахариды растительного (крахмал, целлюлоза, пектиновые вещества), животного происхождения (гликоген, хитин) и бактериального (декстраны) происхождения. Гетерополисахариды в организме обычно связаны с белками (протеогликаны).

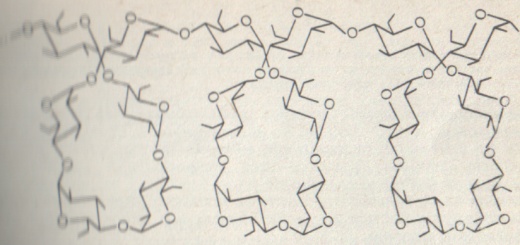 Крахмал. Это смесь двух гомополисахаридов, построенных из D-глюкозы: амилозы(10-20%) и амилопектина (80-90%). В амилозе остатки глюкозы связаны α-1,4-гликозидной связью, цепь неразветвленная, молекулярная масса 40-160 тыс. Макромолекула амилозы свернута в спираль, на каждый виток – шесть молекул моносахарида. В этот внутренний канал может входить подходящая по размеру молекула, например, молекула иода. Эту реакцию крахмала с иодом (образование комплекса, окрашенного в синий цвет) используют как качественную. Амилопектин имеет разветвленное строение, остатки глюкозы связаны α-1,4-гликозидной связью, а в местах разветвления - α-1,6-гликозидной связью. Молекулярная масса 1-6 млн.
Крахмал. Это смесь двух гомополисахаридов, построенных из D-глюкозы: амилозы(10-20%) и амилопектина (80-90%). В амилозе остатки глюкозы связаны α-1,4-гликозидной связью, цепь неразветвленная, молекулярная масса 40-160 тыс. Макромолекула амилозы свернута в спираль, на каждый виток – шесть молекул моносахарида. В этот внутренний канал может входить подходящая по размеру молекула, например, молекула иода. Эту реакцию крахмала с иодом (образование комплекса, окрашенного в синий цвет) используют как качественную. Амилопектин имеет разветвленное строение, остатки глюкозы связаны α-1,4-гликозидной связью, а в местах разветвления - α-1,6-гликозидной связью. Молекулярная масса 1-6 млн.

 Крахмал – белый порошок, в холодной воде он набухает и может раствориться частично в горячей воде. При быстром нагревании крахмала происходит частичный гидролиз, и образуются декстрины - осколки крахмала с меньшей молекулярной массой. При длительном кипячении в кислой среде происходит полный гидролиз крахмала и образуется глюкоза. Крахмал является основным источником глюкозы для человека. Процесс гидролиза протекает с участием амилазы слюны и панкреатической амилазы.
Крахмал – белый порошок, в холодной воде он набухает и может раствориться частично в горячей воде. При быстром нагревании крахмала происходит частичный гидролиз, и образуются декстрины - осколки крахмала с меньшей молекулярной массой. При длительном кипячении в кислой среде происходит полный гидролиз крахмала и образуется глюкоза. Крахмал является основным источником глюкозы для человека. Процесс гидролиза протекает с участием амилазы слюны и панкреатической амилазы.
Гликоген(животный крахмал) является структурным и функциональным аналогом растительного крахмала. По строению он подобен амилопектину, но имеет в 2 раза больше разветвлений, и молекулярная масса у него около 100 млн. Он практически нерастворим в воде. Гидролиз гликогена протекает очень легко и быстро, благодаря разветвленному строению. Благодаря очень большой массе молекула гликогена не может пройти через мембрану и остается в клетке в которой образовался, пока не возникнет потребность в энергии, источником которой является глюкоза. Уровень глюкозы в крови постоянен (~0,1%), т.е. в крови взрослого человека содержится приблизительно 5-6 г глюкозы, этого достаточно на 15 мин его жизнедеятельности. Определенная концентрация глюкозы в крови поддерживается в основном за счет процессов синтеза и гидролиза гликогена. После еды крахмал в течении часа подвергается гидролизу в кишечнике и в виде глюкозы всасывается в кровь. Уровень глюкозы резко повышается и инсулин дает команду к синтезу гликогена. Уровень «сахара», т.е. глюкозы опять возвращается к норме. Когда часть глюкозы, содержащейся в крови окислится, начнется гидролиз гликогена печени и уровень глюкозы в крови опять восстановится до нормы. При некоторых заболеваниях нарушается обмен углеводов. При этом концентрация глюкозы в крови может превысить 10% или резко уменьшится. Это заболевание называют диабетом.
Декстран – полисахарид бактериального происхождения. Он тоже построен из α-D-глюкопиранозных остатков, макромолекулы сильно разветвленные. Растворы декстранов используют как заменители плазмы крови, но большая молекулярная масса ( несколько млн) затрудняет их растворимость. Поэтому обычно используют гидролиз (кислотный или ультразвук), чтобы уменьшить их молекулярную массу и улучшить растворимость. Так получают «клинические декстраны», например, препарат «полиглюкин».

Целлюлоза (клетчатка) – наиболее распространенный растительный полисахарид. Структурной единицей целлюлозы является β-D-глюкопираноза, остатки связаны β-1,4-гликозидными связями. Макромолекулярная цепь целлюлозы не имеет разветвлений, молекулярная масса 400 000- 20 000 000. Целлюлоза не расщепляется пищеварительными ферментами человека, но она является необходимым для нормального питания балластным веществом. Она хорошо набухает, но не растворяется в воде. Заполняя кишечник, она вызывает его сокращения. Имея волокнистое строение, клетчатка адсорбирует на себе многие токсичные вещества и продукты метаболизма и выводит их из организма. Клетчаткой питаются микроорганизмы, которые живут в толстом кишечнике.
 Пектиновые вещества содержатся в плодах и овощах, для них характерно желеобразование в присутствии органических кислот. В основе пектинов лежит полигалактуроновая кислота, остатки D-галактуроновой кислоты связаны α-1,4-гликозидной связью. Некоторые пектиновые вещества обладают противоязвенным действием и являются основой ряда лекарственных препаратов, например, «плантаглюцид».
Пектиновые вещества содержатся в плодах и овощах, для них характерно желеобразование в присутствии органических кислот. В основе пектинов лежит полигалактуроновая кислота, остатки D-галактуроновой кислоты связаны α-1,4-гликозидной связью. Некоторые пектиновые вещества обладают противоязвенным действием и являются основой ряда лекарственных препаратов, например, «плантаглюцид».
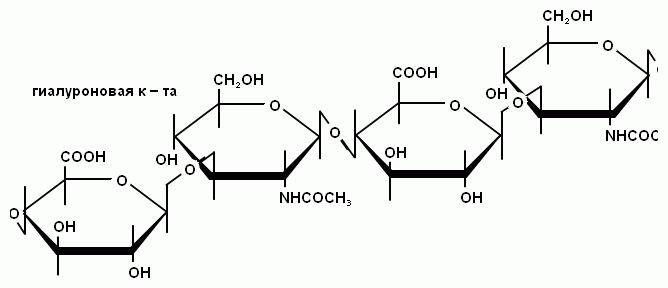 Полисахариды, входящие в состав соединительной ткани, обычно связаны с белками. Такие комплексы называют протеогликанами. Наиболее известные из них: хондроитинсульфаты (кожа, хрящи, сухожилия), гиалуроновая кислота (хрящи, пуповина, стекловидное тело, суставная жидкость), гепарин (печень). Эти полисахариды имеют неразветвленные цепи, которые построены из дисахаридных остатков (уроновые кислоты + N-ацетилгексозамин).
Полисахариды, входящие в состав соединительной ткани, обычно связаны с белками. Такие комплексы называют протеогликанами. Наиболее известные из них: хондроитинсульфаты (кожа, хрящи, сухожилия), гиалуроновая кислота (хрящи, пуповина, стекловидное тело, суставная жидкость), гепарин (печень). Эти полисахариды имеют неразветвленные цепи, которые построены из дисахаридных остатков (уроновые кислоты + N-ацетилгексозамин).
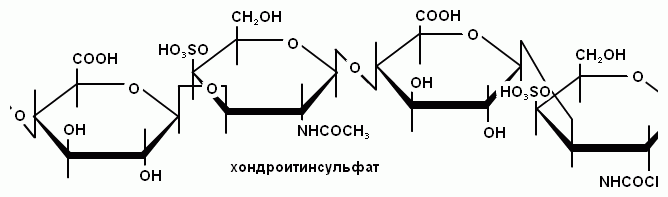 Хондроитинсульфаты кроме того имеют в своем составе остатки серной кислоты. Гиалуроновая кислота имеет высокую молекулярную массу ≈ 106, ее растворы обладают высокой вязкостью, обеспечивая барьерную функцию этой кислоты. Эти полисахариды в организме существуют в виде гелей и удерживают в своей коллоидной структуре большое количество воды. Комплексы гиалуроновой кислоты с хондроитинсульфатами представляют собой поливалентные анионы, способные связывать и удерживать в тканях катионы калия, натрия, кальция. Существуют и другие гетерополисахариды, подробнее о них – в курсе биохимии.
Хондроитинсульфаты кроме того имеют в своем составе остатки серной кислоты. Гиалуроновая кислота имеет высокую молекулярную массу ≈ 106, ее растворы обладают высокой вязкостью, обеспечивая барьерную функцию этой кислоты. Эти полисахариды в организме существуют в виде гелей и удерживают в своей коллоидной структуре большое количество воды. Комплексы гиалуроновой кислоты с хондроитинсульфатами представляют собой поливалентные анионы, способные связывать и удерживать в тканях катионы калия, натрия, кальция. Существуют и другие гетерополисахариды, подробнее о них – в курсе биохимии.