Жесткость воды и способы ее устранения.
Природная вода находится в непрерывном взаимодействии с окружающей средой. Она реагирует с атмосферой, почвой, растительностью, минералами и различными горными породами. При этом вода растворяет органические и неорганические соединения. Характер этого взаимодействия определяет состав природных вод, который поэтому принято оценивать такими технологическими показателями как жесткость, щелочность и солесодержание.
Жесткость воды (Ж) выражается числом миллимолярных масс эквивалента катионов Ca2+, Mg2+, Fe2+ или соответствующих им солей, содержащихся в 1 литре воды.
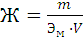 (мэкв/л),
(мэкв/л),
где
m – масса катиона металла или соответствующей соли, находящейся в воде, мг;
Эм – молярная масса эквивалента катиона металла или соответствующей соли, мг;
V – объем воды, л;
Жесткая вода мало пригодна к употреблению. В ней плохо пенится мыло, она неприменима в ряде технологических процессов, т.к. находящиеся в ней катионы металловобразуют труднорастворимые осадки со многими анионами. Жесткая вода образует в паровых котлах и котельных установках слой накипи. Накипь плохо проводит теплоту, вызывает увеличение расхода топлива и ускоряет изнашивание тепловых котлов и котельных установок.
Различают карбонатную жесткость (Жк) жесткость, обусловленную присутствием в воде гидрокарбонатов Ca, Mg, Fe, и некарбонатную жесткость (Жн), вызванную присутствием в воде сульфатов и хлоридов Ca и Mg. Общая жесткость воды равна сумме значений карбонатной и некарбонатной жесткости.
Жо=Жк+Жн
Карбонатную жесткость можно легко устранить даже кипячением, при котором катионы Ca2+ и Mg2+ удаляются, образуя нерастворимые осадки (CaCO3 и MgCO3), поэтому эту жесткость называют также временной.
Э(HCO3)2 → ЭCO3↓ + H2O + CO2, где Э – Ca2+, Mg2+, Fe2+.
Другой метод устранения карбонатной жесткости (метод известкования) - это добавление к воде гидроксида кальция Ca(OH)2 в количестве, необходимом для полного осаждения гидрокарбонатов:
Ca(HCO3)2 + Ca(OH)2 → 2CaCO3↓ + 2H2O
Mg(HCO3)2 + Ca(OH)2 → Mg(OH)2↓ + 2CaCO3↓ + H2O
Метод известкования непригоден для снижения некарбонатной жесткости. Для этой цели необходимо вводить карбонат натрия (сода), фосфат натрия или тетраборат натрия (бура):
Ca(HCO3)2 + Na2CO3 → CaCO3↓ + NaHCO3
CaSO4 + Na2CO3 → CaCO3↓ + Na2SO4
CaCl2 + Na2B4O7 → CaB4O7↓ + 2NaCl
3CaCl2 + 2Na3PO4 → Ca3(PO4)2↓ + 6NaCl
Ионы Ca2+и Mg2+ можно также удалить из воды посредством использования катионитов.
Карбонатная (временная) жесткость в лабораторных условиях определяется титрованием пробы воды стандартным раствором хлороводородной кислоты в присутствии метилоранжа.
Ca(HCO3)2 + 2HCl → CaCl2 + H2O + CO2↑
Расчет карбонатной жесткости, с учетом результатов титрования, проводится по формуле:
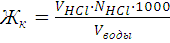 (мэкв/л)
(мэкв/л)
Некарбонатная (постоянная) жесткость рассчитывается по известным значениям общей и карбонатной жесткости:
Жн = Жо - Жк
Общая жесткость в лабораторных условиях определяется титрованием пробы воды стандартным раствором трилона – Б в присутствии индикатора хромогена черного. Расчет производится по формуле:
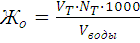 (мэкв/л),
(мэкв/л),
где VT и NT - объем и нормальность раствора трилона – Б.
Вода, жесткость которой имеет значение до 4 мэкв/л, считают мягкой, свыше 12 мэкв/л – очень жесткой.