Связью можно назвать ковалентную связь, образованную при перекрывании атомных орбиталей вне линии, соединяющей атомы.
Связью называют связь, возникающую при обобществлении электронных облаков двух атомов, если облака перекрываются по линии, соединяющей атомы.
Но в молекуле ацетилена в каждом из атомов углерода содержится еще по два р-электрона, которые не принимают участия в образовании σ-связей. Молекула ацетилена имеет плоский линейный «скелет», поэтому оба р-электронных облака в каждом из атомов углерода выступают из плоскости молекулы в перпендикулярном к ней направлении. В итоге, в молекуле ацетилена образуются еще две ковалентные С–С связи, называемые π-связями.
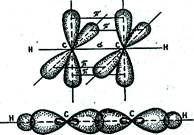
σ-связи являются более прочными, чем π-связи, чем объясняется большая реакционная способность непредельных углеводородов по сравнению с предельными.
Еще один вид гибридизации s- и р-орбиталей осуществляется в соединениях бора, алюминия или углерода (этилен, бензол). Возбужденный атом бора имеет три неспаренные электрона – один s- и два р-электрона. В этом случае при образовании соединений происходит sp2-гибридизация, при этом образуются три одинаковые sp2-гибридные орби-тали, расположенные под углом 120° друг к другу. Так, соединения ВF3, АlСl3, а также этилен и бензол имеют плоское строение, и все три связи В–F, например, в молекуле ВF3 расположены под углом 120° друг к другу.

Посредством образования sp2-гибридных орбиталей объясняются структуры непредельных углеводородов с двойными связями. Так, для молекулы этилена схематично можно изобразить следующую структуру.
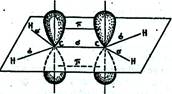
Двойные углерод–углеродные связи состоят из одной σ- и одной π-связи.
Энергия связи – энергия, необходимая для разрыва химической связи во всех молекулах, составляющих один моль вещества. Энергии ковалентных и ионных связей обычно велики и составляют величины порядка 100-800 кДж/моль.
Метод молекулярных орбиталей (ММО)– наиболее универсальный методом описания химической связи, в нем описывается состояние электрона в многоатомной системе, рассматривая молекулу как «многоядерный атом» в котором электроны заселяются по молекулярным орбиталям (рис.).
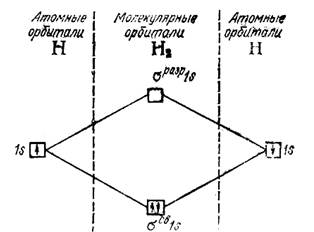
| Рис. Энергетическая схема образования молекулы водорода |