Принцип Паули или запрет Паули (1925 г.): в атоме не может быть двух электронов, обладающих одинаковыми свойствами.
Электронные конфигурации атомов
Так как при химических реакциях ядра реагирующих атомов остаются без изменения (за исключением радиоактивных превращений), то химические свойства атомов зависят от строения их электронных оболочек.
Выше показано, что состояние электронов можно описать набором четырех квантовых чисел, но для полного объяснения строения электронных оболочек атомов нужно знать еще три основных положения: 1) принцип Паули, 2) принцип наименьшей энергии и 3) правило Гунда.
Поскольку свойства электронов характеризуются квантовыми числами, принцип Паули часто формулируется так: в атоме не может быть двух электронов, у которых все четыре квантовых числа были бы одинаковы.
 Максимальное число электронов с одинаковым квантовым числом п выражается формулой: N = 2n2. Отсюда ясно, почему на первом энергетическом уровне может быть не больше 2 электронов, на втором – 8, на третьем – 18 и т. д. Первый энергетический уровень состоит из одного подуровня – 1s, второй, энергетический уровень – из двух подуровней – 2s и 2р, третий – из трех подуровней – 3s, 3р, 3d и т.д.).
Максимальное число электронов с одинаковым квантовым числом п выражается формулой: N = 2n2. Отсюда ясно, почему на первом энергетическом уровне может быть не больше 2 электронов, на втором – 8, на третьем – 18 и т. д. Первый энергетический уровень состоит из одного подуровня – 1s, второй, энергетический уровень – из двух подуровней – 2s и 2р, третий – из трех подуровней – 3s, 3р, 3d и т.д.).
 Состояние электрона в атоме водорода 1Н можно представить как 1s1
Состояние электрона в атоме водорода 1Н можно представить как 1s1
Строение электронной оболочки атома гелия 2Не можно представить как 1s2
 Третий электрон лития согласно принципу Паули уже не может находиться в состоянии 1s, а только в состоянии 2s:
Третий электрон лития согласно принципу Паули уже не может находиться в состоянии 1s, а только в состоянии 2s:
Строение электронных оболочек ряда атомов элементов второго периода периодической таблицы Менделеева:
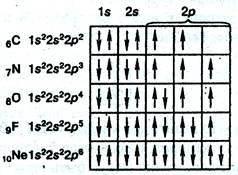
Приведенное расположение спинов определяется так называемым правилом Гунда (1927 г.).