ZnSО4 • 7Н2О М.м. 287,56г/моль
Белый купорос.
Цинка сульфат Zinci sulfas.
В природе цинк встречается в виде минералов галлия ZnСО3 и цинковой обманки ZnS. Цинк найден в мышечной, зубной нервной ткани организма человека. Применение соединений цинка в медицине основано на том, что цинк, как и некоторые другие тяжелые металлы, дает соединения с белками — альбуминаты, растворимые альбуминаты оказывают действие от слабо вяжущего до резко прижигающего. Нерастворимые альбуминаты обычно образуют пленку на тканевой поверхности и такиv образом способствуют заживлению ткани (подсушивающее действие).
Соединения цинка в больших дозах токсичны, при местном применении они могут быть использованы в качестве вяжущих и прижигающих средств, при введении внутрь соединения цинка вызывают рвоту.
Получение
Цинка сульфат получают растворением очищенного от примесей металлического цинка и разведенной серной кислоте:
Zn + H2SO4 → ZnSO4 + Н2↑
Из раствора кристаллизуют гептагидрат цинка сульфата (ZnSO4 •7H2O) при температуре 39-41 °С.
Свойства
Бесцветные прозрачные кристаллы или мелкокристаллический порошок без запаха, имеющий вяжущий металлический вкус. Выветривается на воздухе, а при 280°С полностью теряет кристаллизационную воду. Очень легко растворим в воде, медленно в глицерине. Его водные растворы имеют кислую реакцию среды, практически нерастворим в этаноле.
Химические свойства
Соединения цинка проявляют амфотерные свойства. При растворении цинка оксида в минеральных кислотах образует соли: сульфаты в серной кислоте, хлориды в хлористоводородной, нитраты в азотной:
ZnO + H2SO4 → ZnSO4 + H2O
ZnO + 2HCl →ZnCl2 + H2O
ZnO + 2HNO3 → Zn(NO3)2 + H2O
При растворении оксида цинка в избытке растворов гидроксидов щелочных металлов образуются растворимые в воде гидроксокомплексы:
ZnO + 2NaOH +H2O → Na2[Zn(OH)4]
При растворении в избытке аммиака образуется растворимая комплексная соль:
ZnO + 4NH4OН → [Zn(NH4)4](ОН)2 + 3Н2О
Подлинность.
Катион цинка доказывают официальными реакциями:
1. С натрия сульфидом по образованию белого осадка сульфида цинка, нерастворимого в уксусной кислоте, растворимого в минеральных кислотах:
ZnSO4 + Na2S → ZnS↓+Na2SO4
ZnS+HCl →ZnCl2+H2S↑
2. С гексацианоферратом (II) калия по образованию белого гелеобразного осадка комплексной соли, нерастворимого в кислотах, растворимого в растворах щелочей:
ZnSO4 + K4[Fe(CN)6] → K2Zn[Fe(CN)6]↓ + K2SO4
K2Zn[Fe(CN)6] + 4NaOH → Na2[Zn(OH)4] + K2Na2[Fe(CN)6]
3. Специфичной (не официальной) реакцией на цинк во всех его соединениях является реакция образования зелени Ринмана. Окись цинка прокаливается с нитратом кобальта, при этом получается характерное зеленое окрашивание — зелень Ринмана
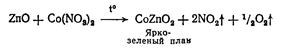
4. Сульфат-ион в цинка сульфате доказывают с бария хлоридом по образованию белого осадка бария сульфата, нерастворимого в кислотах и растворах щелочей:
ZnSO4 + ВаСl2 → BaSO4↓+ ZnCl2
Испытание на чистоту.
1. Устанавливают допустимые общие примеси: хлориды, мышьяк (с помощью эталонных растворов)
2. Недопустимые общие примеси
Ø железо, медь и алюминий обнаруживают по реакции с раствором аммиака (исследуемый раствор должен быть прозрачным и бесцветным);
Ø магний и кальций - по реакции с натрия гидрофосфатом (раствор должен остаться без изменений);
Ø нитриты - по реакции с дифениламином (на границе слоев не должно появляться голубое окрашивание);
Ø карбонаты - по реакции с кислотой хлористоводородной разведенной (не должно наблюдаться выделения пузырьков газа; раствор должен быть бесцветным и прозрачным).
3. Контролируют кислотность, визуально, с помощью рН индикаторов (метилового оранжевого или фенолфталеина).
Количественное определении
Трилонометрическим методом (по иону цинка), который основан на образовании прочных, бесцветных, хорошо растворимых комплексов металла с трилоном Б аналогично определению соединений магния и кальция), f = 1.

Хранение.
Препараты цинка хранят в хорошо укупоренной таре, цинка сульфат на воздухе теряет кристаллизационную воду. По списку Б.
Применение.
Цинка сульфат применяют в глазной практике при конъюнктивитах (0,1- 0,5% растворы), при ларингите (0,25-0,5% растворы для смазывания или пульверизации), внутрь для профилактики гипоцинкемии и рвотного средства.
Форма выпуска:
Субстанция, глазные капли в стеклянных флаконах и полиэтиленовых тюбиках-капельницах, мази, пасты, линименты.