ТИОСУЛЬФАТЫ
ПРИМЕНЕНИЕ АММИАКА
Гидролизом нитридов
Mg3N2 + H2O → Mg(OH)2 + NH3↑
1. Для производства азотной кислоты HNO3, аммиачной селитры NH4NO3, мочевины (карбамида) CO(NH2)2, соды по методу Сольве;
2. Аммиачная вода (25 %-й раствор аммиака в воде) и жидкий аммиак используют как удобрение;
3. В холодильной технике в качестве холодильного агента (R717) ;
4. 10 %-й раствор аммиака – нашатырный спирт применяют в медицине для выведения из обморочного состояния (дают вдыхать пары), для снятия сильного алкогольного опьянения путем индукции рвоты (3 капли на стакан воды внутрь), при укусах насекомых (в виде примочек);
5. Для получения синтетических волокон – найлона, капрона и др.;
6. В легкой промышленности при очистке и крашении хлопка, шерсти и шелка;
7. В производстве природного каучука аммиак помогает сохранить латекс в процессе его перевозки от плантации до завода;
8. В сталелитейной промышленности для азотирования – насыщения поверхностных слоев стали азотом, что значительно увеличивает ее твердость;
9. В быту раствор аммиака используется для выведения пятен.
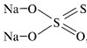 тиосульфат натрия
тиосульфат натрия
|
Тиосульфаты – это соли тиосерной кислоты H2S2O3. Нетоксичны.
Тиосерная кислота – бесцветная вязкая жидкость, не затвердевающая даже при очень низких температурах. Термически неустойчива. Быстро, но не мгновенно разлагается в воде.
Тиокислоты и тиосоли образуются при замещении атома кислорода на атом серы.
В молекуле тиосульфата степень окисления центрального атома серы – +4, бокового – 0.